Clear Sky Science · pt
Imagem de biomoléculas intercelulares usando indicadores de proteínas fluorescentes com âncoras lipid-PEG
Observando as Células Conversarem em Tempo Real
Nossos cérebros e corpos dependem de uma conversa química constante entre células. Íons e neurotransmissores transportam mensagens através de lacunas minúsculas, mas esses sinais rápidos e fugazes são difíceis de ver sem perturbá‑los. Este estudo apresenta uma maneira simples de “pintar” células vivas com sensores fluorescentes que se prendem à sua superfície externa, permitindo que os cientistas observem essas mensagens — especialmente íons de potássio e o neurotransmissor glutamato — ao vivo e em detalhe. 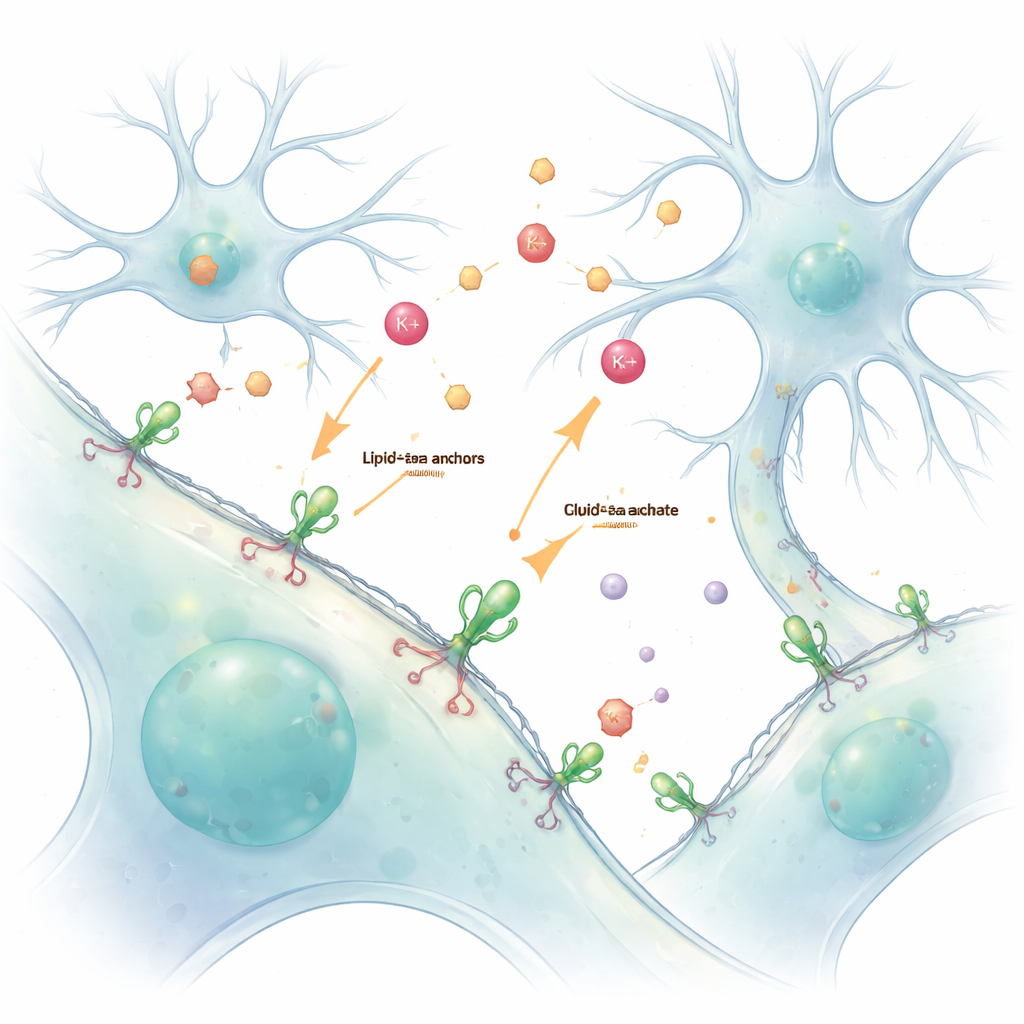
Uma Nova Forma de Marcar a Superfície Celular
Tradicionalmente, os pesquisadores modificam geneticamente as células para que produzam sensores de proteína fluorescente a partir de seu próprio DNA. Embora poderoso, esse método genético frequentemente posiciona mal os sensores dentro da célula, tornando difícil separar o que ocorre no interior daquilo que ocorre no exterior. Os autores resolveram isso usando um gancho químico chamado âncora lipid–PEG. Uma extremidade dessa molécula se insere na membrana externa, enquanto a outra extremidade é quimicamente ligada a um sensor de proteína fluorescente. Quando esses sensores preparados são simplesmente adicionados a células vivas, eles revestem espontaneamente a superfície externa, formando uma camada brilhante e estável que relata o que acontece no fluido circundante.
Transformando Potássio e Glutamato em Luz
A equipe adaptou dois indicadores fluorescentes existentes: GINKO2, que responde a íons de potássio, e R‑iGluSnFR1, que responde ao glutamato. Eles purificaram essas proteínas de bactérias e então anexaram as âncoras lipid–PEG. Em células humanas cultivadas, o sensor de potássio ancorado formou um contorno suave ao longo da superfície celular e clareou sempre que o potássio extracelular aumentava, voltando a escurecer quando os níveis caíam. Importante, suas propriedades de emissão de luz e sensibilidade corresponderam de perto ao sensor original não modificado em experimentos de tubo de ensaio, mostrando que a ancoragem não prejudicou seu desempenho. O mesmo ocorreu com o sensor de glutamato, que permaneceu responsivo após a ancoragem e destacou claramente o glutamato no espaço imediatamente fora das células.
Ouvindo Neurônios em Culturas e Fatias
Os pesquisadores então passaram para células nervosas do hipocampo de camundongo, uma região do cérebro importante para aprendizagem e memória. Eles revestiram esses neurônios com o sensor de glutamato ancorado em lipid–PEG e coraram o interior das mesmas células com um corante de cálcio separado que relata atividade elétrica. Usando microscopia por reflexão interna total, puderam observar flashes vermelhos de glutamato na superfície celular enquanto sinais verdes dentro das células reportavam disparos elétricos. Essa visão em duas cores mostrou que os sensores ancorados podiam acompanhar a liberação espontânea de neurotransmissor sem qualquer modificação genética dos próprios neurônios.
Mapeando Ondas Químicas no Tecido Cerebral
Em seguida, a equipe testou o método em fatias cerebrais agudas, que preservam a conectividade natural do hipocampo. Eles aplicaram o sensor de potássio ancorado às fatias e estimularam eletricamente as fibras nervosas. O sensor ancorado produziu aumentos de fluorescência claros e repetíveis após cada estímulo, enquanto sensores não ancorados rapidamente se difundiram e geraram sinais fracos e instáveis. Banhando as fatias em soluções com níveis conhecidos de potássio, e corrigindo pelo brilho tênue próprio do tecido, os autores construíram uma curva de calibração e estimaram concentrações reais de potássio extracelular. Os níveis basais foram cerca de 2,5 milimolar e subiram para aproximadamente 3,4 milimolar com estimulação moderada, alinhando‑se com medições clássicas por eletrodos. Sensores ancorados tanto para potássio quanto para glutamato revelaram como esses sinais se espalham de forma diferente: as mudanças de glutamato permaneceram próximas às sinapses ativas, enquanto os aumentos de potássio se estenderam por centenas de micrômetros, sugerindo efeitos mais amplos sobre a excitabilidade da rede. 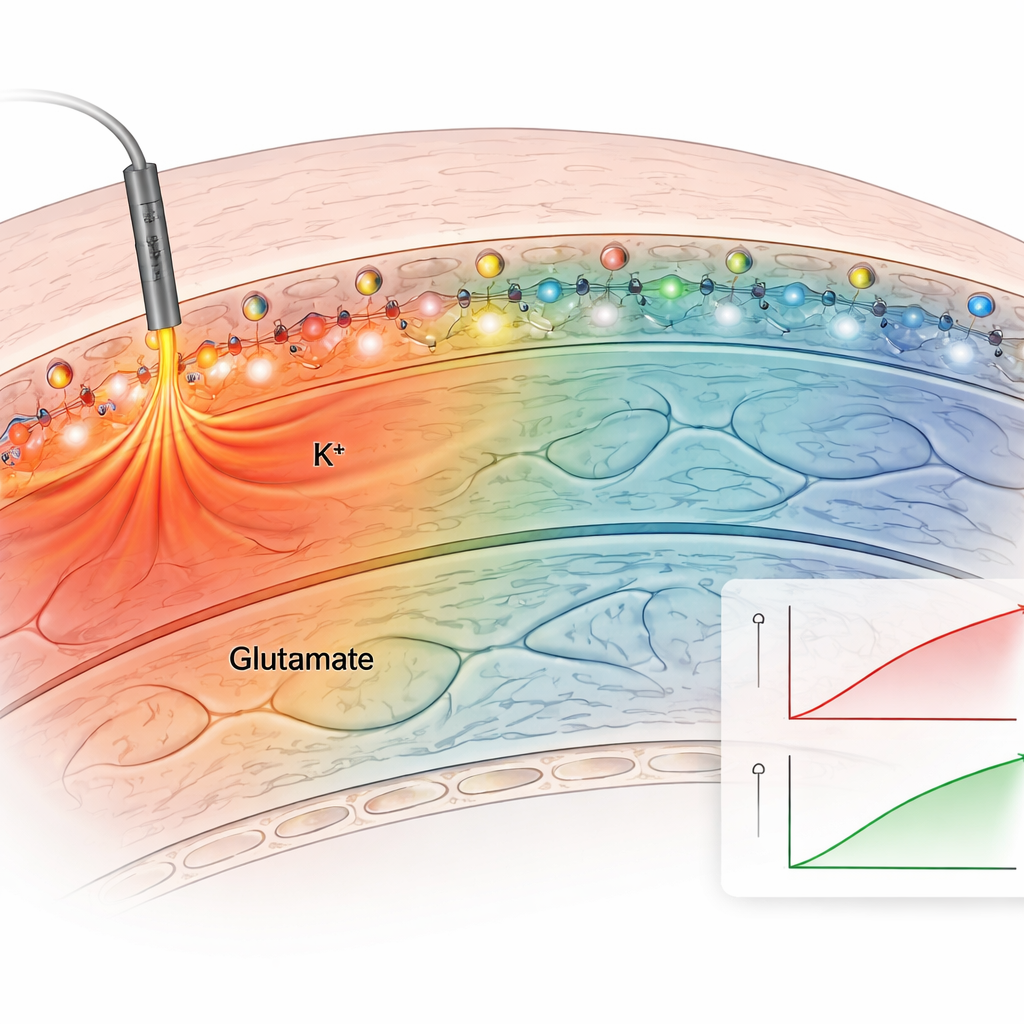
Investigando Como o Cérebro Limpa e Gera Sinais
Porque os sensores estão fixos na superfície celular, os autores puderam dissecar quais processos moldam essas ondas extracelulares. Bloquear transportadores de glutamato, que normalmente removem o glutamato, fez com que o sensor de glutamato ancorado exibisse sinais maiores e de duração mais longa, confirmando que a captação local limita a propagação do glutamato. Bloquear receptores de glutamato do tipo AMPA reduziu tanto as respostas elétricas quanto os sinais de potássio, indicando que a maior parte do aumento de potássio provém de neurônios pós‑sinápticos ativados pela entrada sináptica. Bloquear canais de sódio com tetrodotoxina quase aboliu as mudanças de potássio, vinculando‑as diretamente aos potenciais de ação. Juntos, esses experimentos ilustram como sensores ancorados podem transformar uma química complexa e distribuída em filmes e mapas intuitivos.
Por Que Isso Importa para Pesquisas Futuras do Cérebro
Para não especialistas, a mensagem principal é que este trabalho oferece uma forma rápida e não genética de revestir células e tecidos vivos com repórteres moleculares altamente sensíveis. Em vez de reengenheirar cada tipo celular, os cientistas podem adicionar proteínas sensoras pré‑fabricadas do exterior e visualizar imediatamente como íons e neurotransmissores mudam em tempo real na superfície celular. Essa abordagem melhora o controle, a reprodutibilidade e a precisão espacial, evitando os desafios da entrega gênica, especialmente em preparações delicadas como fatias cerebrais agudas. À medida que mais indicadores fluorescentes forem desenvolvidos para diferentes substâncias químicas, a mesma estratégia de ancoragem lipid–PEG poderá se tornar um conjunto de ferramentas amplamente usado para observar a linguagem química das células por todo o corpo.
Citação: Mita, M., Kiyosue, K. & Tani, T. Imaging intercellular biomolecules by using fluorescent protein indicators with lipid-PEG anchors. Sci Rep 16, 6964 (2026). https://doi.org/10.1038/s41598-026-37240-4
Palavras-chave: sinalização extracelular, biossensores fluorescentes, imagem de glutamato, dinâmica do potássio, neurônios do hipocampo