Clear Sky Science · pt
Convolução dinâmica em grafos com poda abrangente e classificação por GNN para detecção precisa de metástase em linfonodos
Por que pequenas alterações em linfonodos importam
Quando o câncer de mama se espalha, sua primeira parada costuma ser os linfonodos, pequenos filtros ao longo do sistema linfático. Detectar se células cancerígenas alcançaram esses linfonodos é um dos indícios mais importantes que os médicos usam para escolher cirurgia, quimioterapia e radioterapia. Ainda assim, até patologistas experientes podem deixar passar agrupamentos muito pequenos de células cancerosas em imagens digitais de microscópio, especialmente quando elas se parecem quase igual ao tecido saudável. Este estudo apresenta um novo quadro de inteligência artificial que trata o tecido como uma rede de regiões conectadas, permitindo detectar sinais sutis de disseminação com precisão notável.
Transformando imagens de tecido em redes
Os pesquisadores trabalham com lâminas digitais enormes de tecido corado, chamadas whole-slide images, provenientes de biópsias de linfonodos de câncer de mama. Essas imagens contêm milhões de pixels e uma mistura confusa de tipos celulares, cores e texturas. Para domar essa complexidade, a equipe primeiro limpa as imagens: normaliza brilho e cor, reduz ruído e gera cópias aumentadas rotacionando e espelhando patches, para que o computador aprenda a lidar com variações naturais. Cada patch da imagem é então dividido em pequenas regiões relativamente uniformes ("superpixels"), que se tornam os pontos — ou nós — em um grafo, enquanto as relações entre regiões vizinhas formam as linhas de conexão — ou arestas. Essa visão em rede preserva as formas e disposições irregulares do tecido real melhor do que métodos tradicionais baseados em grade.
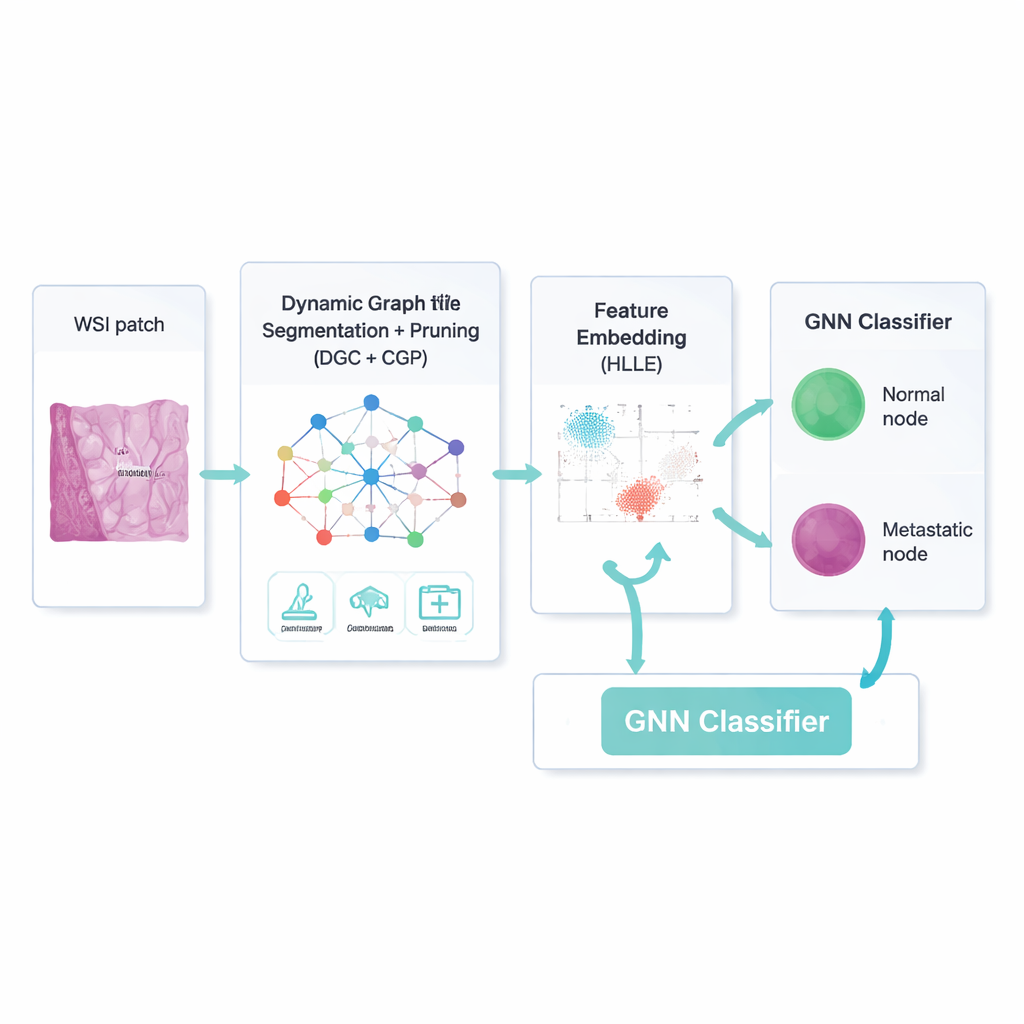
Uma maneira mais inteligente de focar no que importa
Construir uma rede por si só não basta; muitas conexões e características de imagem são irrelevantes ou mesmo enganosas. O quadro, portanto, usa um autoencoder convolucional dinâmico em grafos — um tipo de rede neural que aprende tanto como cada região se apresenta quanto como as regiões influenciam umas às outras. Um mecanismo adicional de "atenção" ensina o modelo a ponderar alguns canais de imagem mais do que outros, por exemplo enfatizando bordas na fronteira de um tumor. Ao mesmo tempo, uma estratégia chamada Comprehensive Graph Gradual Pruning poda gradualmente peças pouco úteis: conexões fracas entre regiões, características numéricas menos informativas e pesos de modelo de baixo impacto. Essa poda ocorre durante o treinamento, não depois, de modo que o sistema aprende a fazer mais com menos, terminando tanto mais rápido quanto mais fácil de interpretar.
Comprimir padrões sem perder sua forma
Depois que o modelo separa as regiões prováveis de linfonodo do tecido de fundo, ele ainda precisa descrever cada região de forma compacta, mas significativa. Para isso, os autores usam uma técnica chamada Hessian-based Locally Linear Embedding. Em termos simples, ela comprime muitas características numéricas em um conjunto menor tentando preservar a "forma" curva de como os exemplos reais se organizam no espaço de características — por exemplo, como micrometástases diferem de células do sistema imune normais ao longo de padrões sutis de textura ou cor. Essas descrições comprimidas tornam-se a entrada para um classificador por rede neural em grafos, que novamente opera sobre a rede de regiões e suas conexões depuradas, decidindo para cada nó se é metastático ou não.
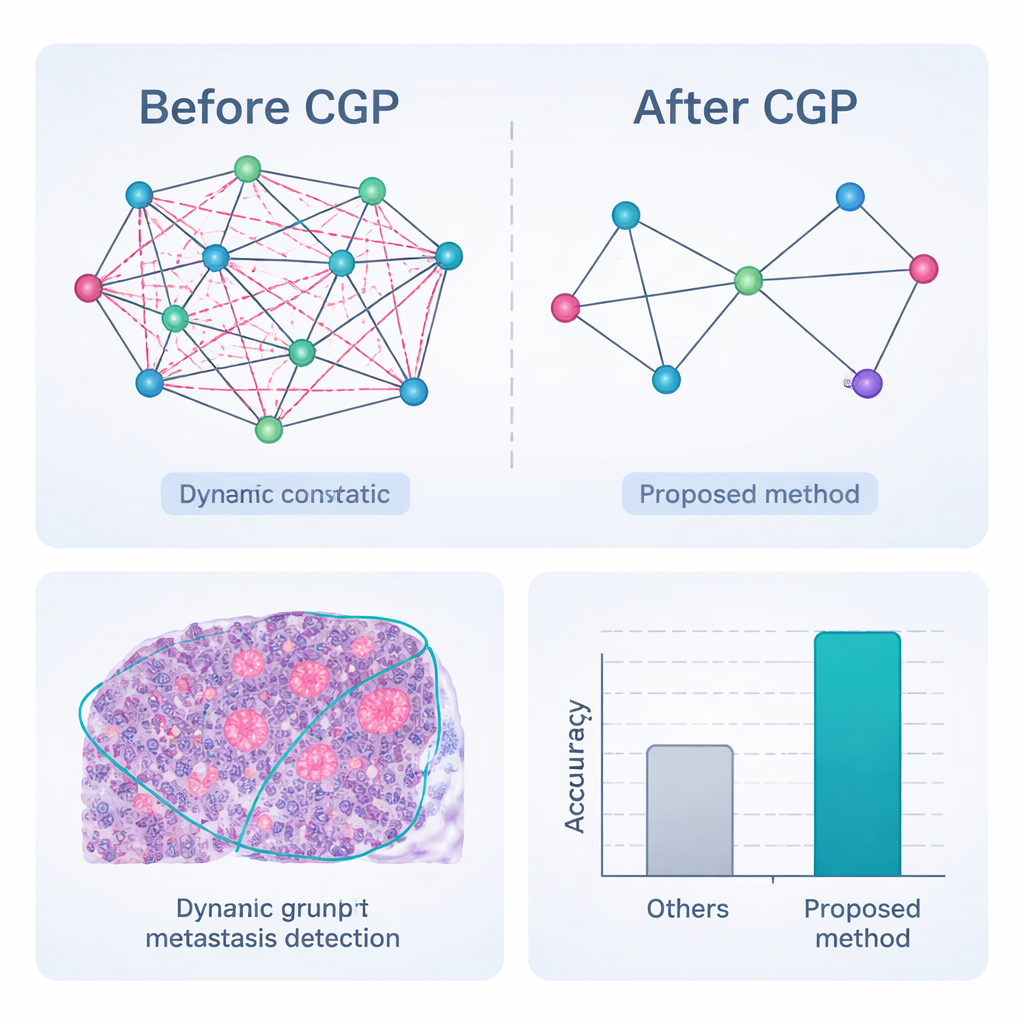
Submetendo o quadro ao teste
O pipeline completo — pré-processamento, segmentação dinâmica em grafos com poda, incorporação de características e classificação baseada em grafos — foi avaliado no CAMELYON17, uma coleção pública de 1.000 lâminas de linfonodos com anotações especializadas de pacientes com câncer de mama. Em comparação com uma série de fortes concorrentes de deep learning, incluindo redes convolucionais populares e modelos híbridos com transformers, o novo método alcançou as maiores pontuações em quase todas as métricas. Classificou corretamente os linfonodos como cancerosos ou não em 98,65% dos casos e apresentou melhor concordância com os contornos de tumor delineados por especialistas, especialmente para metástases muito pequenas ou tênues. Fundamentalmente, porque o grafo é podado de forma agressiva, o sistema obtém esses resultados com muito menos cálculos e menor uso de memória, tornando-o mais adequado para uso em tempo real em laboratórios de patologia movimentados.
O que isso significa para pacientes e clínicos
Na prática, este trabalho mostra como pensar o tecido como uma rede inteligentemente aparada de regiões conectadas pode ajudar computadores a atuar como leitores secundários extremamente cuidadosos de lâminas de linfonodo. Ao concentrar atenção e poder computacional nas estruturas mais informativas enquanto descarta ruído, o quadro é melhor em identificar pequenas sementes de câncer que poderiam passar despercebidas, e faz isso com eficiência suficiente para ser prático. Embora sejam necessárias validações clínicas adicionais, tais ferramentas poderiam auxiliar patologistas a tomar decisões mais rápidas e consistentes sobre a extensão da disseminação do câncer — informação que influencia diretamente planos de tratamento e, em última instância, os desfechos dos pacientes.
Citação: H. N., C., N., S., S., A.R. et al. Dynamic graph convolution with comprehensive pruning and GNN classification for precise lymph node metastasis detection. Sci Rep 16, 6682 (2026). https://doi.org/10.1038/s41598-026-37193-8
Palavras-chave: metástase em linfonodos, patologia digital, redes neurais em grafos, segmentação de imagens médicas, câncer de mama