Clear Sky Science · pt
Caracterização estrutural da ligação de metais na tirosilproteína sulfotransferase humana 2, TPST2
Por que íons metálicos minúsculos importam para a sinalização celular
Dentro de nossas células, incontáveis máquinas moleculares ajustam discretamente como os tecidos crescem, como hormônios atuam e como células imunes se comunicam. Uma dessas máquinas, uma enzima chamada TPST2, adiciona uma pequena etiqueta de sulfato a certas proteínas enquanto elas passam pelo centro de expedição celular, o aparelho de Golgi. Este estudo revela como íons metálicos simples como sódio e manganês ajudam a TPST2 a funcionar com mais eficiência ao rigidificar sutilmente partes de sua estrutura — um insight que pode ligar o equilíbrio mineral nas células ao câncer e a doenças relacionadas a hormônios. 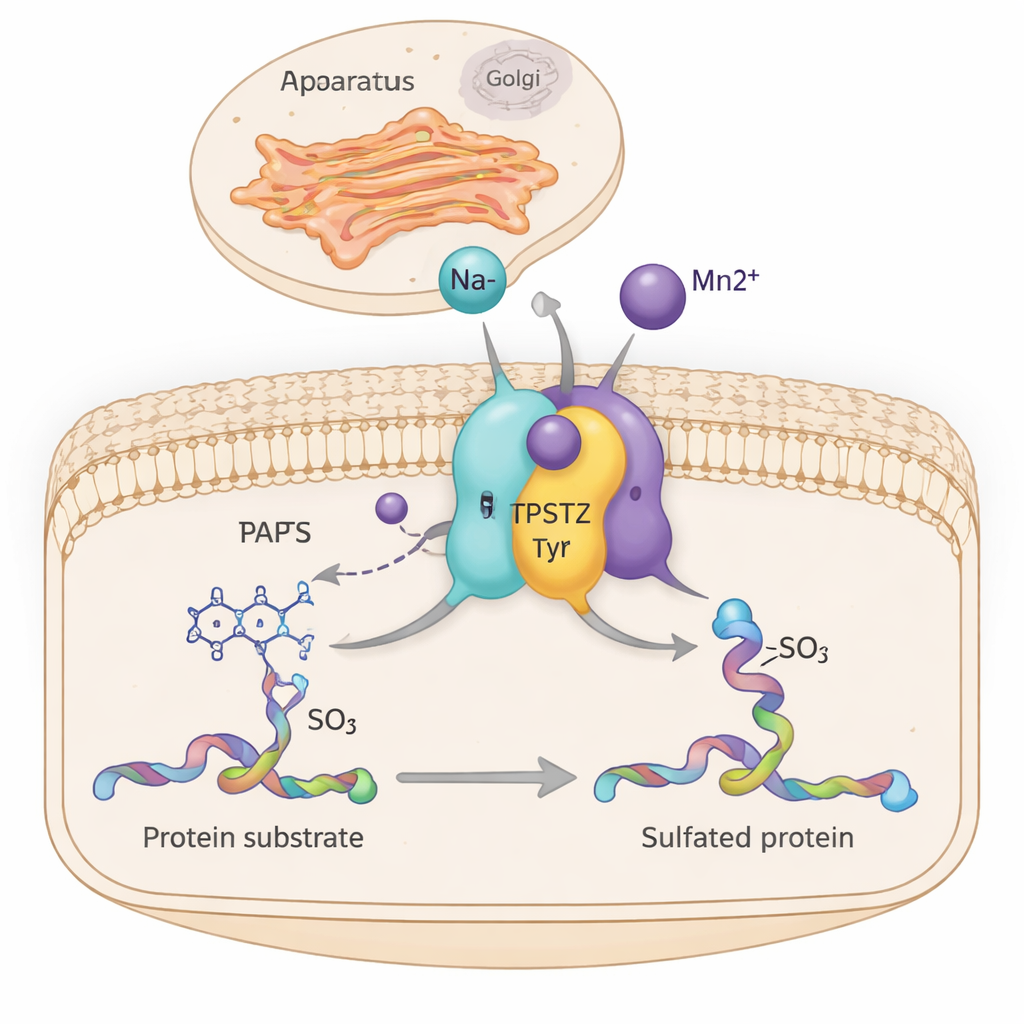
Uma proteína que “decora” outras proteínas
A TPST2 pertence a uma família de enzimas que realizam a “sulfatação de tirosina”, uma modificação química adicionada a resíduos específicos de tirosina em proteínas. Essas proteínas sulfadas desempenham papéis fundamentais fora das células, influenciando a coagulação sanguínea, o movimento de leucócitos, a ligação hormônio–receptor e até a entrada de vírus nas células. Em humanos, existem duas enzimas sulfotransferas principais, TPST1 e TPST2, que ficam na membrana do Golgi e modificam proteínas conforme elas são preparadas para exportação. Estudos em camundongos mostram que a perda de TPST2 atrapalha a produção de hormônio tireoidiano, retarda o crescimento e causa infertilidade masculina, destacando sua importância para a fisiologia normal.
Relações com câncer e evasão imune
Pesquisas recentes ligaram a TPST2 diretamente a doenças. No melanoma, a TPST2 modifica um componente do receptor de interferon de modo que enfraquece a sinalização imune, e bloquear a TPST2 aumenta o efeito de terapias de checkpoint imunológico que miram PD-1. No câncer de pâncreas, uma via dependente de TPST2 ajuda a estabilizar uma proteína (integrina β4) que promove o crescimento e a disseminação do tumor. Inibir a TPST2 nesses modelos desacelera a divisão celular e a invasão do câncer. Como a TPST2 atua sobre proteínas na superfície celular, ela reconfigura efetivamente como as células detectam e respondem ao ambiente, tornando-a um alvo atraente para novas terapias.
Encontrando os “botões de liga” metálicos
Bioquímicos há muito sabem que a TPST2 se torna muito mais ativa quando metais divalentes como o manganês (Mn²⁺) estão presentes, mas a razão estrutural faltava. Neste estudo, os autores produziram o núcleo catalítico da TPST2 humana e o cristalizaram juntamente com um subproduto da reação e com sódio (Na⁺) ou manganês. Usando cristalografia de raios X de alta resolução, descobriram dois pequenos bolsões de ligação a metais dentro da enzima, cada um com um arranjo nítido e de seis coordenadas (octaédrico) dos átomos circundantes. Ao ajustar o comprimento de onda dos raios X às assinaturas únicas de diferentes metais, confirmaram que o Mn²⁺ ocupa seletivamente esses sítios, enquanto metais como zinco e cobre se ligam fracamente em outros locais ou não se ligam.
Enrijecendo partes móveis-chave em vez de remodelar tudo
Surpreendentemente, a TPST2 com sódio e a TPST2 com manganês apresentaram aparência quase idêntica no conjunto; não houve uma abertura ou fechamento dramáticos da proteína. Em vez disso, os metais afetaram principalmente duas regiões flexíveis próximas à entrada do sítio ativo: uma hélice chamada α3 e uma alça próxima conhecida como alça α12–α13. Em estados sem metal ou com ligação frouxa, esses segmentos se movem e são parcialmente desordenados. Quando Na⁺ se liga, tornam-se mais ordenados; o Mn²⁺ os aperta ainda mais, como mostrado pela redução do movimento térmico nos dados de raios X e por análises computacionais de flexibilidade. Essa rigidez adicional eleva modestamente a temperatura de fusão da enzima e provavelmente reduz o custo “entrópico” de organizar o sítio ativo — facilitando e acelerando a orientação dos substratos pela TPST2 na posição correta para a sulfatação. 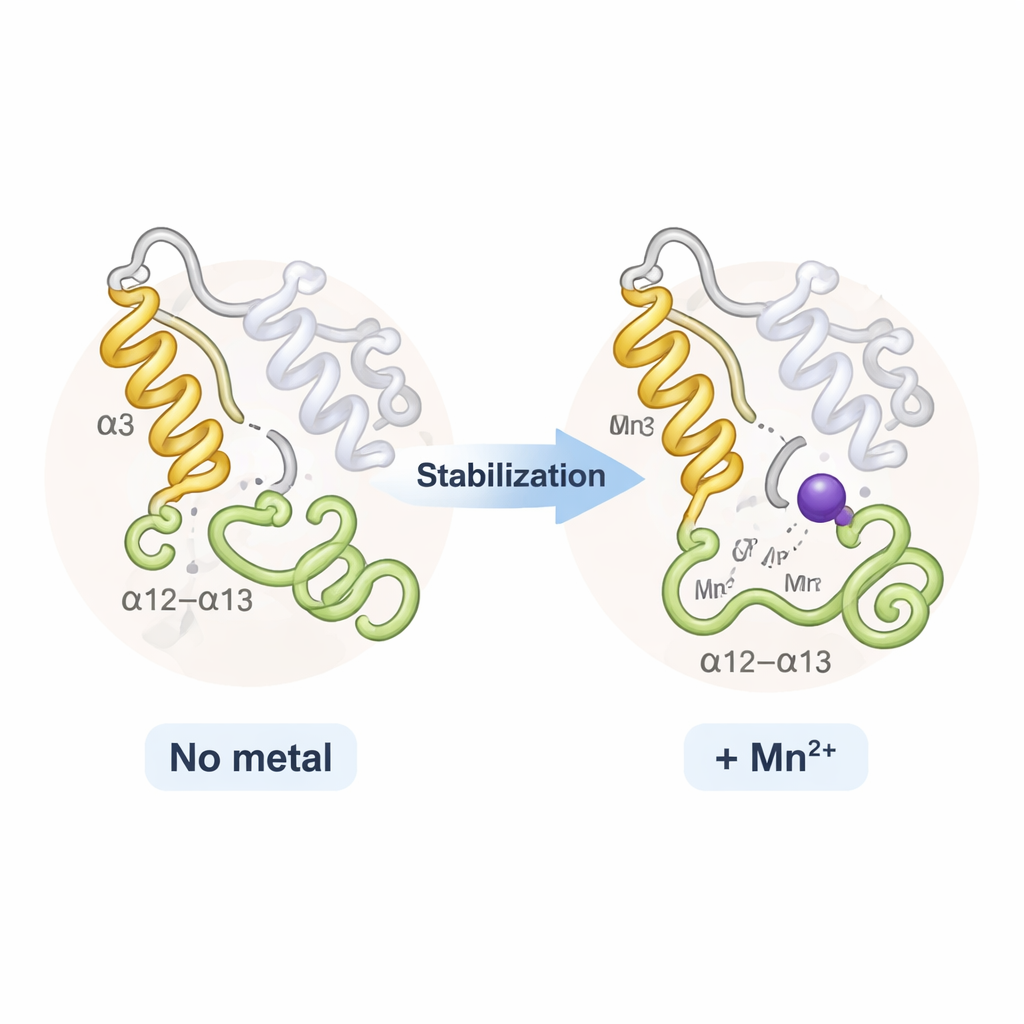
Dos minerais celulares ao controle da sinalização
Os autores propõem um modelo de “ativação por ordenação”. Na ausência de metal ligado, a TPST2 é flexível em torno da entrada do sítio ativo e funciona de forma ineficiente. O sódio, abundante nas células, pode se ligar aos mesmos sítios e criar um estado parcialmente ordenado e moderadamente ativo. O manganês, presente em quantidades micromolares cuidadosamente controladas no Golgi, liga-se com mais força e trava as regiões-chave em um arranjo ideal, maximizando a eficiência catalítica. Isso sugere que mudanças sutis nos níveis de manganês no Golgi poderiam ajustar quão fortemente a TPST2 modifica seus alvos. Como a TPST2 influencia a produção hormonal e a sinalização relacionada ao câncer, o trabalho destaca um possível elo entre o equilíbrio de íons metálicos, as “decorações” proteicas e a doença — além de fornecer uma base estrutural para projetar fármacos que modulam a atividade da TPST2 ao mimetizar ou interromper a ligação de metais.
Citação: Jin, M., Noh, C., Yang, J. et al. Structural characterization of metal binding in human tyrosylprotein sulfotransferase 2, TPST2. Sci Rep 16, 6066 (2026). https://doi.org/10.1038/s41598-026-37189-4
Palavras-chave: sulfatação de tirosina, TPST2, manganês, aparelho de Golgi, modificação de proteínas