Clear Sky Science · pt
Triagens em todo o genoma identificam reguladores centrais da expressão da proteína priônica na superfície celular
Por que isso importa para a saúde cerebral
As doenças priônicas, como a doença de Creutzfeldt–Jakob em humanos e a “doença da vaca louca” em bovinos, são raras, mas sempre fatais, e afetam o cérebro. Um agente central é uma proteína normal do cérebro, chamada proteína priônica, que pode se dobrar de forma errônea e espalhar o dano de célula a célula. Quanto mais dessa proteína estiver na superfície dos neurônios, mais fácil é a instalação da doença. Este estudo propôs mapear, em todo o genoma, quais genes controlam quanto da proteína priônica aparece na face externa de células do tipo neuronal. Esse mapa pode ajudar cientistas a projetar novas formas de reduzir essa proteína e, potencialmente, desacelerar várias doenças neurodegenerativas.
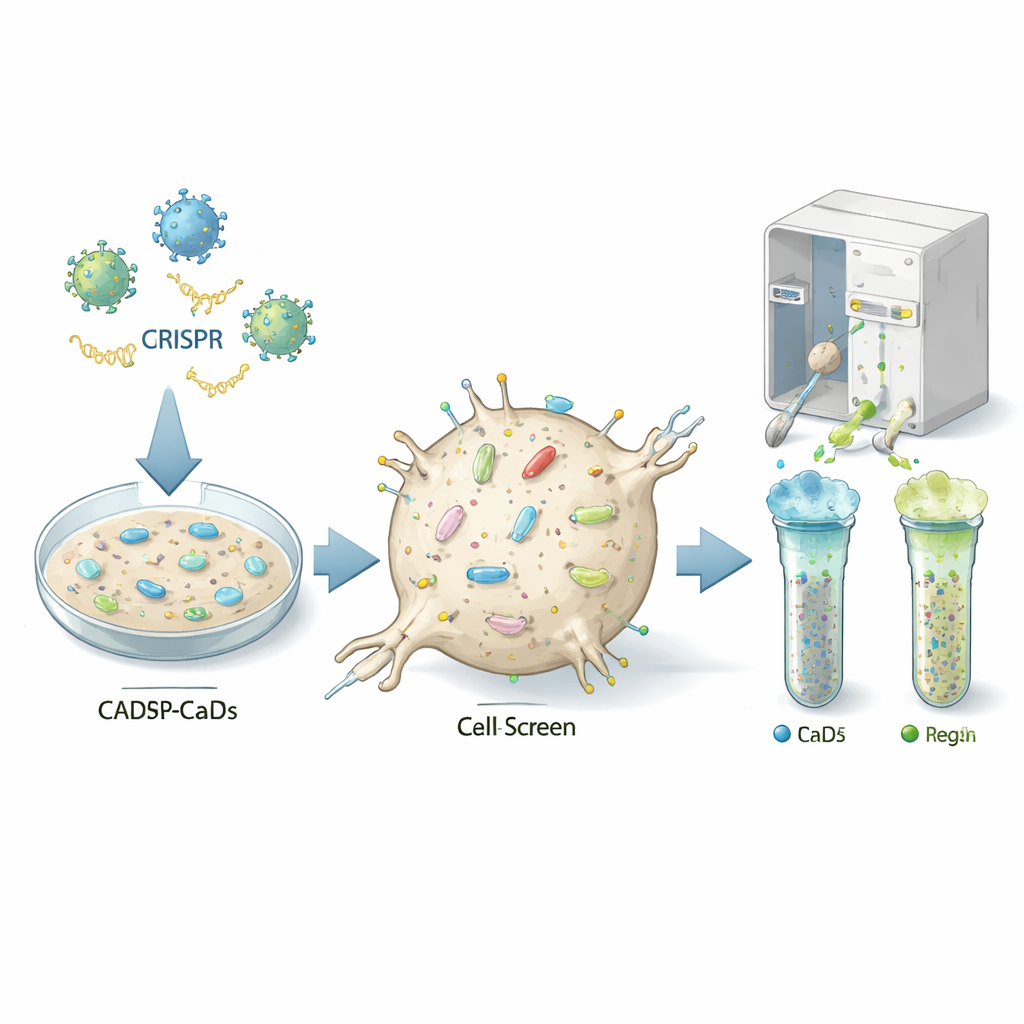
Encontrando os botões de controle da célula
Os autores usaram uma poderosa abordagem de edição genética chamada CRISPR para desligar quase todos os genes, um a um, em uma linhagem celular de camundongo com características neuronais suscetível à infecção por príons (chamada células CAD5). Cada célula recebeu uma “batida” genética diferente, de modo que a população resultante continha milhões de variantes, cada uma com um gene específico ausente. Em seguida, a equipe marcou as células com anticorpos fluorescentes que reconhecem a proteína priônica normal na superfície celular e usou um separador celular para isolar células com níveis incomumente baixos ou altos dessa proteína. Ao sequenciar quais RNAs-guia estavam enriquecidos nos grupos de baixa ou alta expressão, puderam inferir quais genes inativados normalmente atuam como interruptores de liga/desliga para a proteína priônica na superfície celular.
Dois estados celulares, respostas sobrepostas
Os neurônios não têm todos a mesma aparência ou comportamento ao longo de sua vida, então os pesquisadores investigaram se os mesmos genes controlam a proteína priônica em diferentes estados celulares. Células CAD5 podem ser mantidas em um estado de crescimento rápido, menos especializado, ou levadas — pela remoção de soro do meio de cultura — a um formato mais maduro e semelhante a neurônio. A equipe realizou a mesma triagem CRISPR em todo o genoma nas duas condições. Nas células indiferenciadas (menos maduras) validaram 46 genes que aumentam, e 21 que diminuem, a proteína priônica de superfície quando presentes. Nas células diferenciadas (mais neuronais) confirmaram 41 reguladores positivos e 13 reguladores negativos. Vinte e três genes — em sua maioria aqueles que ajudam a ligar uma “âncora” lipídica à proteína — foram compartilhados entre ambos os estados celulares, destacando uma maquinaria regulatória central que opera independentemente da maturidade.
Principais linhas de montagem que importam
Análises adicionais revelaram que muitos dos genes recém-identificados pertencem a conhecidas “linhas de montagem” celulares que modificam proteínas enquanto elas viajam até a superfície. Uma via principal constrói a âncora GPI, uma pequena estrutura rica em lipídios que prende a proteína priônica à face externa da membrana celular. Interromper quase qualquer etapa dessa via reduziu a quantidade de proteína priônica que alcançou a superfície, tanto em células imaturas quanto maduras. Uma segunda via envolve a glicosilação N-ligada, na qual cadeias complexas de açúcares são adicionadas às proteínas enquanto passam pelas membranas internas da célula. Genes dessa via de adição de açúcares surgiram principalmente como importantes nas células menos maduras. Quando os pesquisadores trataram as células com pequenas moléculas que bloqueiam etapas específicas da glicosilação, os níveis de proteína priônica de superfície caíram em cerca de um terço sem matar as células, confirmando os achados genéticos.
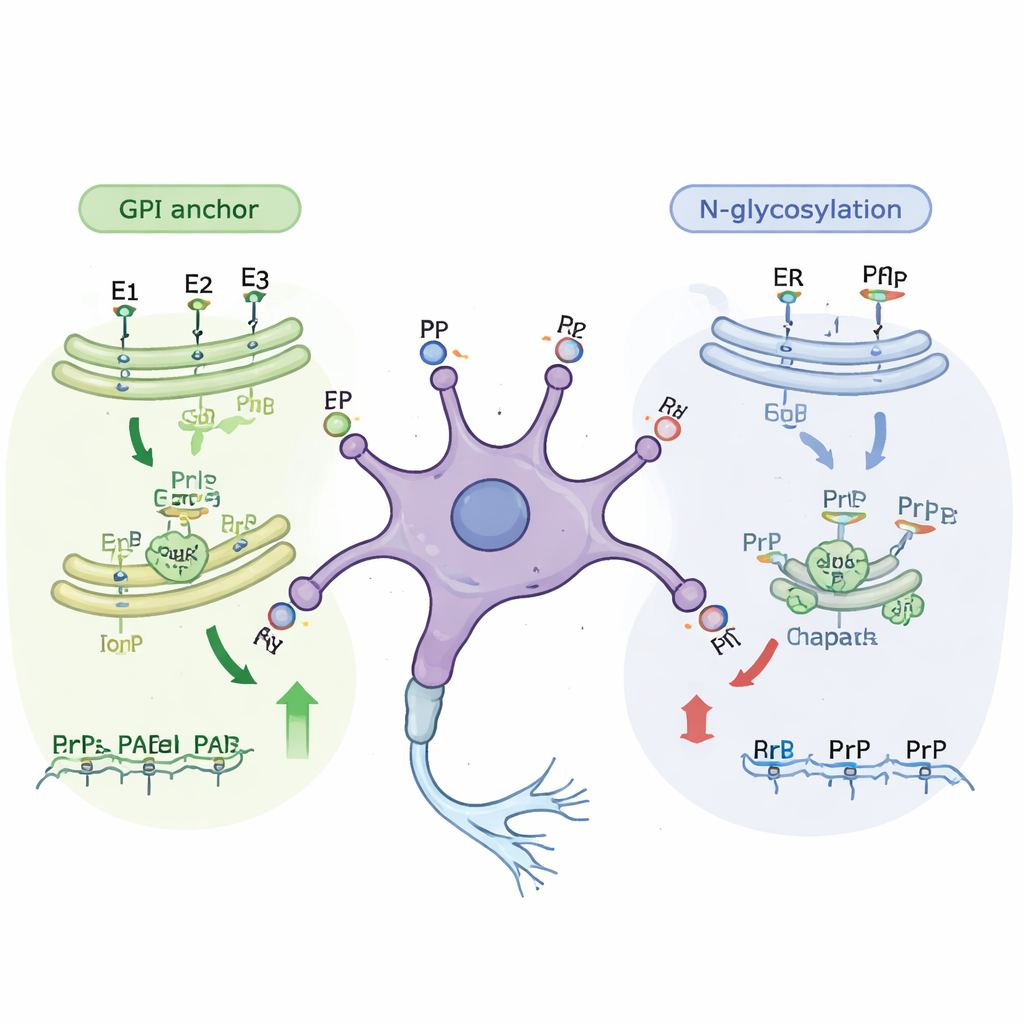
Proteínas auxiliares e respostas ao estresse
As triagens também destacaram chaperonas moleculares — proteínas que ajudam outras proteínas a se dobrarem corretamente — como reguladoras importantes da proteína priônica. Em particular, Hspa5 (também chamada BiP), uma chaperona central no compartimento de dobramento proteico da célula, emergiu como reguladora positiva nas células mais semelhantes a neurônios. Quando os pesquisadores usaram um fármaco para inibir Hspa5, os níveis de proteína priônica de superfície caíram em ambos os estados celulares, novamente sem dano óbvio às células. Outros alvos incluíam genes envolvidos no transporte de proteínas pela célula, no controle de ativação gênica e várias proteínas ligadas à função sináptica e a outras doenças cerebrais, como Alzheimer e ELA. Juntos, esses resultados mostram que os níveis de proteína priônica na superfície celular são moldados por uma rede de vias que abrangem produção, modificação, tráfego e controle de qualidade das proteínas.
O que isso significa para tratamentos futuros
Este trabalho fornece o primeiro catálogo abrangente de genes que controlam quanto da proteína priônica aparece na superfície de células com características neuronais suscetíveis à infecção por príons. Alguns desses genes, especialmente os das vias da âncora GPI e da N-glicosilação e o sistema de chaperonas Hspa5, surgem como pontos de partida promissores para descoberta de fármacos: reduzir sua atividade deve diminuir a quantidade de proteína priônica disponível para se dobrar mal, e estudos anteriores mostram que até reduções parciais podem atrasar significativamente a doença em animais. Ao mesmo tempo, as diferenças claras entre células imaturas e maduras ressaltam que o estado das células cerebrais importa na escolha de alvos. Embora mais trabalho seja necessário para testar como a manipulação desses genes afeta a infecção priônica real e outras condições neurodegenerativas em cérebros vivos, este estudo oferece um roteiro de alavancas celulares que os pesquisadores podem explorar para desacelerar ou prevenir essas doenças devastadoras.
Citação: Beauchemin, K.S., Supattapone, S. Genome-wide screens identify core regulators of cell surface prion protein expression. Sci Rep 16, 5895 (2026). https://doi.org/10.1038/s41598-026-37137-2
Palavras-chave: proteína priônica, triagem CRISPR, neurodegeneração, glicosilação de proteínas, âncora GPI