Clear Sky Science · pt
Resfriamento ultra-rápido em dupla superfície sólida com pressão aprimorada melhora a recuperação pós-descongelamento em hepatócitos e fatias hepáticas de corte preciso
Por que congelar tecido hepático importa
Manter células e tecidos vivos fora do corpo é um dos motores discretos da medicina moderna. Células hepáticas congeladas ajudam pesquisadores a testar novos medicamentos, modelar doenças e, um dia, podem reparar órgãos com falha. Mas congelar material vivo é complicado: se cristais de gelo crescem dentro ou entre as células, eles rompem estruturas delicadas. Este estudo explora uma nova maneira de congelar células hepáticas e fatias finas de fígado tão rapidamente, e em condições tão controladas, que cristais de gelo danosos praticamente não têm tempo para se formar.
O problema do gelo e dos protetores químicos
A criopreservação convencional depende de duas ferramentas imperfeitas: frio e químicos. À medida que as amostras são resfriadas, a água tende a formar gelo, que pode perfurar membranas e desestruturar tecidos. Para combater isso, os cientistas adicionam agentes crioprotetores, como o dimetilsulfóxido (DMSO), que ajudam a água a solidificar em um estado vítreo em vez de gelo cristalino. Contudo, nas concentrações elevadas tipicamente usadas, esses agentes podem por si só envenenar as células ou causar inchaço e encolhimento danosos à medida que se movem para dentro e fora do tecido. O objetivo dos autores foi reduzir a quantidade de DMSO necessária ao mesmo tempo em que evitam gelo prejudicial, tornando o armazenamento de células e tecidos hepáticos mais seguro e prático.
Uma nova forma de pressionar e resfriar ao mesmo tempo
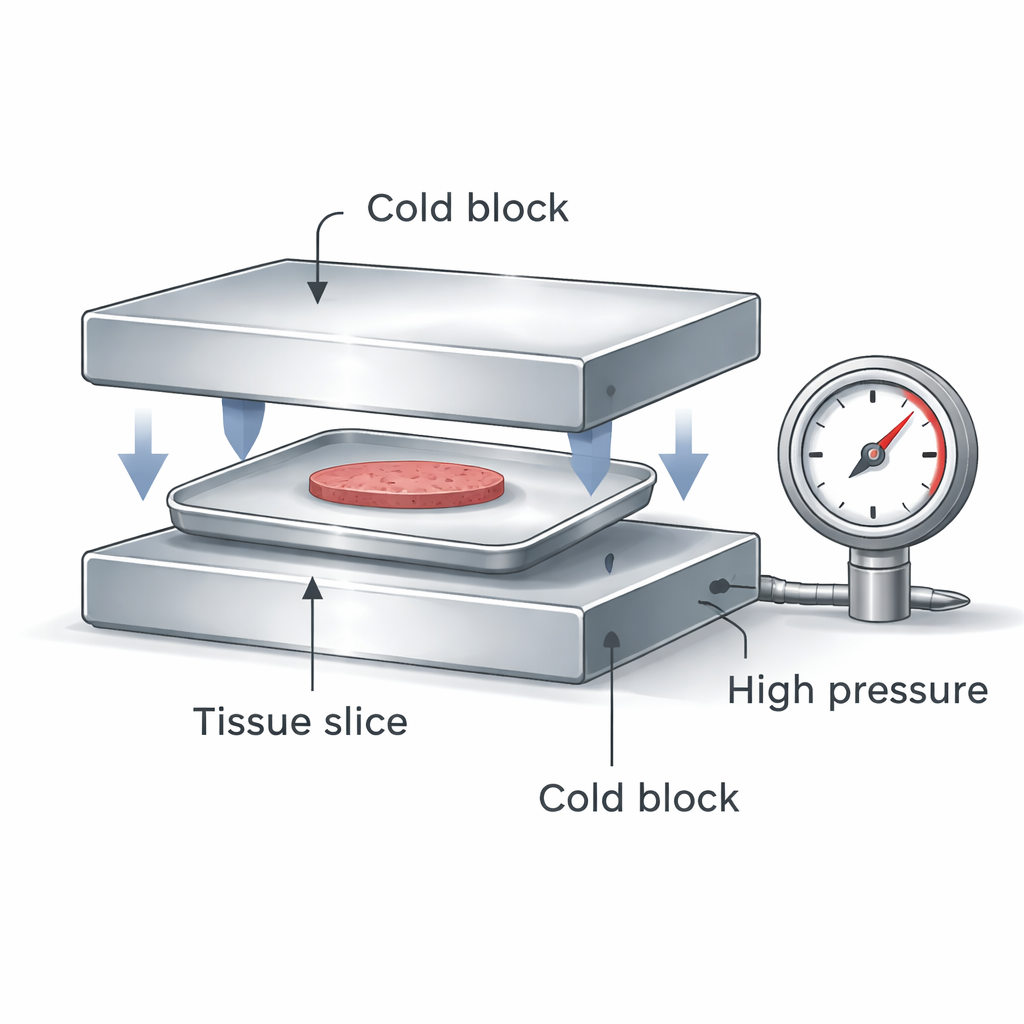
A equipe projetou um dispositivo compacto que sanduícha um recipiente selado e plano de alumínio contendo células hepáticas ou fatias hepáticas de corte preciso entre dois blocos metálicos extremamente frios. Quando os blocos se pressionam, fazem duas coisas importantes simultaneamente: criam alta pressão dentro do recipiente selado e extraem calor da amostra tanto pelo topo quanto pela base. A alta pressão altera o comportamento da água, de modo que o gelo se forma a temperaturas mais baixas e a solução vitrifica com mais facilidade. O contato em dupla face proporciona uma taxa de resfriamento muito mais rápida e uniforme do que simplesmente mergulhar um frasco plástico em nitrogênio líquido, e o recipiente selado mantém a amostra isolada de contaminação.
Encontrando o ponto ideal entre segurança e sobrevivência
Para verificar se essa abordagem era suave o bastante para material vivo, os pesquisadores primeiro checaram se o próprio recipiente de alumínio não prejudicava células HepG2 de origem hepática durante os curtos tempos de manuseio usados. A sobrevivência celular manteve-se essencialmente inalterada. Em seguida, expuseram essas células a diferentes níveis de DMSO antes do congelamento e confirmaram uma troca conhecida: mais DMSO suprime melhor o gelo, mas torna-se claramente tóxico em 30%, enquanto 20% permanece em grande parte tolerável. Para fatias de fígado de camundongo, testaram quanta pressão o tecido podia suportar na ausência de congelamento. Rajadas breves de até 150 megapascais tiveram pouco efeito na viabilidade, mas 200 megapascais causaram cerca de 30% de queda, marcando um limite superior para operação segura.
Fatias hepáticas melhor preservadas após o descongelamento
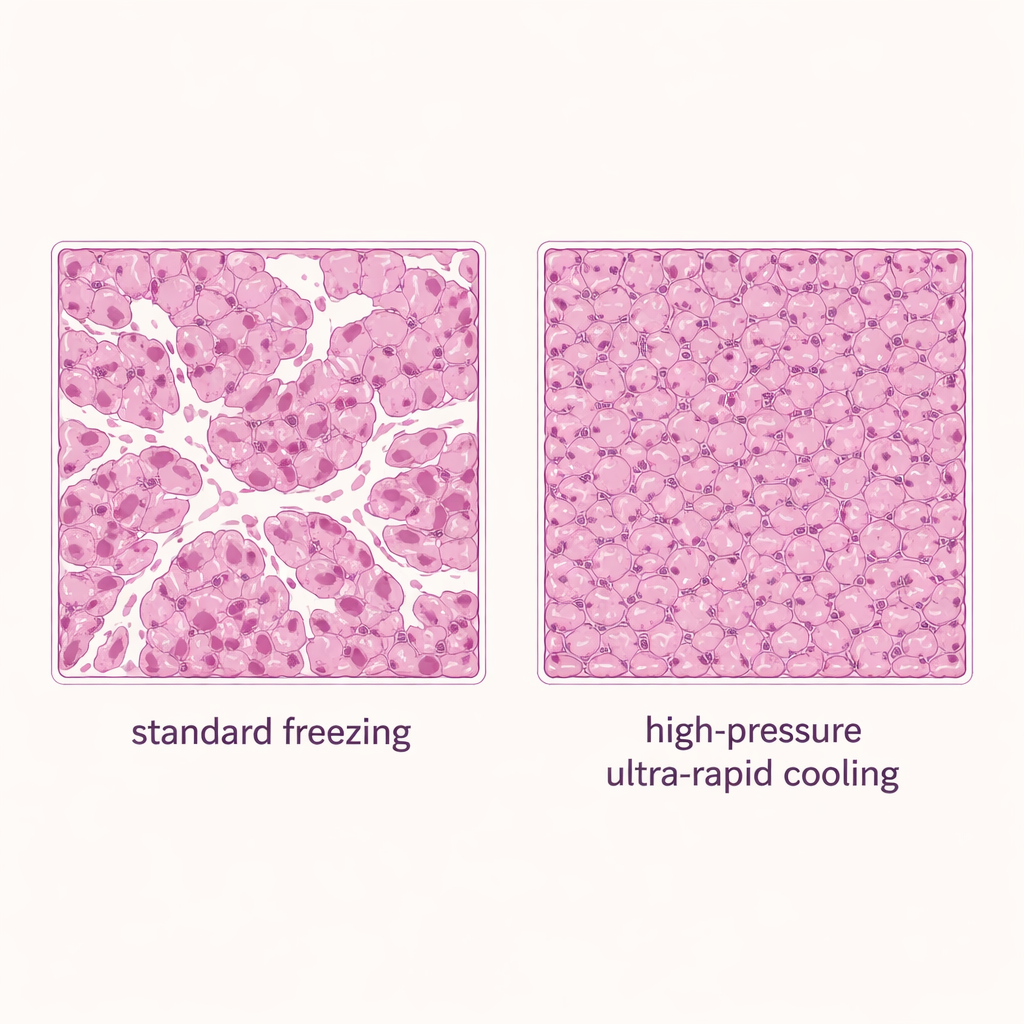
Com faixas seguras estabelecidas, os autores compararam três métodos de congelamento para fatias hepáticas: imersão padrão do recipiente selado em nitrogênio líquido (uma abordagem por convecção, baseada em fluido), resfriamento por superfície sólida sem pressão adicional e resfriamento por superfície sólida com alta pressão de 150 megapascais. Todos os grupos usaram 20% de DMSO. O método assistido por pressão apresentou os melhores resultados: cerca de 80% da viabilidade original do tecido foi mantida, superando tanto o congelamento convencional quanto o resfriamento por superfície sólida isoladamente. A microscopia de fatias de tecido coradas corroborou esses achados. Amostras congeladas por imersão convencional exibiram muitos espaços brancos abertos — assinaturas de dano por gelo — enquanto o resfriamento por superfície sólida com pressão produzidas tecido mais denso, mais intacto e com muito menos lacunas.
O que isso significa para o futuro do armazenamento de tecido
No geral, o estudo mostra que comprimir uma fatia de fígado selada em alumínio entre dois blocos ultrafrios sob pressão controlada pode melhorar muito a capacidade do tecido de sobreviver ao descongelamento. Ao combinar resfriamento mais rápido e uniforme com o comportamento da água alterado pela pressão, o método limita o crescimento de gelo danoso ao mesmo tempo em que usa uma concentração moderada e clinicamente familiar de DMSO. Para um leitor leigo, a conclusão é que engenharia mais inteligente — como embalamos e resfriamos o tecido — pode ser tão importante quanto os químicos que adicionamos. Essa abordagem de dupla face sob alta pressão pode se tornar um passo em direção a um armazenamento de tecido hepático mais seguro e confiável e, eventualmente, de outros órgãos para pesquisa e terapia.
Citação: Amini, M., Benson, J.D. Pressure enhanced dual-solid-surface ultra-rapid cooling improves post-thaw recovery in hepatocytes and precision cut liver slices. Sci Rep 16, 5994 (2026). https://doi.org/10.1038/s41598-026-37136-3
Palavras-chave: criopreservação, tecido hepático, vitrificação, resfriamento em alta pressão, congelamento sem gelo