Clear Sky Science · pt
LncRNAs associadas à senescência TRMP e TRMP-S promovem o câncer gástrico ativando IGFL4
Por que esta pesquisa importa
O câncer de estômago (gástrico) continua sendo um dos mais letais do mundo, em grande parte porque frequentemente é detectado tardiamente e pode ser difícil de tratar. Este estudo revela como duas moléculas genéticas pouco conhecidas, chamadas TRMP e TRMP-S, ajudam tumores gástricos a crescer e a se disseminar. Ao expor a sequência de eventos que elas desencadeiam dentro das células cancerosas e no ambiente imune do tumor, o trabalho aponta novas maneiras pelas quais médicos poderão, no futuro, diagnosticar pacientes mais cedo e desenvolver tratamentos direcionados mais eficazes.
Mensagens ocultas em nosso DNA
A maioria das pessoas pensa em genes como plantas de instruções para proteínas, mas nosso DNA também produz RNAs longos não codificantes (lncRNAs) que não geram proteínas e, ainda assim, influenciam fortemente o comportamento celular. TRMP e sua variante de splicing mais curta TRMP-S são dois desses lncRNAs. Eles já haviam sido associados ao envelhecimento e ao controle do ciclo celular em células de pulmão e cólon, mas seu papel no câncer gástrico era desconhecido. Como lncRNAs podem servir como marcadores para diagnóstico e alvos terapêuticos, os autores buscaram descobrir se TRMP e TRMP-S promovem a transformação de células gástricas em cancerosas e como podem interagir com outras moléculas para fazê-lo.
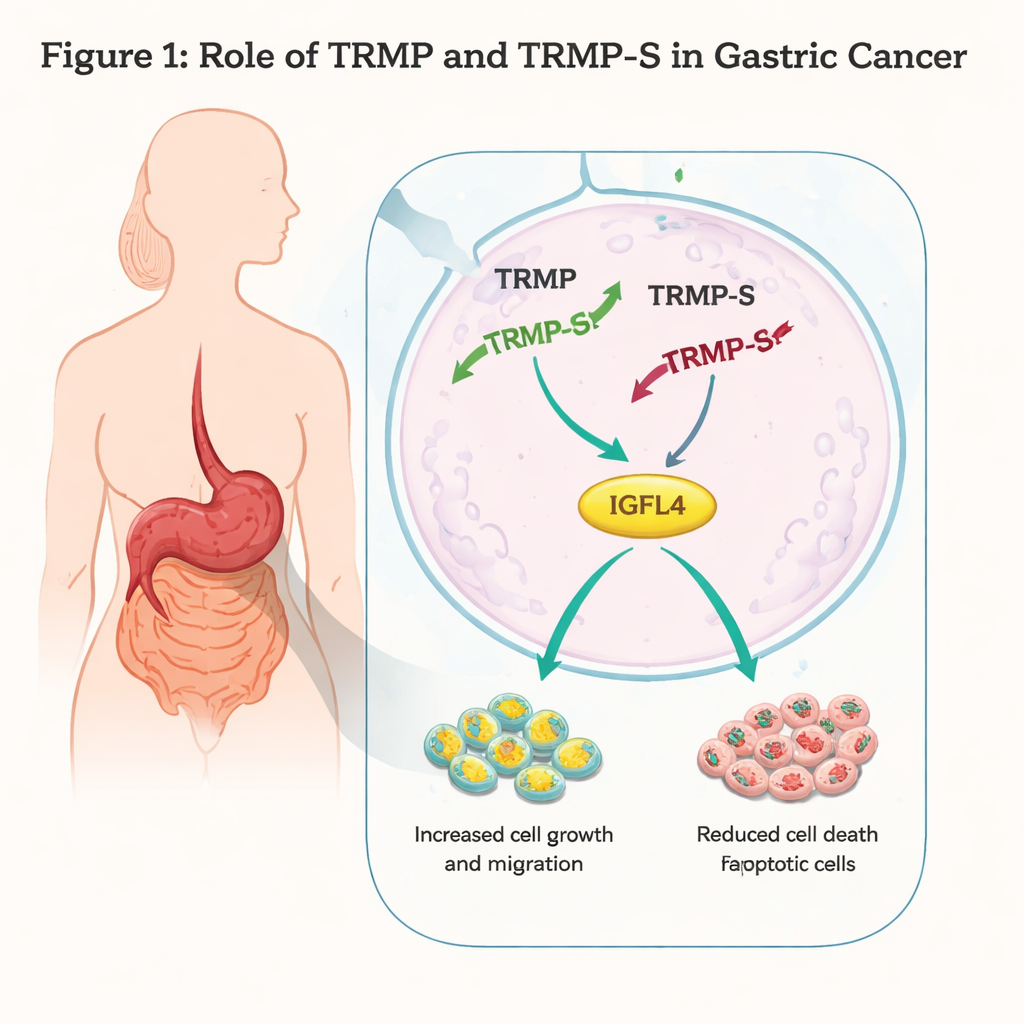
Desligando um acelerador do câncer
Os pesquisadores trabalharam com duas linhagens humanas de câncer gástrico, AGS e MKN45, e usaram ferramentas genéticas para reduzir os níveis de TRMP-S e TRMP. Quando silenciaram TRMP-S, as células cancerosas cresceram mais lentamente, formaram menos colônias e mostraram menor capacidade de migrar através de barreiras artificiais ou fechar feridas em cultura. Citometria de fluxo e análises de proteínas mostraram que mais células estavam passando por morte celular programada (apoptose) e que o ciclo celular era interrompido na fase G1, um “ponto de verificação” chave antes da cópia do DNA. Os níveis de p73, membro da família supressora tumoral p53, aumentaram quando TRMP-S foi perdido, coerente com um controle do ciclo celular mais forte e maior mortalidade celular. Esses resultados indicam que, normalmente, TRMP-S atua como um pedal do acelerador para células do câncer gástrico.
Um parceiro-chave: o sinal IGFL4
Para entender como TRMP e TRMP-S exercem seus efeitos, a equipe explorou grandes conjuntos de dados de pacientes do The Cancer Genome Atlas e de uma coorte coreana de câncer gástrico. Procuraram genes que estivessem anormalmente elevados em tumores e positivamente correlacionados com os níveis de TRMP, e então construíram um “modelo de risco” de seis genes que previu sobrevida dos pacientes — pontuações mais altas associaram-se a piores desfechos. Entre esses genes, um se destacou: IGFL4, membro de uma família relacionada aos fatores de crescimento semelhantes à insulina, conhecidos por favorecer crescimento e sobrevivência em muitos cânceres. Em células de câncer gástrico, reduzir TRMP-S diminuiu fortemente os níveis de RNA e proteína de IGFL4, enquanto um ensaio de imunoprecipitação de RNA mostrou que tanto TRMP quanto TRMP-S se ligam fisicamente à proteína IGFL4. A redução direta de TRMP teve o mesmo efeito atenuante sobre IGFL4, sugerindo que esses lncRNAs ajudam a estabilizar ou favorecer a produção desse sinal promotor de crescimento.
Retardando a disseminação e remodelando o cenário imune
Quando os pesquisadores usaram pequenos RNAs interferentes para silenciar o próprio IGFL4, as células de câncer gástrico desaceleraram o crescimento, migraram menos e mostraram menor capacidade de invadir através de membranas e fechar feridas. A análise de dados de tumores de pacientes revelou que os níveis de IGFL4 eram significativamente maiores em tumores gástricos do que em tecido gástrico normal, e elevados em muitos outros tipos de câncer também. Importante, tumores com expressão alta de IGFL4 exibiram padrões distintos de infiltração de células imunes: mais macrófagos indiferenciados (M0) e menos plasmócitos, monócitos, eosinófilos e neutrófilos. Pontuações imunes computacionais sugeriram que tumores com IGFL4 alto podem responder melhor a imunoterapias modernas que bloqueiam pontos de verificação imunes, indicando que IGFL4 pode ajudar a identificar pacientes com maior chance de se beneficiar desses tratamentos.
Um pequeno RNA que freia
O estudo também revelou um contrapeso a essa via promotora do câncer. Ao correlacionar microRNAs e expressão gênica em dados de pacientes, os autores identificaram miR-129-5p como um pequeno RNA negativamente associado tanto a TRMP quanto a IGFL4. Em células de câncer gástrico, adicionar miR-129-5p reduziu os níveis de IGFL4 e desacelerou o crescimento, enquanto bloquear miR-129-5p aumentou IGFL4 e acelerou a proliferação. Outro microRNA candidato, miR-4739, não afetou mensuravelmente IGFL4 e foi descartado. Esses resultados suportam uma cadeia regulatória na qual TRMP, TRMP-S, miR-129-5p e IGFL4 formam uma rede que ajusta o quão agressivamente as células do câncer gástrico crescem e como interagem com seu entorno.
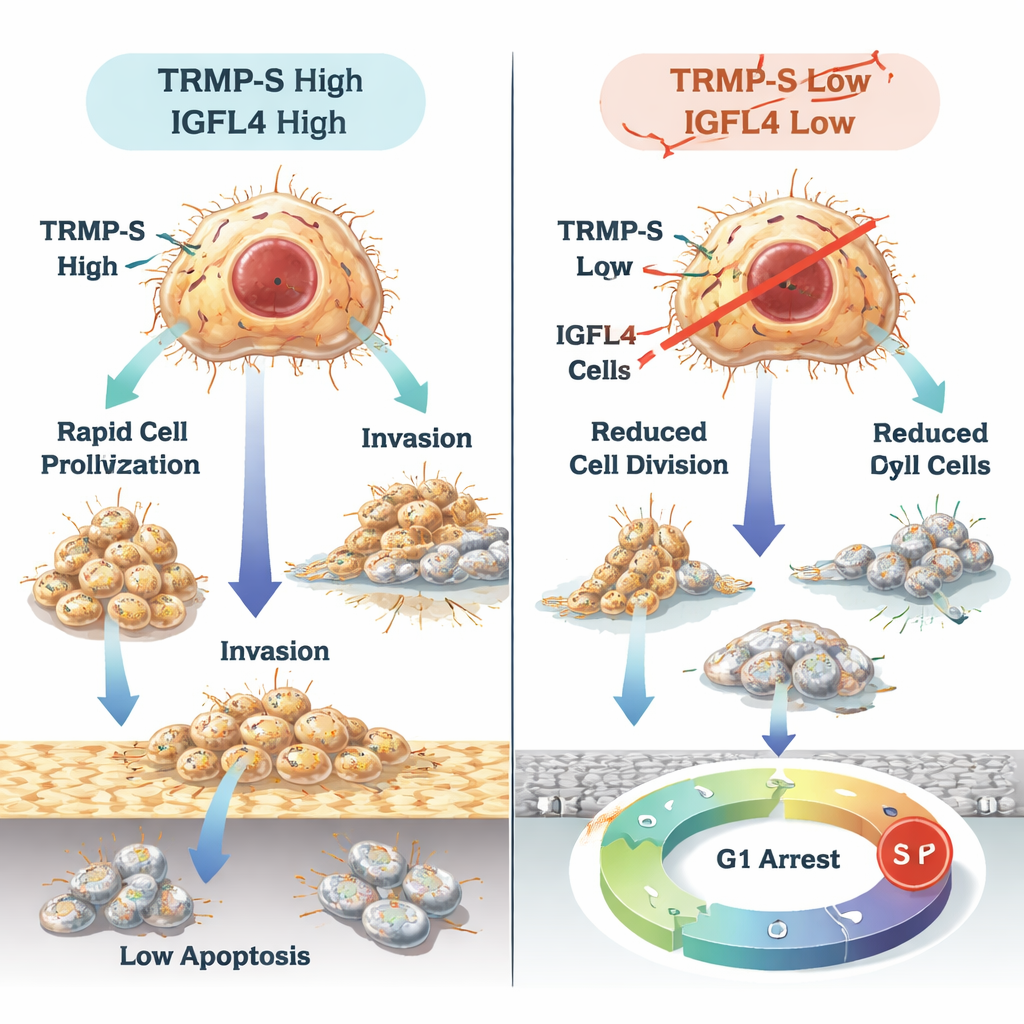
O que isso pode significar para pacientes
Em termos diretos, este trabalho mostra que TRMP e TRMP-S atuam como diretores nos bastidores que ativam IGFL4 e ajudam as células do câncer gástrico a crescer, espalhar-se e escapar de mecanismos naturais de freio. Ao mesmo tempo, o pequeno RNA miR-129-5p funciona como um freio sobre IGFL4, e o próprio IGFL4 ajuda a moldar como as células imunes se reúnem ao redor dos tumores e o quão bem terapias que despertam o sistema imune podem funcionar. Embora sejam necessárias mais pesquisas e testes clínicos, TRMP, TRMP-S, IGFL4 e miR-129-5p representam, em conjunto, um conjunto promissor de marcadores para prever prognóstico e potenciais novos alvos para drogas destinadas a frear ou interromper o câncer gástrico.
Citação: Zhang, M., Mi, Y., Li, F. et al. Senescence-associated LncRNAs TRMP and TRMP-S promote gastric cancer by activating IGFL4. Sci Rep 16, 6740 (2026). https://doi.org/10.1038/s41598-026-37106-9
Palavras-chave: câncer gástrico, RNA longo não codificante, TRMP, IGFL4, microambiente tumoral