Clear Sky Science · pt
Identificação de RBX1 como regulador da transcrição de LIPT1 e seu papel na morte celular induzida por cobre em células de GBM
Por que o cobre e os tumores cerebrais importam
O glioblastoma multiforme é uma das formas mais letais de câncer cerebral, com a maioria dos pacientes sobrevivendo apenas por um curto período após o diagnóstico, apesar de cirurgias agressivas, radioterapia e quimioterapia. Este estudo explora um aliado inesperado contra esses tumores: o metal cobre. Os pesquisadores analisam uma forma recentemente reconhecida de morte celular desencadeada pelo cobre e identificam uma via molecular que pode ajudar médicos a aproveitar esse processo para enfraquecer tumores e, potencialmente, reforçar o ataque do sistema imunológico às células cancerosas.
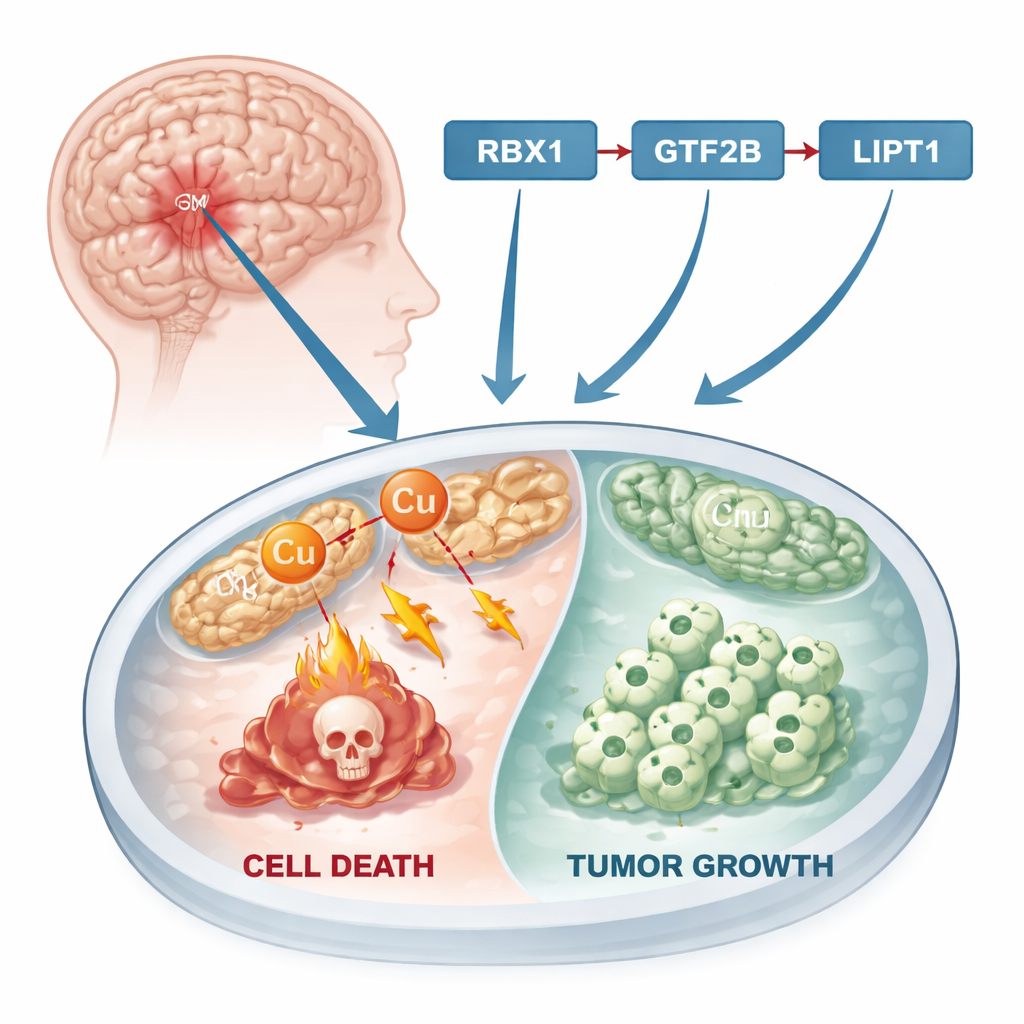
Uma nova forma de as células morrerem
Durante décadas, a pesquisa sobre câncer se concentrou em formas conhecidas de morte celular, como a apoptose, em que células danificadas se desligam silenciosamente. Recentemente, cientistas descobriram uma rota diferente chamada morte celular induzida por cobre, ou “cuprotose”. Nesse processo, o excesso de cobre se acumula nas usinas de energia da célula, as mitocôndrias. Lá, ele perturba proteínas-chave, fazendo com que agregados tóxicos se formem e, em última instância, matem a célula. Como muitos tumores apresentam metabolismo de metais alterado e níveis de cobre mais altos do que tecidos normais, a cuprotose oferece um ponto de pressão potencial: se os pesquisadores conseguirem empurrar as células tumorais para essa morte dirigida pelo cobre, talvez consigam frear ou interromper o crescimento do câncer.
Destacando um gene-chave no glioblastoma
Os autores começaram investigando um conjunto de genes já conhecidos por participar da cuprotose e perguntaram como eles se comportam em amostras de glioblastoma versus tecido cerebral normal. Um gene em particular, chamado LIPT1, se destacou. Ele estava mais ativo no tecido de glioblastoma e em várias linhas celulares de glioblastoma do que em células cerebrais normais. Importante, pacientes cujos tumores apresentavam maior atividade de LIPT1 tendiam a ficar mais tempo sem recidiva após o tratamento. Níveis altos de LIPT1 também se associaram a maior presença de células T CD8, os principais assassinos do câncer pelo sistema imune, sugerindo que esse gene pode ajudar a tornar o microambiente tumoral mais vulnerável ao ataque imunológico.
O que acontece quando o interruptor de morte por cobre é reduzido
Para testar se LIPT1 realmente afeta a morte induzida por cobre, a equipe expôs células de glioblastoma a uma combinação medicamentosa portadora de cobre que desencadeia a cuprotose de forma confiável. Em seguida, usaram ferramentas genéticas para reduzir os níveis de LIPT1. Quando LIPT1 foi suprimido, as células tumorais ficaram mais resistentes à morte induzida por cobre, sobreviveram melhor e exibiram maior capacidade de migração e invasão — comportamentos associados a um câncer mais agressivo. Em culturas mistas de células tumorais e células T CD8 humanas, a diminuição de LIPT1 também reduziu a liberação de moléculas sinalizadoras imunes e tornou as células cancerosas mais difíceis de serem destruídas pelas T cells. Em conjunto, esses experimentos indicam que LIPT1 aumenta a sensibilidade à morte induzida por cobre e favorece a atividade imune antitumoral.
Seguindo a cadeia de comando até RBX1
O próximo desafio foi entender por que LIPT1 está aumentado no glioblastoma. Ao combinar vários grandes bancos de dados de genes e proteínas, os pesquisadores identificaram um fator de transcrição — uma espécie de chave mestra da atividade gênica — chamado GTF2B, que se liga próximo ao gene LIPT1 e provavelmente aumenta sua expressão. Eles então investigaram o que controla o próprio GTF2B. Uma segunda proteína, RBX1, emergiu como forte candidata. RBX1 faz parte do sistema celular de marcação e descarte que sinaliza outras proteínas para degradação. Em células de glioblastoma, os níveis de RBX1 eram mais baixos do que no tecido cerebral normal, enquanto GTF2B e LIPT1 estavam aumentados. Ensaios laboratoriais mostraram que RBX1 pode anexar pequenas “marcas me destrua” ao GTF2B, levando à sua degradação; quando RBX1 foi aumentado, os níveis de GTF2B e a atividade de LIPT1 caíram, e bloquear a maquinaria de degradação celular reverteu esse efeito.
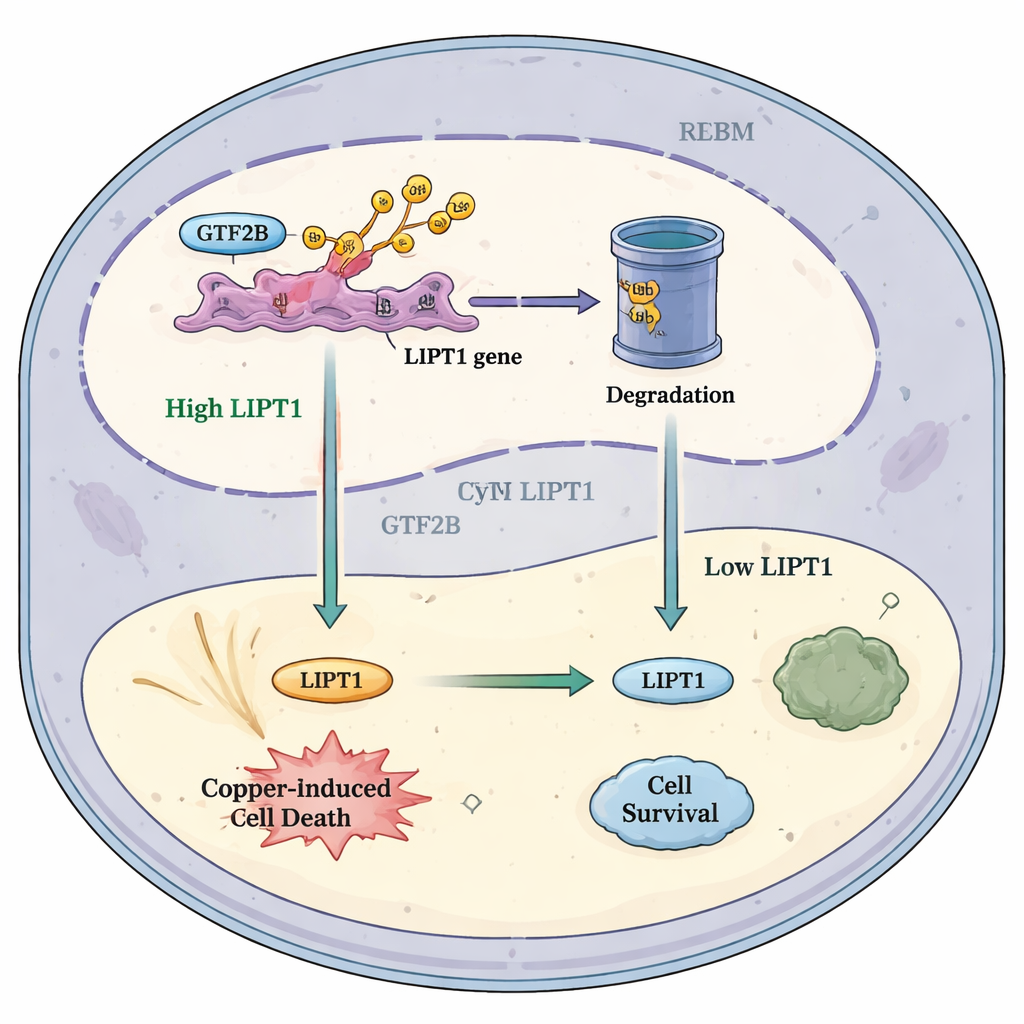
Como essa via poderia ajudar tratamentos futuros
Reunindo essas descobertas, os autores propõem um modelo simples: em condições saudáveis, RBX1 mantém GTF2B sob controle, limitando o quanto este ativa o gene LIPT1. No glioblastoma, a redução de RBX1 significa que menos GTF2B é degradado. O excesso de GTF2B então aumenta LIPT1, elevando a sensibilidade das células tumorais à morte induzida por cobre e atraindo mais células imunes que combatem o câncer. Esse modelo sugere que afinar cuidadosamente a via RBX1–GTF2B–LIPT1, possivelmente em conjunto com drogas que visam o cobre e imunoterapias, pode inclinar a balança dentro dos tumores cerebrais em direção à autodestruição. Embora muitas etapas sejam necessárias antes que essa ideia chegue aos pacientes, o estudo destaca uma interseção promissora entre biologia de metais, regulação gênica e imunologia do câncer que pode abrir novas vias terapêuticas para um dos cânceres mais persistentes.
Citação: Zeng, J., Liu, J., Hua, S. et al. Identification of RBX1 as a regulator of LIPT1 transcription and its role in copper-induced cell death in GBM cells. Sci Rep 16, 6837 (2026). https://doi.org/10.1038/s41598-026-37105-w
Palavras-chave: glioblastoma, morte celular induzida por cobre, LIPT1, imunologia tumoral, via RBX1