Clear Sky Science · pt
Predição, por aprendizado de máquina, de transformação hemorrágica pós-trombectomia usando DSA quantitativo
Por que isso importa para pacientes com AVC
Quando alguém sofre um AVC grave, os médicos às vezes conseguem remover o coágulo da artéria principal do cérebro usando um dispositivo minúsculo em um procedimento chamado trombectomia mecânica. Isso transformou o atendimento ao AVC, mas muitos pacientes ainda evoluem mal porque alguns desenvolvem novo sangramento no cérebro. O estudo por trás deste artigo faz uma pergunta simples, porém crucial: podemos usar informações que já são coletadas em sala de cirurgia, juntamente com aprendizado de máquina moderno, para prever quais pacientes têm maior probabilidade de sangrar e precisam de proteção adicional?
Indo além de “artéria aberta ou fechada”
Hoje, o sucesso após a trombectomia costuma ser avaliado pela aparência da artéria bloqueada na angiografia, uma espécie de filme de raio-X em tempo real dos vasos sanguíneos. Mas essa classificação grosseira não revela o que ocorre nos pequenos vasos a jusante do cérebro, onde o dano e o sangramento realmente acontecem. Alguns pacientes com reabertura das grandes artérias aparentemente perfeita ainda desenvolvem hemorragia cerebral grave, uma complicação chamada transformação hemorrágica. Os autores suspeitaram que medições mais detalhadas do fluxo sanguíneo nesses pequenos vasos, extraídas da mesma angiografia, poderiam conter pistas ocultas sobre quem está em risco.
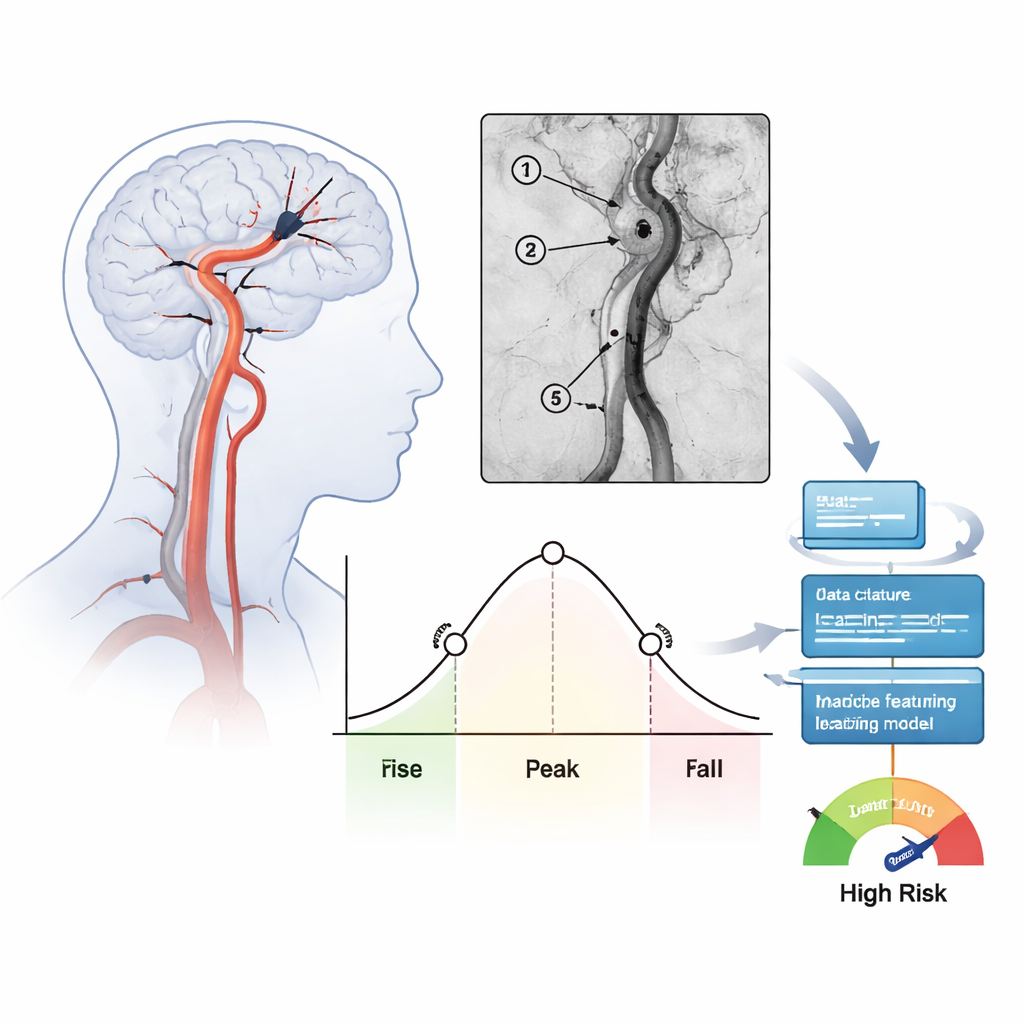
Transformando filmes angiográficos em números
A equipe estudou 171 pessoas tratadas por AVCs severos na parte anterior do cérebro ao longo de um ano em um único hospital. Depois que os médicos removeram o coágulo e restauraram o fluxo, registraram as vistas angiográficas padrão e então analisaram como o contraste injetado se lavava em e fora de vários pontos-chave ao longo da artéria tratada. Para cada região, calcularam medidas de tempo, como quanto tempo o sangue precisava para passar (tempo médio de trânsito) e quão larga era a principal onda de contraste (full width at half maximum). Esses números resumem se o sangue se move lentamente e de forma constante ou passa rapidamente em um pulso estreito. No total, 39 dessas características de fluxo foram extraídas para cada paciente e verificadas quanto à consistência entre avaliadores independentes.
Ensinando o computador a reconhecer padrões de risco
Os pesquisadores então usaram um conjunto de métodos comuns de aprendizado de máquina para verificar se essas características de fluxo, isoladas ou combinadas com dados clínicos básicos como idade e gravidade do AVC, poderiam distinguir pacientes que depois desenvolveram sangramento cerebral daqueles que não desenvolveram. Para evitar overfitting, eles primeiro usaram cinco técnicas diferentes de seleção de características para escolher as medidas mais informativas e dividiram repetidamente os dados em grupos de treino e teste com validação cruzada. Entre muitas combinações testadas, um modelo relativamente simples — regressão logística, ajustada com um filtro de características “Elastic Net” — teve o melhor desempenho. Quando se baseou apenas em medidas de fluxo derivadas da angiografia, separou corretamente, em média, pacientes com e sem hemorragia com uma área sob a curva ROC de cerca de 0,81. Quando fatores clínicos foram adicionados, o desempenho subiu para aproximadamente 0,86, sugerindo que o modelo poderia ser uma forte ferramenta de apoio à decisão.
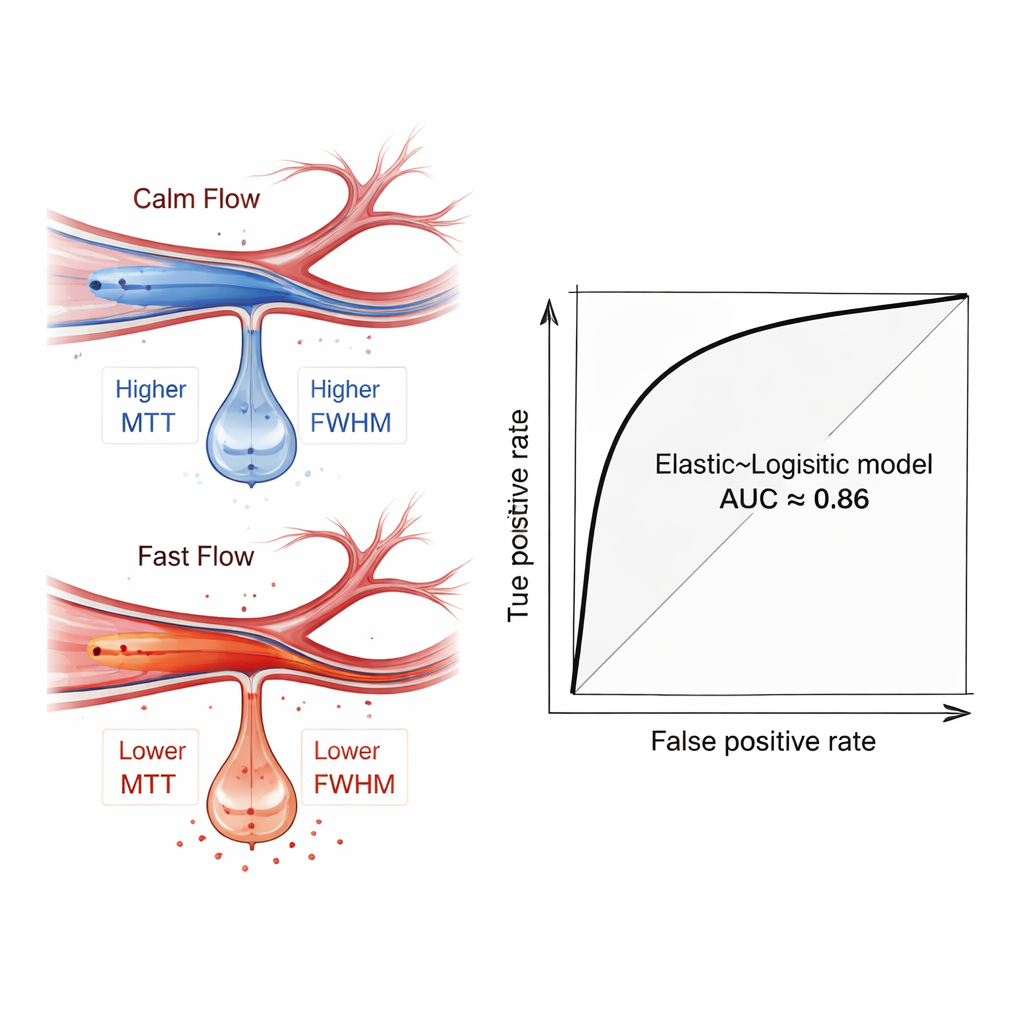
O que os sinais de fluxo sanguíneo revelaram
Aprofundando-se nos modelos treinados, os autores usaram uma técnica de interpretabilidade chamada SHAP para ver quais características mais importavam. Medidas que capturam quanto tempo e quão espalhado era o pulso de fluxo — especialmente em um ramo mais distal da artéria cerebral média — destacaram-se como preditores chave. Pacientes que depois sangraram tendiam a mostrar fluxo mais rápido e mais focalizado nesses vasos distais, refletido por tempos de trânsito menores e picos mais estreitos. Esse padrão é uma impressão hemodinâmica de “hiperperfusão”, um estado no qual tecido cerebral frágil, subitamente inundado por sangue em alta velocidade após um período de isquemia, tem maior probabilidade de vazar e sangrar. Importante, esse sinal emergiu mesmo quando comparações simples de grupo não mostraram diferenças estatísticas dramáticas, sublinhando o valor de uma análise multicaracterística baseada em máquina.
Como isso pode mudar o cuidado à beira do leito
Como o método usa imagens que já são adquiridas durante a trombectomia, não exige exames, contraste ou radiação adicionais. Uma vez desenhadas as regiões de interesse — um passo que atualmente leva alguns minutos — o computador pode calcular automaticamente as medidas de fluxo e gerar uma estimativa personalizada de risco de sangramento. Em princípio, isso poderia ajudar médicos a ajustar metas pressóricas, decidir quão agressivamente usar medicamentos anticoagulantes e agendar tomografias mais precoces em pacientes identificados como de alto risco. Os autores alertam que seu estudo é retrospectivo e de um único centro, de modo que ensaios maiores e multicêntricos são necessários antes que a ferramenta possa orientar o cuidado rotineiro. Ainda assim, oferece uma prova de conceito clara: ao transformar angiogramas de AVC em dados numéricos ricos e permitir que o aprendizado de máquina os analise, podemos ir além de simplesmente perguntar “a artéria está aberta?” para “a microcirculação do cérebro está segura?” — uma mudança que pode, em última análise, poupar mais pacientes de sangramentos perigosos pós-tratamento.
Citação: Li, H., Pang, C., Guo, X. et al. Machine learning-enabled prediction of hemorrhagic transformation post-thrombectomy using quantitative DSA. Sci Rep 16, 6008 (2026). https://doi.org/10.1038/s41598-026-37036-6
Palavras-chave: acidente vascular cerebral, trombectomia mecânica, hemorragia cerebral, aprendizado de máquina, angiografia