Clear Sky Science · pt
Impacto dos tratamentos sistêmicos específicos para neoplasias neuroendócrinas na expressão e função de CXCR4 em células de tumor neuroendócrino
Por que isto importa para o cuidado oncológico futuro
Quando certos cânceres raros do intestino e do pâncreas se tornam mais agressivos, frequentemente deixam de responder aos tratamentos-alvo padrão. Médicos e pesquisadores precisam com urgência de novas maneiras de visualizar e atacar esses tumores mais resistentes. Este estudo faz uma pergunta prática com grandes implicações: os quimioterápicos e os medicamentos-alvo que os pacientes já recebem alteram um marcador tumoral chave chamado CXCR4, que está sendo desenvolvido tanto como um “farol” diagnóstico quanto como alvo terapêutico?
Um alvo que muda em células tumorais agressivas
As neoplasias neuroendócrinas são cânceres raros que surgem de células produtoras de hormônios, mais frequentemente no intestino e no pâncreas. Em sua forma inicial, mais ordenada, esses tumores geralmente apresentam uma molécula de superfície chamada receptor de somatostatina 2, que os médicos conseguem imagear e tratar com fármacos radioativos especializados. À medida que a doença se torna mais agressiva, esses tumores tendem a perder esse marcador, tornando-se mais difíceis de detectar e alvejar. Ao mesmo tempo, muitos deles ativam outra molécula de superfície, um receptor chamado CXCR4, associado a crescimento mais rápido, disseminação para órgãos distantes e pior sobrevida. Como o CXCR4 pode ser imageado com um traçador PET e potencialmente atacado com fármacos radioativos ou baseados em anticorpos, ele se tornou um promissor alvo “reserva” quando as opções padrão falham.
Testando drogas do mundo real em modelos celulares tumorais
Os pesquisadores quiseram saber como os medicamentos já usados para tratar tumores neuroendócrinos de alto grau afetam o próprio CXCR4. Se essas drogas reduzirem acidentalmente o CXCR4, podem enfraquecer futuras imagens ou terapias baseadas em CXCR4 — mas também podem ajudar a conter a agressividade do câncer. A equipe trabalhou com três diferentes linhagens celulares humanas que representam formas agressivas da doença, incluindo uma linhagem híbrida que reproduz de perto tumores especialmente difíceis de tratar. Eles expuseram essas células a seis agentes comuns: as quimioterapias cisplatina, etoposídeo, estreptozotocina, 5‑fluorouracil, a droga oral temozolomida e o inibidor alvo mTOR everolimo. Após o tratamento, mediram o CXCR4 nos níveis genético e proteico e testaram a capacidade das células de captar um traçador PET que busca o CXCR4.
Algumas drogas reduzem o sinal de CXCR4
Os resultados mostraram que nem todos os medicamentos oncológicos são iguais em relação a esse receptor. A cisplatina reduziu claramente a atividade genética do CXCR4 em duas das três linhagens celulares e cortou de forma significativa a captação do traçador em duas delas, indicando menos receptores funcionais para o ligante. A temozolomida e o everolimo também diminuíram os níveis genético e proteico de CXCR4 em várias linhagens, embora isso nem sempre tenha se traduzido em uma queda estatisticamente clara na captação do traçador. Em contraste, o etoposídeo e a estreptozotocina tiveram pouco efeito sobre o CXCR4, enquanto o 5‑fluorouracil produziu alterações modestas que não alteraram fortemente a ligação do traçador. No geral, o padrão sugere que cisplatina, temozolomida e everolimo podem reduzir o CXCR4 nessas células tumorais agressivas, enquanto os outros agentes o deixam principalmente inalterado.
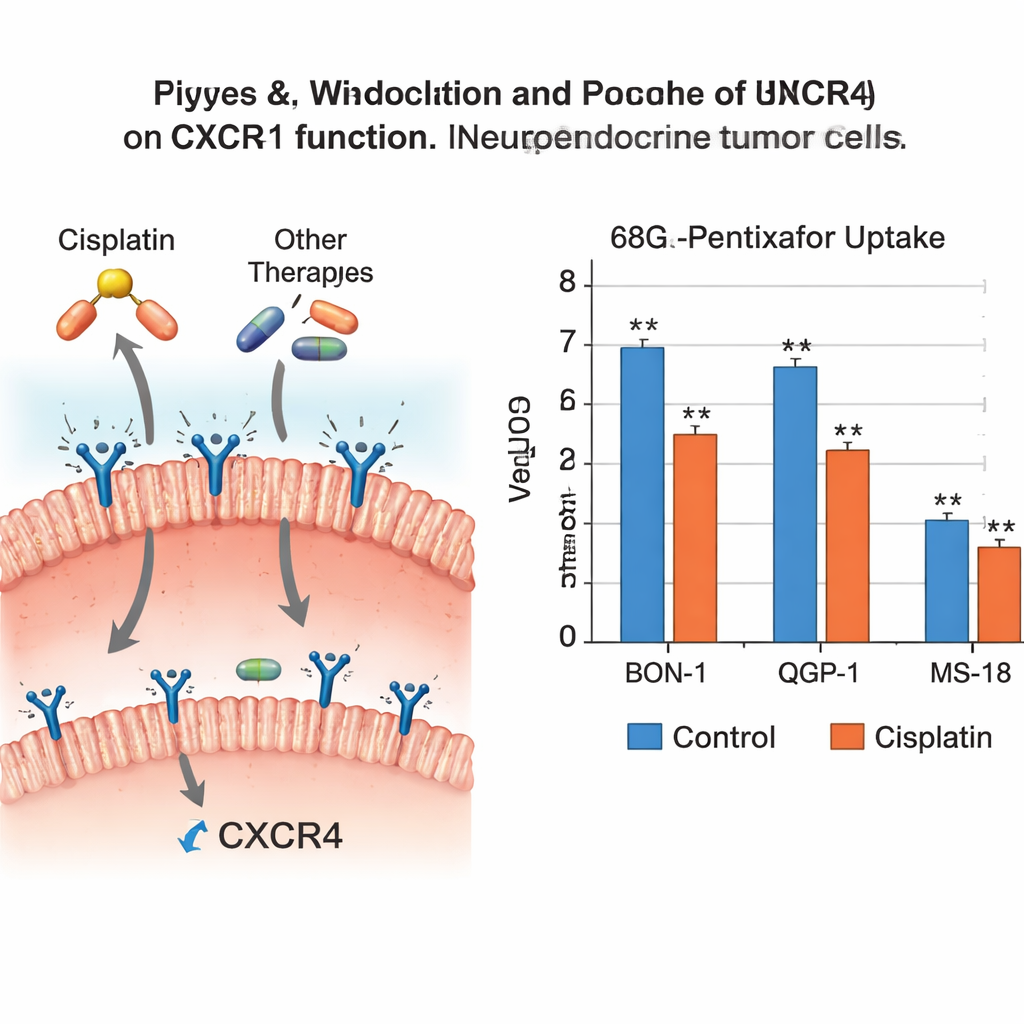
O que isso significa para exames e o momento do tratamento
Essas descobertas trazem uma mensagem dupla para o cuidado futuro dos pacientes. Por um lado, reduzir o CXCR4 pode fazer parte de como drogas como cisplatina, temozolomida e everolimo retardam a disseminação tumoral, já que altos níveis de CXCR4 estão ligados à invasividade e metástase. Por outro lado, se o CXCR4 de um tumor estiver suprimido por tratamento em curso, exames PET baseados em CXCR4 podem subestimar a extensão da doença, e terapias radioativas direcionadas ao CXCR4 podem ter menos pontos de ancoragem para atingir. O estudo sugere que combinar tratamentos direcionados ao CXCR4 diretamente com esses medicamentos sistêmicos é improvável de melhorar a eficácia das terapias centradas em CXCR4 e pode até atenuá-las.
Uma nova peça do quebra-cabeça para a terapia personalizada
Para não especialistas, a conclusão principal é que um único marcador tumoral pode desempenhar dois papéis ao mesmo tempo: pode ser um sinal de alerta de doença agressiva e, ao mesmo tempo, uma alça útil para imagem e tratamento direcionado. Esta pesquisa mostra que alguns medicamentos oncológicos estabelecidos podem ajustar discretamente esse marcador para cima ou para baixo. Na prática, isso poderia influenciar quando agendar exames e terapias baseadas em CXCR4 — idealmente quando o receptor estiver mais abundante — e pode ajudar a explicar por que certos tratamentos são eficazes contra tumores neuroendócrinos de crescimento rápido. Embora esses resultados provenham de modelos celulares e precisem de confirmação em pacientes, eles representam um passo importante rumo a um sequenciamento mais inteligente das terapias para pessoas com esses cânceres desafiadores.
Citação: Däubler, C., Böttcher, C., Landwehr, LS. et al. Impact of neuroendocrine neoplasm-specific systemic treatments on expression and function of CXCR4 in neuroendocrine tumor cells. Sci Rep 16, 4339 (2026). https://doi.org/10.1038/s41598-026-37026-8
Palavras-chave: tumores neuroendócrinos, CXCR4, cisplatina, everolimo, imagem direcionada