Clear Sky Science · pt
Imageamento de vida útil de fluorescência sem marcadores pode distinguir câncer de tecido saudável em tumores orais caninos de ocorrência espontânea
Vendo o Câncer sob Uma Nova Luz
Os cânceres orais, tanto em humanos quanto em animais de estimação, são notoriamente difíceis de remover por completo. Os cirurgiões precisam cortar margens “de segurança” amplas ao redor de um tumor para evitar deixar células cancerosas ocultas, mas na boca isso pode significar perda de osso, dentes e tecidos moles vitais que afetam a alimentação e a fala. Este estudo explora um método de imageamento baseado em luz usado durante a cirurgia em cães de companhia que pode ajudar os cirurgiões a distinguir, em tempo real, o tecido canceroso do saudável — potencialmente poupando mais tecido normal sem abrir mão do controle do câncer.
Por Que as Bordas dos Tumores São Tão Difíceis de Encontrar
Na cirurgia de cabeça e pescoço hoje, os médicos frequentemente dependem da análise rápida de tecido congelado para julgar se as margens de um tumor removido estão realmente livres de câncer. Esse processo é lento, amostra apenas pequenas áreas e pode deixar de detectar doença. Desafios semelhantes afetam o tratamento de cães com tumores orais, onde a recidiva local continua sendo comum. Como não existe um método confiável para “ver” o câncer microscópico durante a operação, os cirurgiões tipicamente removem margens generosas, o que pode prejudicar a mastigação, a deglutição e a aparência. Os autores buscaram testar uma abordagem de imageamento não invasiva que pudesse traçar uma linha mais nítida entre o câncer e o tecido normal diretamente na sala de cirurgia.
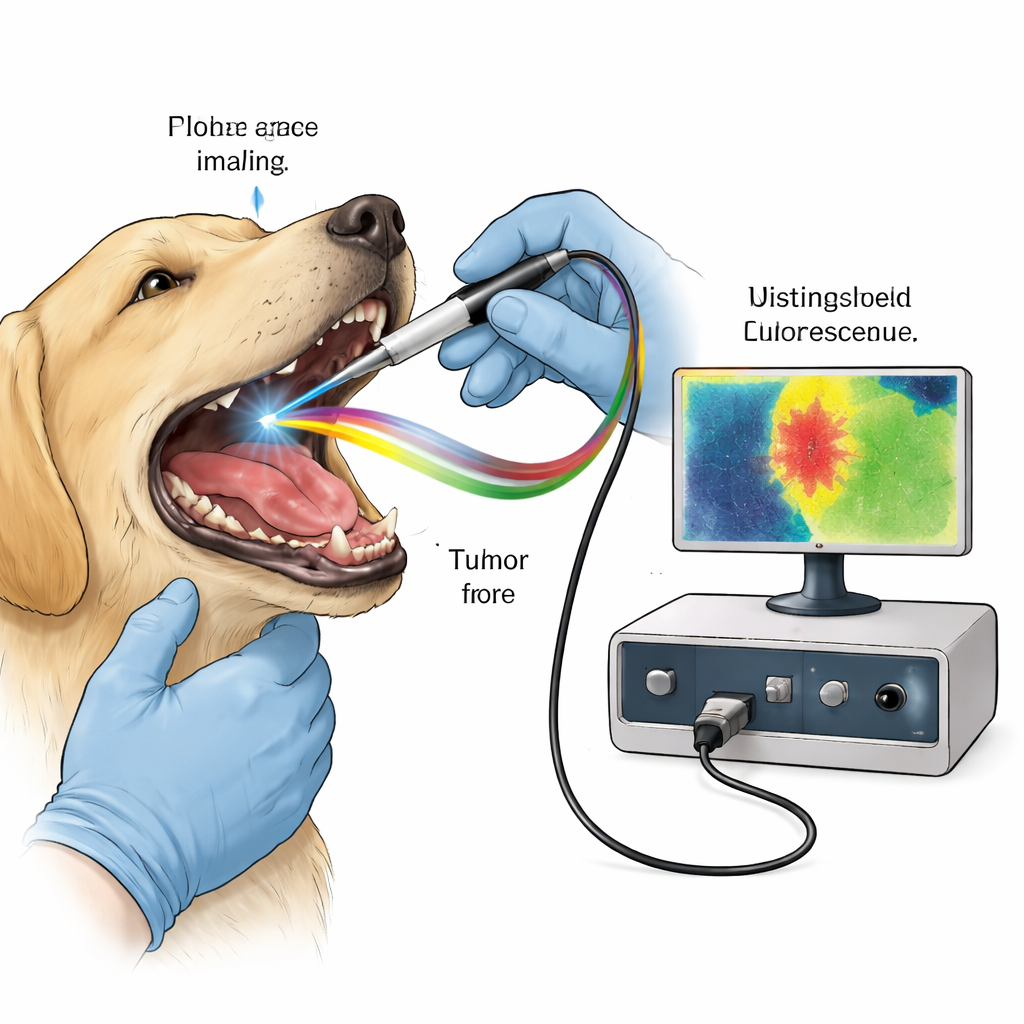
Usando o Brilho Natural como Guia Cirúrgico
Muitas moléculas nos nossos tecidos emitem naturalmente um fraco brilho fluorescente após serem excitadas por um pulso breve de laser. O colágeno no tecido conjuntivo e moléculas ligadas ao metabolismo celular, como NADH e FAD, têm cores e tempos característicos ao brilharem e apagarem. O câncer perturba a estrutura tecidual e o uso de energia, alterando sutismente essa impressão digital fluorescente. O imageamento da vida útil da fluorescência (FLIm) não mede apenas o quão brilhante o tecido brilha; mede quanto tempo esse brilho dura em bilionésimos de segundo, uma propriedade menos afetada pelas condições de observação. A equipe usou uma sonda manual personalizada que emite pulsos ultravioleta rápidos na região do tumor de cães anestesiados e registra a fluorescência retornada em três canais espectrais ajustados para colágeno, moléculas metabólicas e um composto emissor vermelho chamado protoporfirina IX (PpIX).
Adicionar um Corante que Procura o Câncer: Ajuda ou Exagero?
É possível fazer a PpIX acumular-se em muitos tumores administrando aos pacientes um fármaco precursor, o ácido 5-aminolevulínico (5-ALA), por via oral. Sob luz azul, áreas ricas em PpIX frequentemente brilham em rosa intenso e são usadas pelos cirurgiões para localizar o câncer. Os pesquisadores primeiro confirmaram em linhagens celulares de câncer oral canino que o 5-ALA levou a forte fluorescência de PpIX e mostraram que genes envolvidos na produção e importação de 5-ALA estavam mais ativos nas células cancerosas. Em seguida, inscreveram 15 cães de companhia com tumores orais de ocorrência natural e lhes administraram 5-ALA algumas horas antes da cirurgia. Na sala de cirurgia, a maioria dos tumores fluoresceu visivelmente, mas algumas lesões inflamatórias ou virais não cancerosas também acenderam, sugerindo que a cor visual sozinha pode não marcar de forma confiável as bordas do tumor.
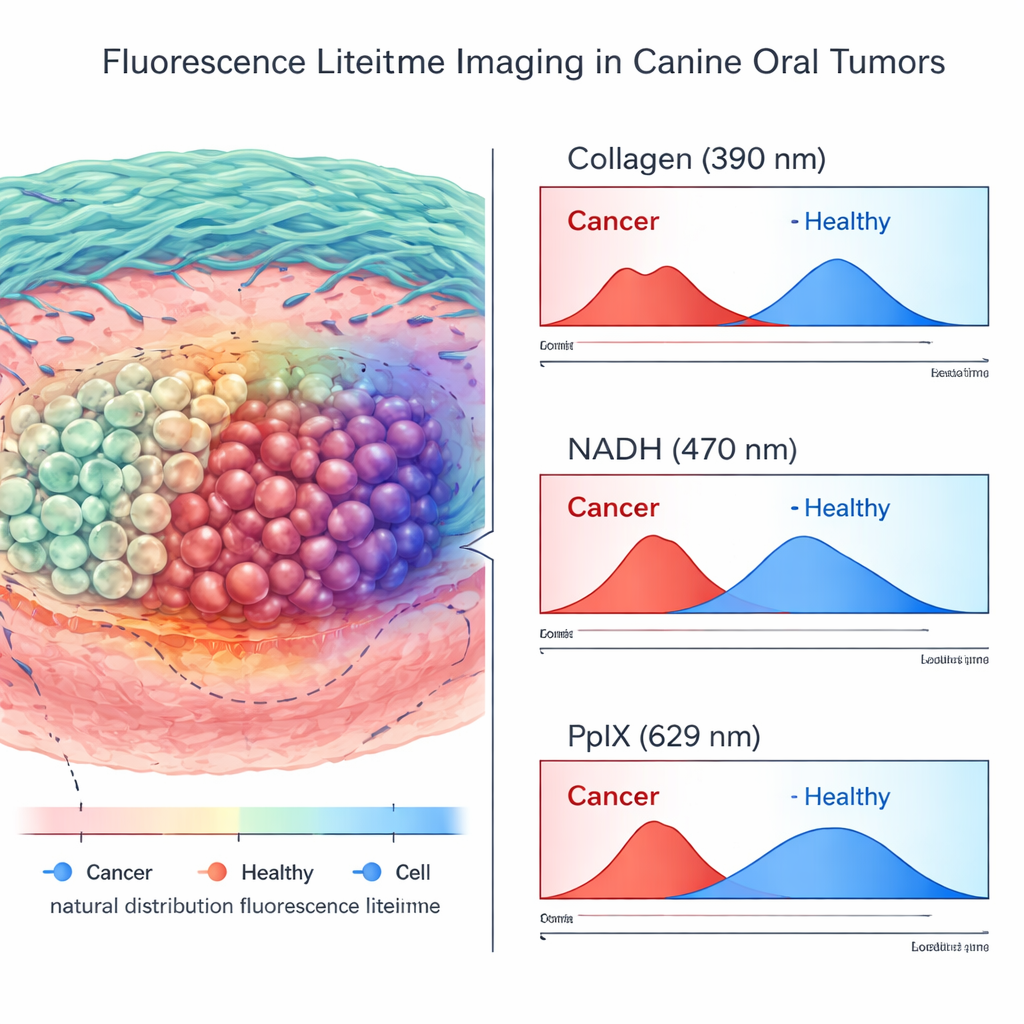
O Que as Imagens de Vida Útil Revelaram
Em mais de 200.000 pontos de medição de alta qualidade provenientes de tumores e tecidos normais próximos, a equipe comparou os sinais de FLIm com mapas patológicos detalhados. Eles descobriram que muitas características de vida útil e intensidade diferiam significativamente entre tecido canceroso e saudável. No entanto, a separação mais forte e consistente veio dos canais sem marcação: vidas úteis mais curtas na faixa sensível ao colágeno e mudanças características na faixa sensível ao NADH estavam fortemente associadas ao câncer. Em contraste, o canal de PpIX — aquele potencializado pelo 5-ALA administrado — forneceu informações menos confiáveis em tecido vivo. Suas medições variaram amplamente em regiões normais, provavelmente porque gengivas e mucosas inflamadas acumulavam 5-ALA ou continham porfirinas fluorescentas naturais que imitavam o sinal tumoral.
Da Sala de Cirurgia ao Laboratório e de Volta
Quando os pesquisadores imagearam as amostras removidas na mesa de trabalho, o quadro mudou ligeiramente. Fora do corpo, algumas características baseadas em PpIX tornaram-se mais úteis para distinguir câncer de tecido saudável, sugerindo um papel potencial em checagens de margem “à beira da cadeira”. Ainda assim, quando modelos estatísticos sofisticados e aprendizado de máquina foram aplicados, os classificadores de melhor desempenho tanto para dados intraoperatórios quanto ex-operatórios apoiaram-se fortemente nos sinais de autofluorescência natural em vez do corante adicionado. O FLIm sem marcador alcançou precisão respeitável em distinguir câncer de tecido normal por si só, enquanto a inclusão de PpIX adicionou pouco e às vezes introduziu confusão.
O Que Isso Significa para Cirurgias Futuras
Para proprietários de animais de estimação e, em última instância, pacientes humanos, a mensagem principal é que os cirurgiões podem um dia dispor de uma ferramenta baseada em luz que os ajude a ver onde o câncer termina e o tecido saudável começa, sem depender de drogas ou corantes adicionais. Este trabalho em cães — um modelo realista de grande porte para o câncer oral humano — mostra que as assinaturas fluorescentes naturais do próprio corpo podem ser suficientes para orientar decisões na sala de cirurgia. A adição de 5-ALA e PpIX neste contexto não melhorou a precisão o bastante para justificar o custo, a complexidade e os potenciais efeitos colaterais extras. Os autores concluem que esforços futuros devem focar no aprimoramento do imageamento de vida útil da fluorescência sem marcadores — possivelmente adaptando a análise a sítios anatômicos específicos — em vez de buscar mais agentes de contraste. Se bem-sucedida, essa tecnologia poderia reduzir reoperações e preservar mais tecido normal, mantendo o câncer sob controle.
Citação: Goldschmidt, S., Marcu, L., Ehrlich, K. et al. Label-free fluorescence lifetime imaging can distinguish cancer from healthy tissue in spontaneously occurring canine oral tumors. Sci Rep 16, 6077 (2026). https://doi.org/10.1038/s41598-026-37001-3
Palavras-chave: imageamento de câncer oral, tumores orais caninos, vida útil da fluorescência, margens cirúrgicas, 5-ALA PpIX