Clear Sky Science · pt
Sequenciamento de amplicons com Oxford Nanopore Technologies como alternativa diagnóstica para lentivírus de pequenos ruminantes em ovinos
Infecções ocultas em ovinos do dia a dia
Ovinos ao redor do mundo carregam silenciosamente vírus que podem reduzir sua saúde, encurtar suas vidas e causar prejuízos aos produtores—muitas vezes sem sintomas óbvios durante anos. Este estudo explora uma nova forma de revelar essas infecções ocultas usando uma tecnologia portátil de sequenciamento de DNA, oferecendo um possível avanço na forma como protegemos o bem-estar animal, a renda das fazendas e até a segurança alimentar.
Uma doença lenta, cara e difícil de detectar
O trabalho foca nos lentivírus de pequenos ruminantes (SRLV), um grupo de vírus que infecta ovinos e caprinos. Em ovinos, causam a doença Maedi-Visna, uma infecção de longa duração que pode levar a problemas respiratórios, artrite, doença neurológica e inflamação crônica da glândula mamária. Muitos animais infectados nunca exibem sinais claros, ainda assim o vírus reduz a produção de leite, aumenta a mortalidade de cordeiros e força o abate precoce. Em alguns rebanhos leiteiros europeus, incluindo na Espanha e na Grécia, cerca de metade dos animais pode estar infectada, tornando essa uma das doenças mais importantes em ovinos de produção intensiva.
Por que os testes atuais deixam muitos infectados passar
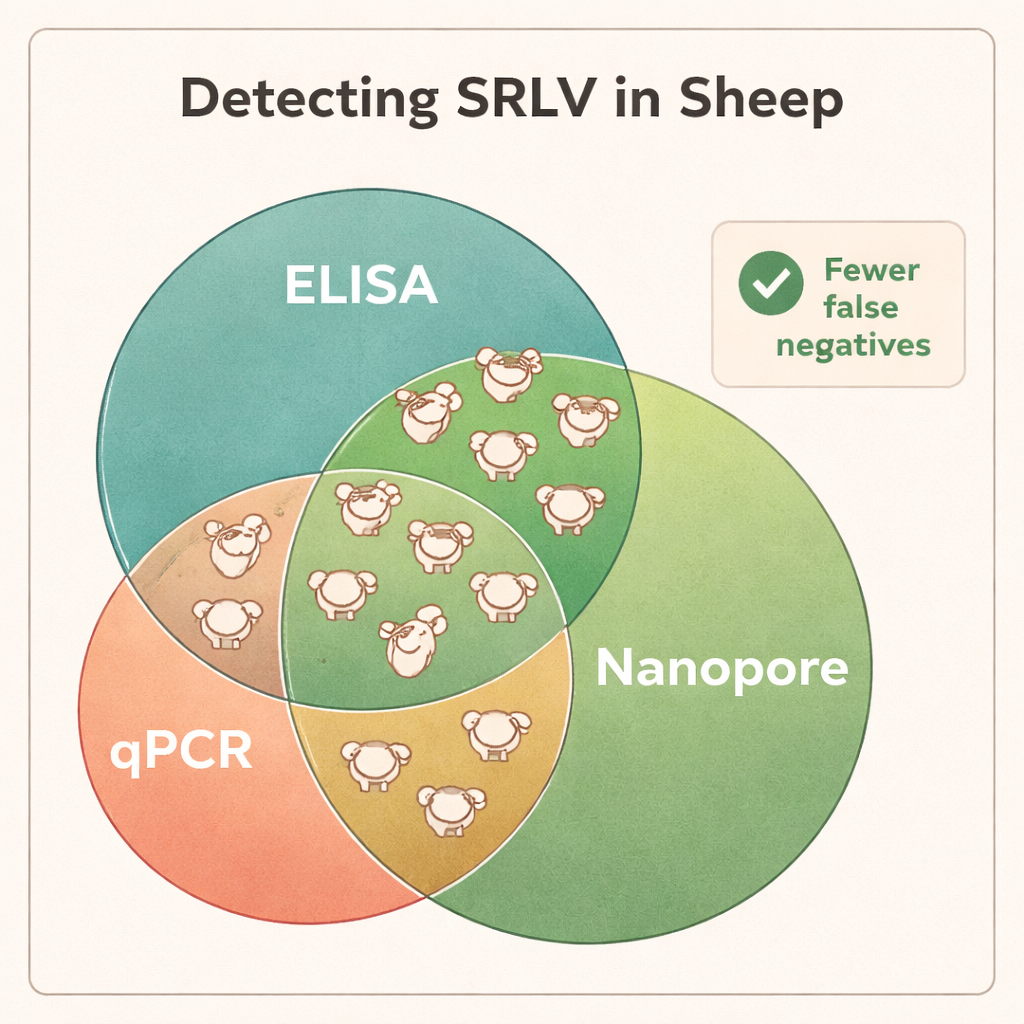
Hoje, as fazendas dependem principalmente de testes sanguíneos que detectam anticorpos (ELISA) ou de testes de DNA padrão (qPCR) para decidir quais animais estão infectados e devem ser removidos do rebanho. Mas os SRLVs mutam e recombinam rapidamente, gerando muitas variantes virais ligeiramente diferentes. Algumas variantes são pouco reconhecidas pelos testes de anticorpos, e alguns ovinos infectados nunca desenvolvem respostas anticorpos fortes. O qPCR, que mira trechos curtos e muito específicos do DNA viral, também pode falhar se essas regiões-alvo mudarem. Como resultado, muitos animais realmente infectados testam negativo e permanecem no rebanho, espalhando o vírus silenciosamente.
Usando leitura em tempo real do DNA para encontrar o vírus
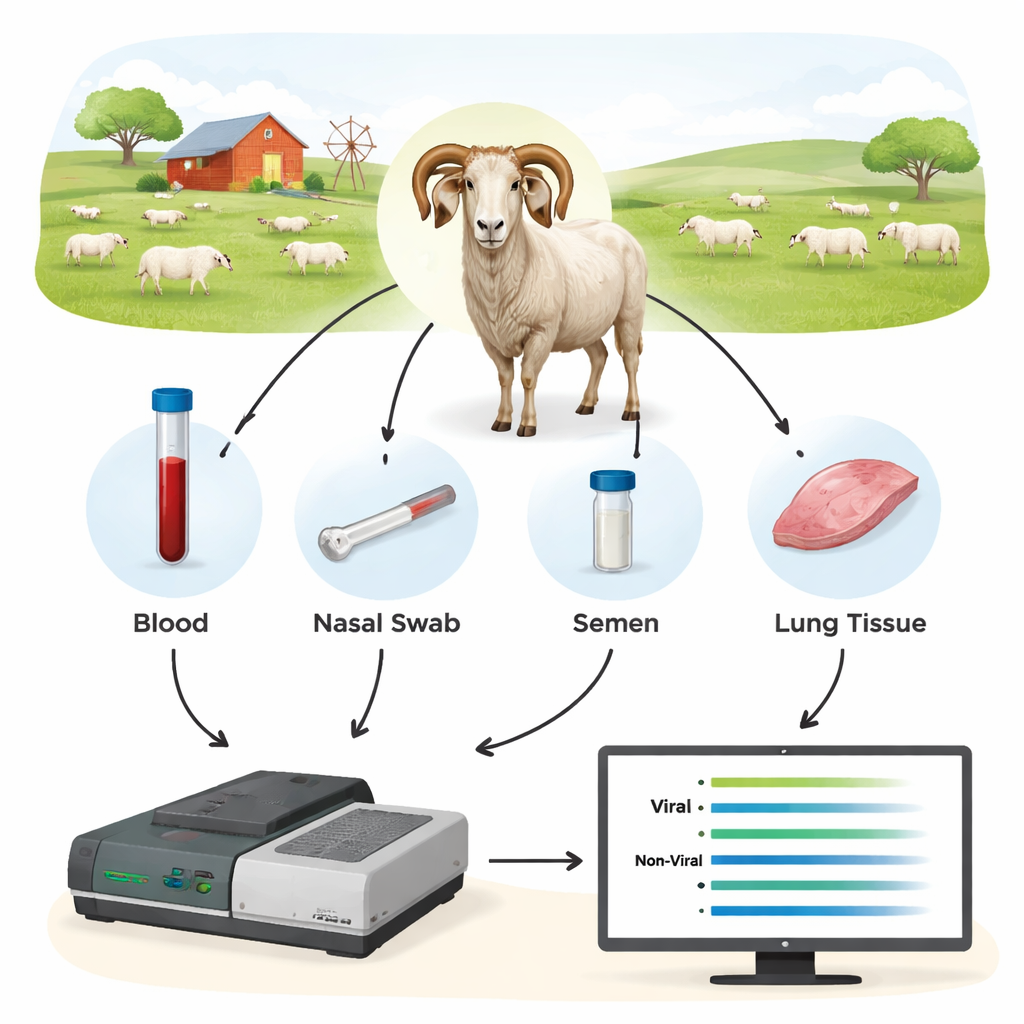
Os pesquisadores testaram um método de terceira geração chamado sequenciamento Oxford Nanopore como um novo tipo de ferramenta diagnóstica. Em vez de procurar um único e minúsculo trecho de DNA viral, eles primeiro amplificaram trechos mais longos de genes virais-chave a partir das amostras dos animais e então sequenciaram esses fragmentos em tempo real em um dispositivo Nanopore. Coletaram sangue, swabs nasais, sêmen e células de sangue e pulmão de 44 carneiros e ovinos adicionais, muitos dos quais já haviam sido testados por métodos convencionais. Ao focar em regiões virais relativamente conservadas, mas longas o bastante para revelar a estirpe exata, a equipe pôde tanto detectar a infecção quanto identificar quais tipos virais estavam presentes.
Sangue funciona melhor—e encontra o que outros testes perdem
O sequenciamento mostrou que o DNA do sangue total foi o material mais confiável para descobrir SRLV, mesmo que o vírus viva principalmente em um pequeno subconjunto de leucócitos. Tecidos pulmonares de animais fortemente infectados forneceram quantidades muito altas de DNA viral, mas tais amostras só estão disponíveis após o abate. Em contraste, swabs nasais, sêmen e leucócitos purificados ofereceram material viral insuficiente para diagnóstico consistente. Quando os cientistas compararam os resultados do Nanopore com os testes padrão ELISA e qPCR, as diferenças foram marcantes: o sequenciamento Nanopore confirmou a infecção em todos os carneiros positivos por ELISA, mas também revelou que muitos animais negativos por ELISA estavam, de fato, infectados. Entre diferentes rebanhos, cerca de 40–45% dos animais rotulados como “negativos” pelo ELISA acabaram por carregar o vírus, e o qPCR deixou escapar uma parcela ainda maior. Os dados de sequenciamento também revelaram coinfecções com diferentes tipos de SRLV em alguns carneiros, informação que os testes tradicionais não fornecem facilmente.
De respostas simples sim/não a percepções mais profundas
Como o Nanopore lê as sequências virais reais, ele pode ir além de um diagnóstico simples de sim ou não. A equipe usou os dados para comparar estirpes virais, construir árvores filogenéticas dos vírus circulantes em seus rebanhos e estudar diferenças sutis em proteínas virais que podem explicar por que alguns animais escapam da detecção por kits ELISA padrão. Demonstraram que certas versões de uma proteína viral-chave, alvo dos testes comerciais de anticorpos, diferem notavelmente entre animais soropositivos e soronegativos. Com o tempo, essas informações poderiam ajudar a refinar tanto os testes sorológicos quanto programas de seleção voltados a escolher animais naturalmente mais resistentes à infecção.
O que isso significa para produtores e saúde animal
Para não-especialistas, a mensagem central é direta: ao ler trechos mais longos do DNA viral diretamente, o sequenciamento Nanopore pode revelar mais ovinos infectados, mais cedo e com mais precisão do que os testes rotineiros atuais. Ele também informa quais estirpes virais exatas estão presentes em um rebanho. Embora essa abordagem ainda seja mais complexa e custosa que um único exame de sangue, a tecnologia está se tornando mais rápida, barata e portátil. Se integrada a programas de controle, ela poderia reduzir drasticamente o número de portadores “ocultos”, melhorar o desenho de vacinas e testes e apoiar a seleção de animais mais resistentes—tornando a ovinocultura mais sustentável e humana.
Citação: Serrano, M., González, C., Roy, R. et al. Amplicon sequencing with Oxford nanopore technologies as a diagnostic alternative for small ruminant lentiviruses in sheep. Sci Rep 16, 6212 (2026). https://doi.org/10.1038/s41598-026-36989-y
Palavras-chave: saúde de ovinos, lentivírus, sequenciamento nanopore, diagnóstico veterinário, Maedi-Visna