Clear Sky Science · pt
Análise proteômica quantitativa do plasma após condicionamento isquêmico remoto em acidente vascular cerebral isquêmico agudo
Por que apertar um braço pode ajudar a proteger o cérebro
Quando alguém tem um AVC causado por um vaso sanguíneo bloqueado, cada minuto de fluxo sanguíneo perdido ameaça as células cerebrais. Os tratamentos padrão visam reabrir a artéria obstruída, mas muitos pacientes chegam tarde demais ou não são elegíveis. Pesquisadores exploram uma terapia adjuvante surpreendentemente simples: interromper brevemente o fluxo sanguíneo em um braço ou perna com um manguito de pressão arterial, uma estratégia chamada condicionamento isquêmico remoto (RIC). Este estudo faz uma pergunta-chave para transformar essa ideia em terapia real: o que exatamente o RIC altera no sangue de pacientes com AVC, e essas mudanças poderiam apontar quem poderia se beneficiar mais?
Um sinal suave de estresse enviado do membro ao cérebro
O RIC funciona inflando repetidamente um manguito em um membro por alguns minutos e depois desinflando-o, criando episódios curtos e inofensivos de baixo fluxo sanguíneo. Experimentos em animais e ensaios clínicos iniciais sugerem que esse “estresse controlado” pode sinalizar órgãos distantes, incluindo o cérebro, para ativar programas de proteção. Em um grande ensaio clínico chamado RICAMIS, pacientes com AVC isquêmico moderado que receberam RIC além dos cuidados usuais tiveram melhor evolução aos 90 dias do que aqueles que receberam apenas os cuidados habituais. No entanto, outro ensaio (RESIST) não observou esse benefício, deixando os médicos incertos sobre quando e para quem o RIC realmente funciona. O estudo atual investiga o sangue dos pacientes em busca de pistas moleculares — proteínas mensuráveis, ou biomarcadores, que mudam ao longo do tempo com o RIC.
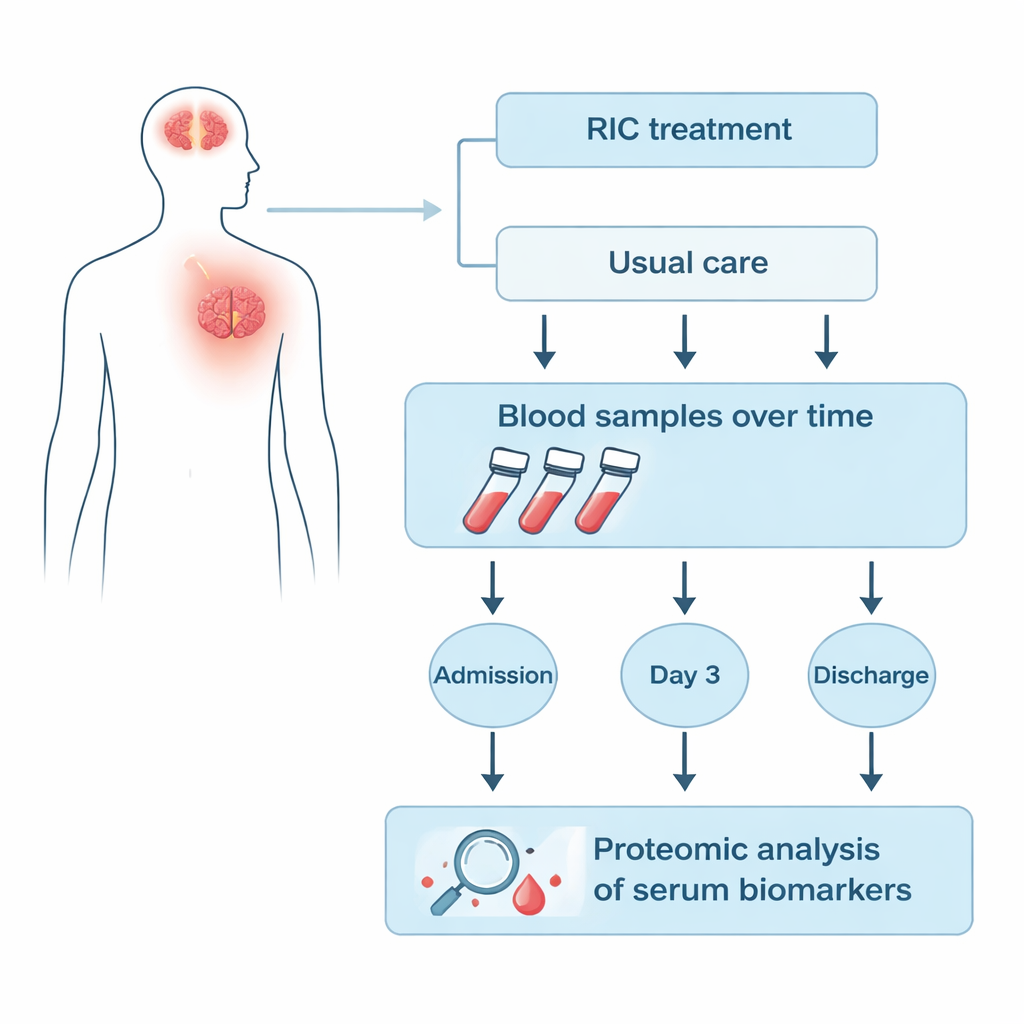
Acompanhando o sangue dos pacientes durante a internação
Os pesquisadores focaram em 25 pacientes do ensaio RICAMIS que tiveram amostras de sangue coletadas em três momentos: na admissão, três dias após a atribuição do tratamento e na alta hospitalar. Nove pacientes receberam RIC além dos cuidados usuais, enquanto dezesseis receberam apenas os cuidados habituais. Usando uma técnica chamada proteômica quantitativa, a equipe mediu centenas de proteínas na porção sérica do sangue de uma só vez, em vez de analisar apenas alguns marcadores pré‑selecionados. Em seguida, compararam como o nível de cada proteína subiu ou caiu ao longo do tempo no grupo RIC em relação ao grupo controle para encontrar assinaturas que estivessem exclusivamente ligadas ao RIC.
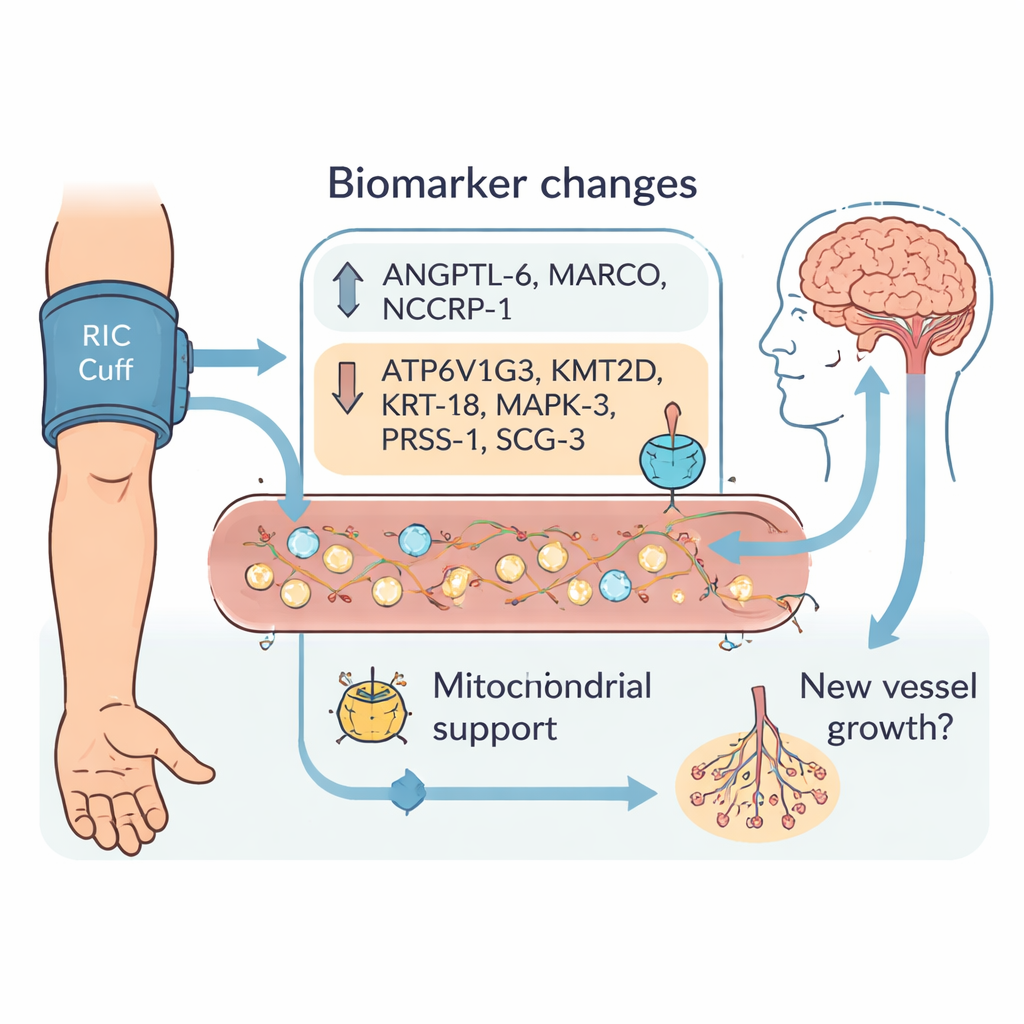
Nove sinais que se destacam na corrente sanguínea
Ao longo da internação, várias dezenas de proteínas variaram de forma diferente entre os dois grupos. Após filtragem cuidadosa, a equipe destacou nove biomarcadores cujas mudanças da admissão ao dia 3 e até a alta separaram claramente os pacientes tratados com RIC dos controles. Três proteínas — ANGPTL‑6, MARCO e NCCRP‑1 — aumentaram mais com RIC. Seis outras — ATP6V1G3, KMT2D, KRT‑18, MAPK‑3, PRSS‑1 e SCG‑3 — tenderam a diminuir. Muitas dessas moléculas estão envolvidas em como as células gerenciam energia em suas pequenas usinas, as mitocôndrias, ou em como novos vasos sanguíneos crescem e se remodelam. Isso corrobora a ideia de que o RIC não se limita a proteger neurônios do dano, mas pode ajudar regiões cerebrais lesionadas a se reorganizar, reparar seu suprimento sanguíneo e recuperar função ao longo de dias a semanas.
Pistas sobre uso de energia e crescimento de novos vasos
Para entender melhor o que essas nove proteínas podem estar fazendo, os autores as mapearam em vias biológicas conhecidas. Duas delas, KMT2D e MAPK‑3, estão conectadas a como o DNA é empacotado e como genes são ligados ou desligados, especialmente em programas relacionados ao crescimento vascular. Outras, como ATP6V1G3 e KRT‑18, foram associadas em trabalhos anteriores à manutenção de mitocôndrias saudáveis e à proteção do tecido cardíaco após lesão. Em conjunto, esses padrões apontam para o RIC empurrando o corpo em direção a um uso de energia mais eficiente e incentivando o crescimento ou remodelamento de vasos — potencialmente melhorando o fluxo sanguíneo ao redor da área danificada pelo AVC. Ao mesmo tempo, alguns marcadores, como NCCRP‑1 e MARCO, podem refletir as respostas agudas de estresse e imunes do corpo ao procedimento de inflação do manguito, ressaltando que o RIC desencadeia uma reação corporal complexa.
O que isso significa para o cuidado futuro do AVC
Este pequeno estudo exploratório não pode provar exatamente como o RIC protege o cérebro, e envolveu apenas 25 pacientes de um único país, portanto os achados precisam de confirmação em grupos muito maiores e mais diversos. Ainda assim, identificar uma lista curta de nove proteínas que se movem consistentemente em direções opostas com e sem RIC é um passo importante. No futuro, esses biomarcadores poderiam ajudar médicos a dizer rapidamente se o RIC está “fazendo efeito” em um paciente, orientar a escolha de quem deve recebê‑lo ou até inspirar tratamentos farmacológicos que imitem seus efeitos benéficos sem o manguito. Por enquanto, o trabalho reforça uma ideia simples, porém poderosa: ao estressar com segurança uma parte do corpo, podemos conseguir induzir o cérebro a um estado mais resiliente e melhor apto a se curar após um AVC.
Citação: Cui, Y., Liu, F., Cai, JR. et al. Quantitative proteomic analysis of plasma after remote ischemic conditioning in acute ischemic stroke. Sci Rep 16, 6106 (2026). https://doi.org/10.1038/s41598-026-36968-3
Palavras-chave: acidente vascular cerebral isquêmico agudo, condicionamento isquêmico remoto, biomarcadores séricos, análise proteômica, neuroproteção