Clear Sky Science · pt
Uma subpopulação pró-inflamatória de neutrófilos impulsiona a lesão por isquemia–reperfusão intestinal via a via de estresse do retículo endoplasmático mediada por ATF4
Quando o Fluxo Sanguíneo Prejudica o Intestino
Cirurgiões e médicos de terapia intensiva há muito se deparam com um paradoxo perigoso: quando o suprimento de sangue para o intestino é interrompido e depois restabelecido, o próprio restabelecimento do fluxo pode danificar gravemente o revestimento intestinal. Esse processo, chamado lesão por isquemia–reperfusão intestinal, pode levar a complicações potencialmente fatais, como sepse e falência múltipla de órgãos. O estudo resumido aqui revela que nem todas as células imunes que correm ao local são iguais — um subconjunto especialmente agressivo de glóbulos brancos desempenha um papel central em transformar uma resposta que salva vidas em algo prejudicial.
A Frágil Muralha Protetora do Intestino
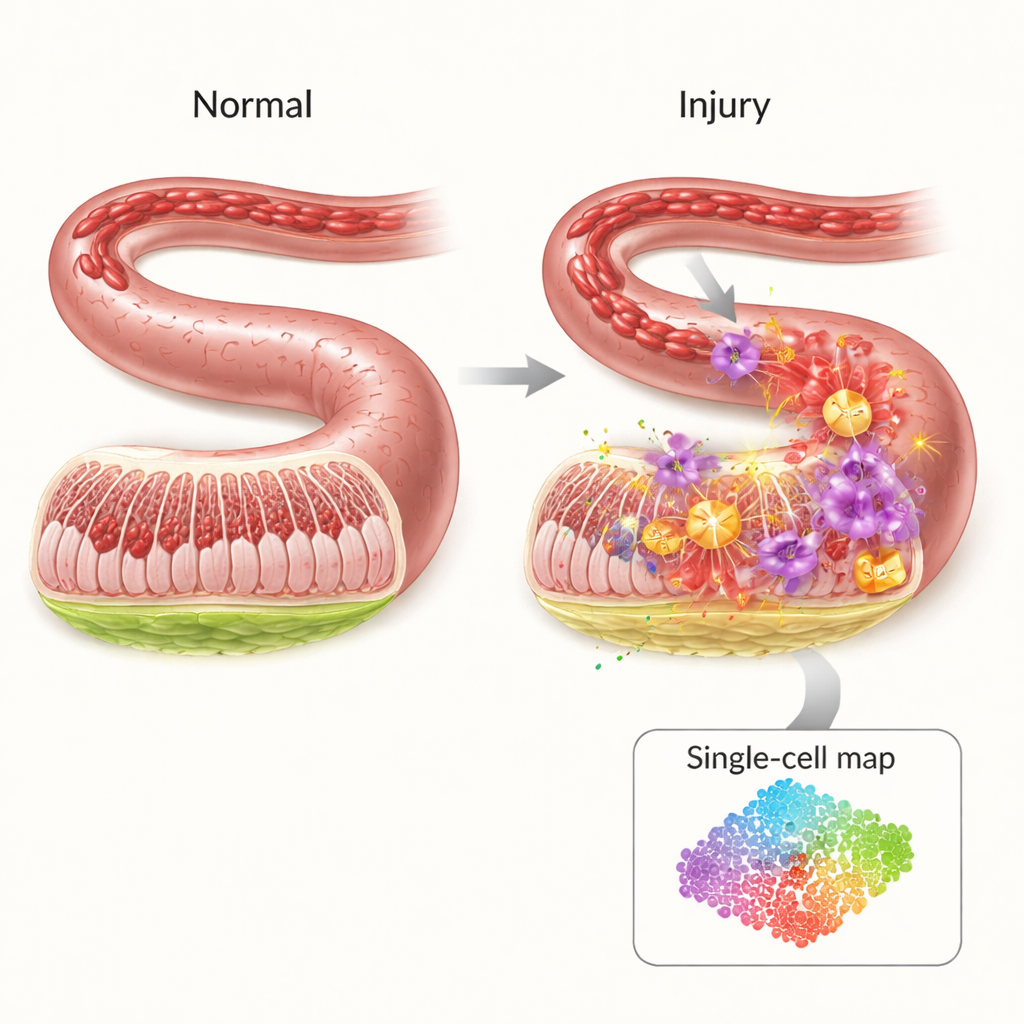
O interior do intestino é revestido por uma barreira fina, porém altamente organizada, que mantém bactérias e toxinas confinadas ao trato gastrointestinal enquanto permite a passagem de nutrientes. Quando o fluxo sanguíneo é interrompido — por exemplo durante choque, grandes cirurgias ou traumas graves — essa barreira fica privada de oxigênio. Surpreendentemente, a maior parte do dano ocorre não durante a falta de sangue em si, mas quando a circulação retorna. A súbita chegada de oxigênio e células imunes desencadeia uma tempestade de sinais inflamatórios e moléculas reativas que podem abrir brechas na parede intestinal, permitindo que germes vazem para a corrente sanguínea. Apesar de sua importância clínica, os médicos atualmente dispõem de poucos tratamentos direcionados para prevenir essa cascata.
Aproximando-se das Células Individuais
Para descobrir quem faz o quê durante essa crise, os pesquisadores usaram sequenciamento de RNA de célula única, uma técnica que identifica quais genes estão ativos em milhares de células individuais ao mesmo tempo. Em um modelo murino de isquemia–reperfusão intestinal, eles compararam intestinos lesionados a saudáveis e mapearam 19 tipos celulares principais. Constatou-se que certas células imunes — especialmente neutrófilos e monócitos inflamatórios — se expandiram dramaticamente após a lesão, enquanto células protetoras como linfócitos T, B e células natural killer diminuíram. As redes de comunicação entre os tipos celulares também mudaram, com os neutrófilos emergindo como centros que enviam e recebem muitos sinais inflamatórios, indicando-os como motores-chave do dano.
Um Subconjunto Nocivo de Células Primeiras-Respondentes
Os neutrófilos estão entre os primeiros respondedores mais rápidos do corpo, deslocando-se pela corrente sanguínea para combater infecções e remover detritos. Mas este estudo mostra que, dentro da população de neutrófilos, um subgrupo particularmente agressivo é responsável por grande parte do dano colateral no intestino. Quando os cientistas deplecionaram neutrófilos em camundongos antes de induzir isquemia–reperfusão, os animais apresentaram menos encurtamento intestinal, níveis mais baixos de marcadores de lesão no sangue, melhor aparência tecidual ao microscópio e proteínas de selamento mais intactas no revestimento intestinal. Em experimentos de co-cultura, neutrófilos obtidos de camundongos lesionados prejudicaram diretamente células intestinais, reduzindo sua sobrevivência, aumentando a morte celular e desorganizando proteínas “fechadura” essenciais que mantêm a barreira intestinal íntegra.
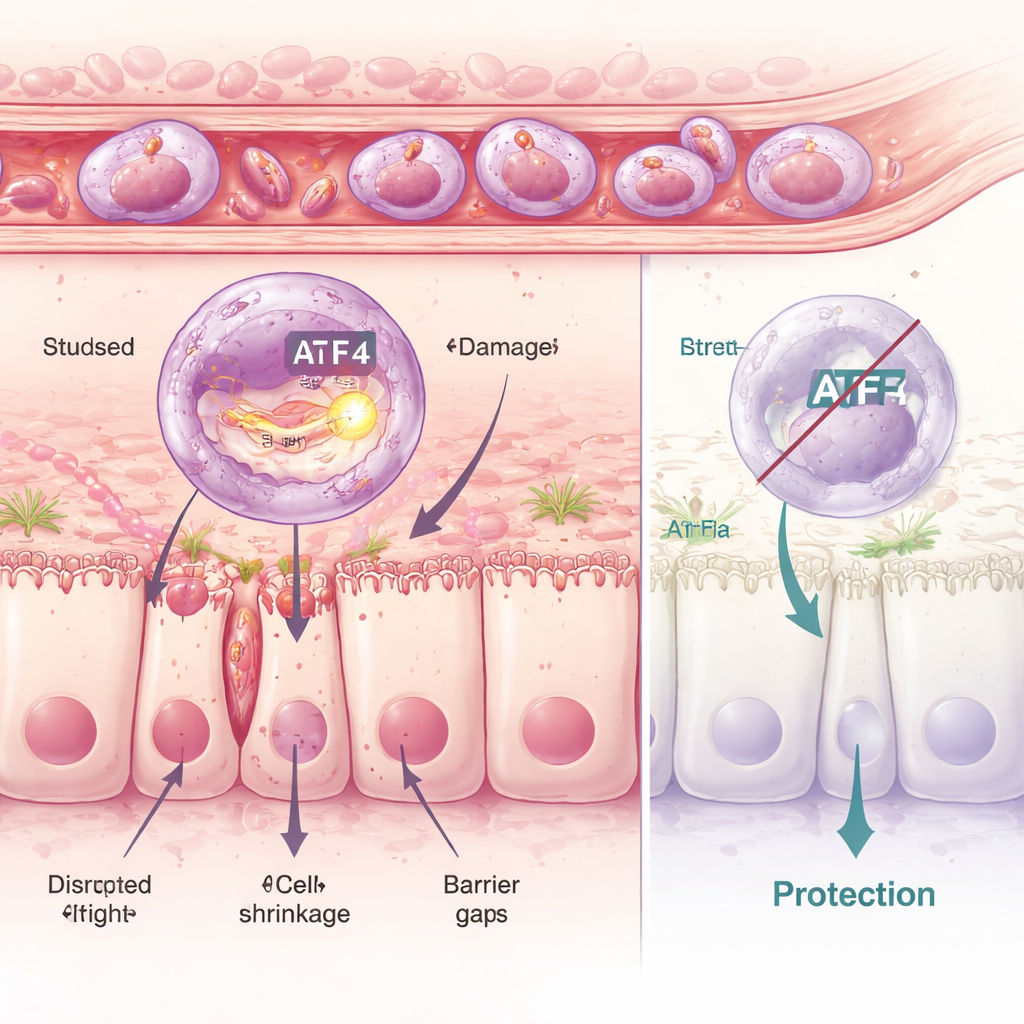
Estresse Dentro das Células: Quando o Controle de Qualidade Falha
Aprofundando-se, os pesquisadores examinaram neutrófilos um a um e identificaram seis subgrupos distintos. Um deles, chamado aglomerado C5, destacou-se por seu forte perfil inflamatório e por ativar um programa molecular de estresse dentro de uma estrutura chamada retículo endoplasmático, a oficina de dobramento de proteínas da célula. Um controlador-chave desse programa é uma proteína denominada ATF4. Nas células C5 nocivas, ATF4 e seus genes-alvo estavam altamente ativos. Ao usar fármacos que aumentam ou reduzem essa resposta interna de estresse, a equipe mostrou que mais estresse significava mais dano intestinal, enquanto bloqueá-lo preservava a barreira. Camundongos geneticamente modificados para não expressar ATF4 ficaram amplamente protegidos: mesmo quando drogas que induzem estresse foram administradas, seus neutrófilos já não conseguiam executar plenamente o programa danoso, e o revestimento intestinal permaneceu muito mais íntegro.
O que Isso Significa para Tratamentos Futuros
Em conjunto, esses achados desenham um panorama claro para não especialistas: entre o enxame de células imunes que inundam o intestino quando o fluxo sanguíneo retorna, um subconjunto específico de neutrófilos primado pelo estresse age como uma equipe de limpeza zelosa demais que derruba o prédio junto com os detritos. Seu poder destrutivo depende de uma via de estresse interna controlada por ATF4. Abafar essa via — sem eliminar todos os neutrófilos — poderia oferecer uma forma de proteger o intestino durante eventos de alto risco, como grandes cirurgias, infecções graves ou traumas. Embora mais trabalho seja necessário para confirmar esses resultados em humanos e para encontrar fármacos seguros e precisos, o estudo abre uma rota promissora para terapias que mantenham a barreira intestinal íntegra quando os pacientes mais precisam.
Citação: Yang, Y., Zhou, Q., Liu, S. et al. A pro-inflammatory neutrophil subpopulation drives intestinal ischemia–reperfusion injury via the ATF4-mediated endoplasmic reticulum stress pathway. Sci Rep 16, 6117 (2026). https://doi.org/10.1038/s41598-026-36938-9
Palavras-chave: barreira intestinal, isquemia reperfusão, neutrófilos, estresse do retículo endoplasmático, ATF4