Clear Sky Science · pt
Síntese e avaliação anticâncer de novos derivados tioimidazólicos contendo um grupo trimetoxicinila
Novas ferramentas químicas na luta contra o câncer
Os medicamentos de quimioterapia frequentemente danificam células saudáveis junto com os tumores, levando a efeitos colaterais severos. Este estudo explora uma nova família de moléculas sintéticas que buscam atingir as células cancerosas muito mais fortemente do que o tecido normal. Ao unir de maneira inteligente dois blocos químicos já conhecidos por funcionarem bem em medicamentos, os pesquisadores criaram compostos que exibem potente e direcionada morte de células cancerosas em modelos de tubo de ensaio e tumorais 3D, enquanto deixam as células saudáveis, em grande parte, intactas.
Construindo moléculas anticâncer mais inteligentes
A equipe concentrou-se em duas estruturas químicas “privilegiadas” que reaparecem em medicamentos de sucesso. Uma é o imidazol, um anel pequeno que se encaixa bem em muitos alvos biológicos. A outra é um grupo trimetoxifenil (TMP), um padrão de três cadeias laterais que contêm oxigênio em um anel aromático que é central em diversos fármacos anticâncer que perturbam a divisão celular. Ao introduzir um átomo de enxofre no núcleo do imidazol (criando um tioimidazol) e ligá-lo a um grupo TMP, os químicos pretendiam ajustar como as moléculas se deslocam no organismo e quão fortemente se ligam a proteínas relacionadas ao câncer. Usando uma rota sintética em etapas, eles construíram uma biblioteca de compostos relacionados, cada um sutilmente modificado para investigar que características importam mais para a atividade anticâncer. 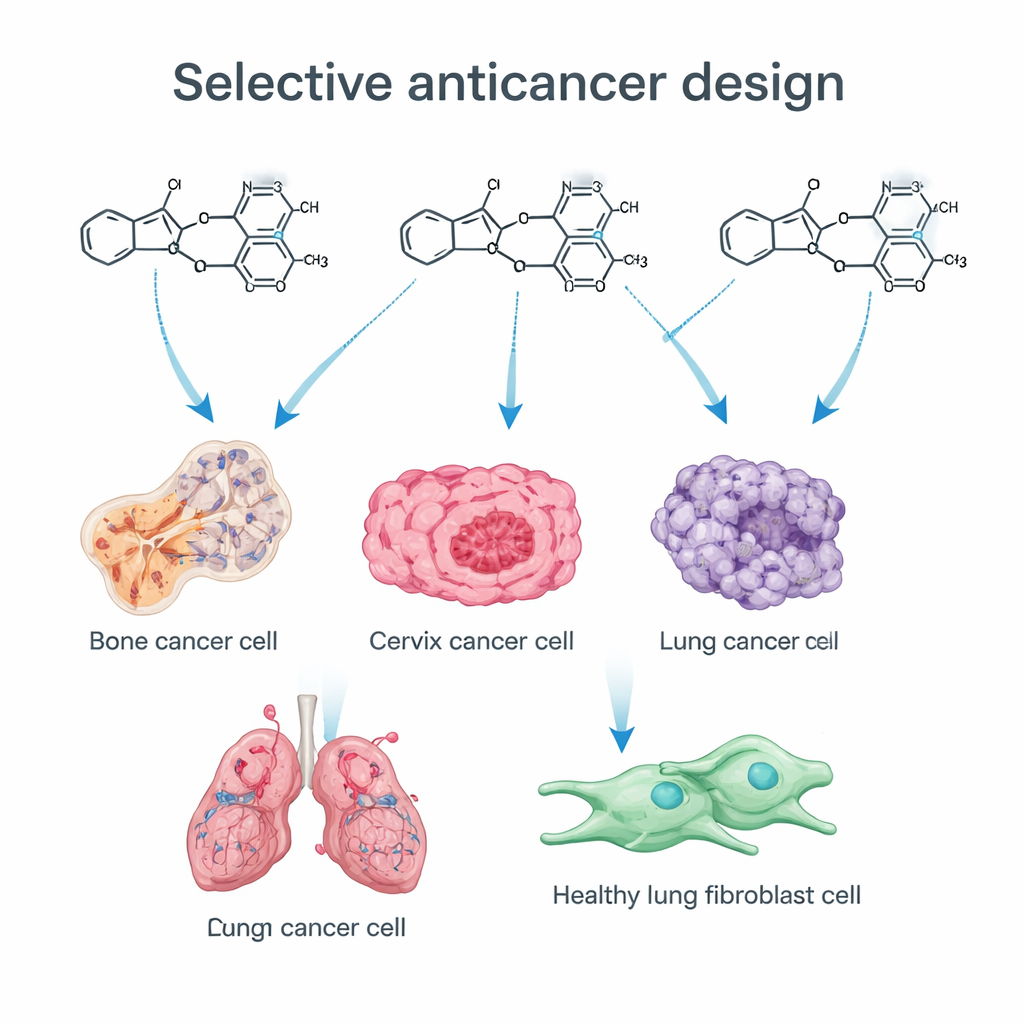
Testando células cancerosas enquanto poupam tecido saudável
As novas moléculas foram testadas em quatro linhagens de células humanas cancerosas — osteossarcoma (osso), cervical, colorretal e de pulmão — bem como em fibroblastos pulmonares não cancerosos. Muitos dos compostos retardaram ou cessaram o crescimento das células cancerosas, mas um em particular, denominado 13b, destacou-se. Ele matou células de câncer de osso e cervical em concentrações muito baixas, mas não mostrou toxicidade detectável em fibroblastos normais mesmo em doses mais de 60 vezes maiores. Vários outros compostos foram moderadamente potentes, porém menos seletivos, ressaltando como pequenas mudanças estruturais — como adicionar um átomo de cloro ou um grupo nitro em posições específicas — podem inclinar a balança entre toxicidade ampla e ação dirigida ao câncer.
Como o composto líder faz as células cancerosas se autodestruírem
Para entender o que 13b realmente faz dentro das células, os pesquisadores buscaram sinais característicos de morte celular programada, ou apoptose. Células cancerosas tratadas com 13b tornaram-se positivas para Annexina V e ativaram as enzimas caspase-3 e -7, marcadores clássicos de que a célula foi levada a um programa ordenado de suicídio, e não simplesmente a um rompimento. A microscopia revelou pontos brilhantes de γH2AX, um sinal de fraturas nas fitas de DNA, nos núcleos das células tratadas. Com o tempo, o arcabouço interno das células começou a se reorganizar e se degradar, especialmente em células de câncer cervical, que arredondaram e se desanexaram — pistas visuais de que a apoptose estava em curso. Em conjunto, esses achados mostram que 13b danifica o DNA das células cancerosas e então as conduz por uma via de morte controlada.
De camadas celulares planas a mini-tumores 3D
A maioria dos testes laboratoriais cultiva células cancerosas em camadas finas, que não imitam completamente a estrutura densa e por camadas dos tumores reais. Para resolver isso, a equipe cultivou as células cancerosas em esferoides tridimensionais — pequenos aglomerados esféricos que se assemelham melhor à arquitetura de um tumor e aos desafios de penetração de fármaco. Quando esses esferoides foram tratados com 13b, eles encolheram de forma dependente da dose. Os esferoides de câncer ósseo foram especialmente sensíveis, tornando-se pequenos, frouxos e fragmentados em níveis mais altos do fármaco. Colorantes fluorescentes mostraram ondas de apoptose movendo-se da periferia do esferoide para o interior à medida que a concentração aumentava, comprovando que 13b consegue penetrar e matar células por toda essa estrutura compacta. 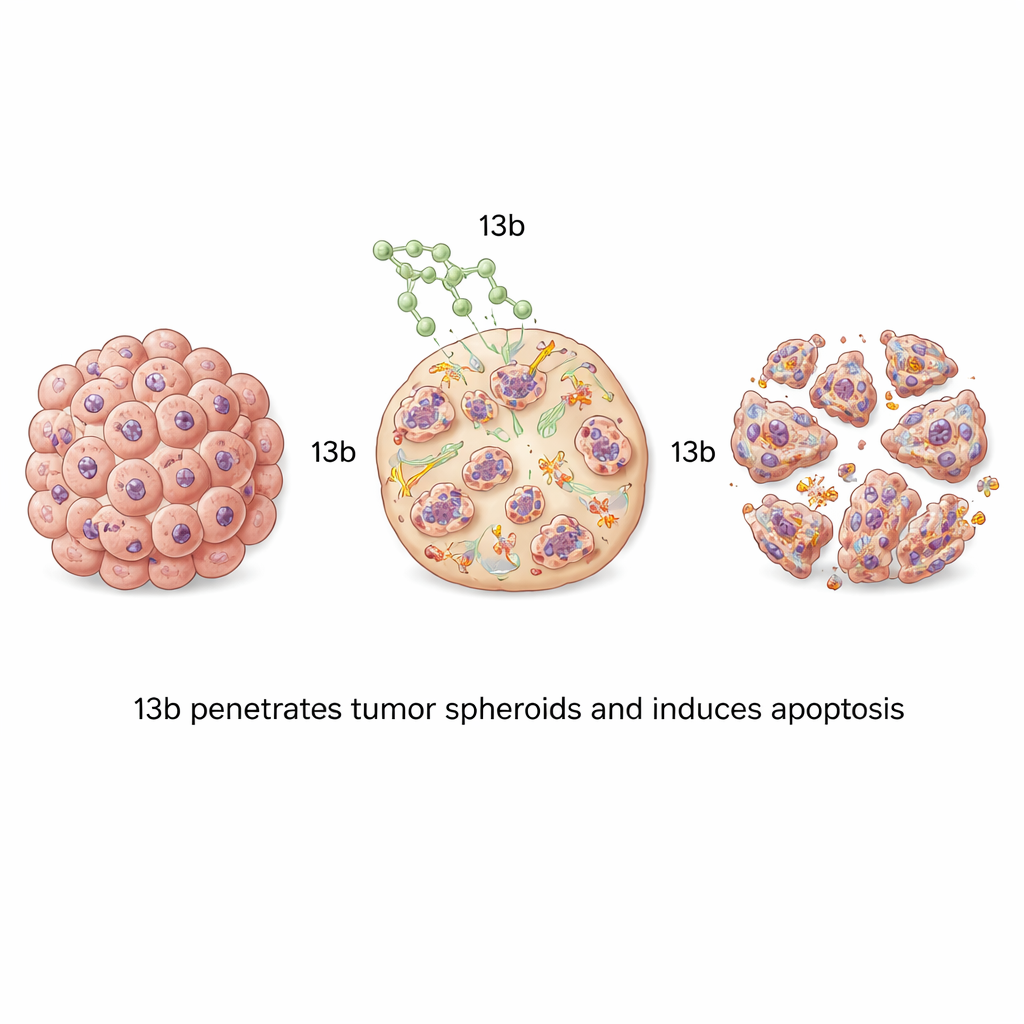
Por que este trabalho importa para tratamentos futuros do câncer
Para um público não especializado, a mensagem principal é que os pesquisadores criaram uma nova classe de pequenas moléculas que combinam as melhores características de dois componentes de fármacos já comprovados em um desenho híbrido. Seu composto líder, 13b, é capaz de reconhecer e destruir células cancerosas de forma eficiente enquanto poupa, em grande medida, as células saudáveis em testes laboratoriais, e permanece eficaz mesmo em modelos tumorais 3D mais realistas. Embora ainda haja muito trabalho a fazer — como identificar seus alvos moleculares exatos, melhorar sua solubilidade e testá-lo em animais — este estudo mostra que mesclar as estruturas tioimidazol e TMP é uma estratégia promissora para desenvolver agentes anticâncer mais seletivos e potentes.
Citação: Maciejewska, N., Grybaitė, B., Anusevičius, K. et al. Synthesis and anticancer evaluation of novel thioimidazole derivatives bearing a trimethoxyphenyl moiety. Sci Rep 16, 6271 (2026). https://doi.org/10.1038/s41598-026-36890-8
Palavras-chave: agentes anticâncer, derivados de imidazol, trimetoxifenil, apoptose, esfenoides tumorais 3D