Clear Sky Science · pt
YTHDC1 modula o fenótipo maligno do retinoblastoma via autofagia mediada por SQSTM1
Por que isso importa para o câncer ocular infantil
O retinoblastoma é o câncer ocular mais comum em crianças pequenas. Os médicos frequentemente conseguem curá-lo quando diagnosticado precocemente, mas, uma vez que o tumor começa a invadir os tecidos ao redor do olho ou a se espalhar rumo ao cérebro, salvar tanto a vida quanto a visão da criança torna-se muito mais difícil. Este estudo investiga um “freio” molecular dentro das células tumorais — duas moléculas chamadas YTHDC1 e SQSTM1 — que parecem ajudar a manter o retinoblastoma menos agressivo. Entender como esse freio funciona pode abrir novos caminhos para tratamentos mais direcionados e menos agressivos.
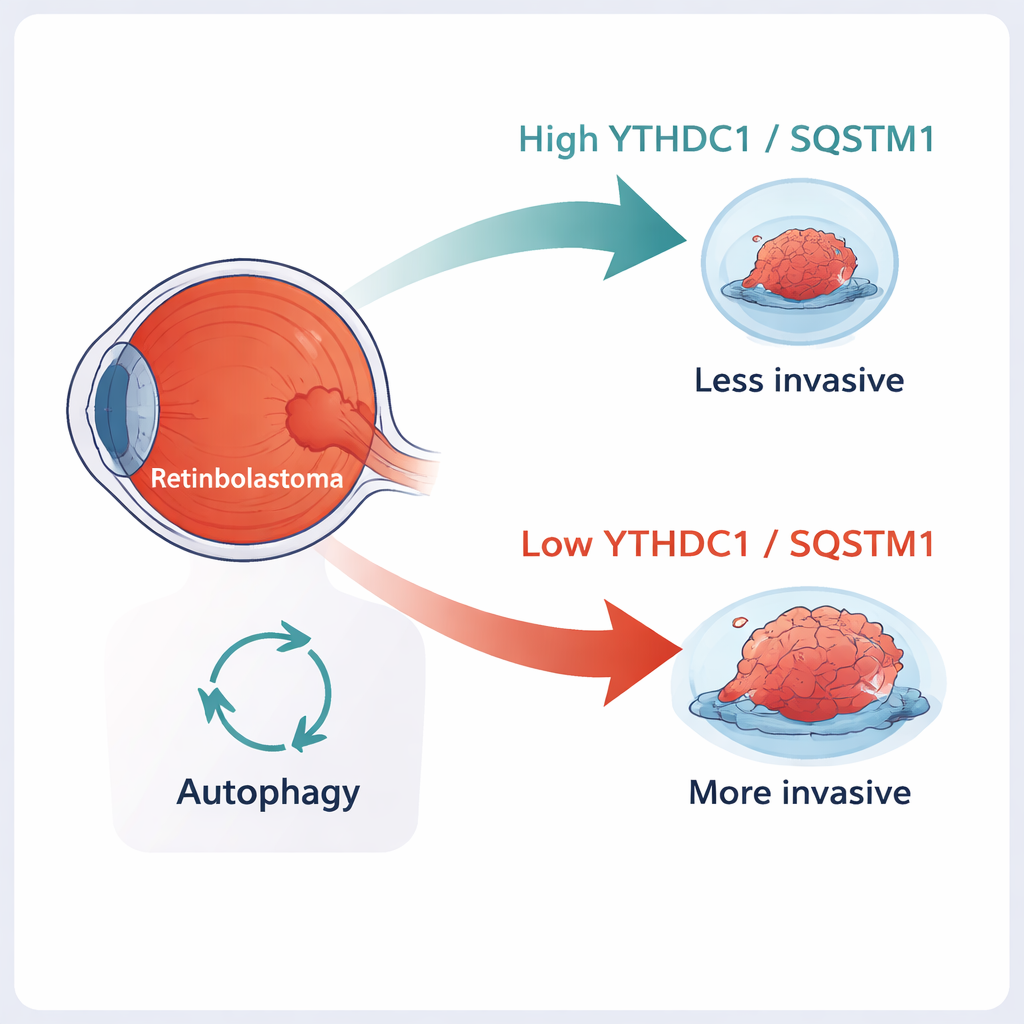
Um olhar mais atento sobre tumores oculares infantis
O retinoblastoma surge da camada sensível à luz do olho, a retina, geralmente em crianças com menos de cinco anos. Classicamente, a doença começa quando ambas as cópias de um gene guardião, RB1, são perdidas. Mas a perda de RB1 por si só não explica completamente por que alguns tumores permanecem confinados ao olho enquanto outros penetram nos tecidos vizinhos ou se espalham ao longo do nervo óptico. Cada vez mais, os pesquisadores têm percebido que marcas químicas colocadas no RNA — as mensagens temporárias que dizem às células quais proteínas produzir — podem influenciar fortemente o comportamento dos cânceres. Uma das marcas mais comuns, chamada m6A, pode alterar a estabilidade dessas mensagens e quanto tempo elas persistem dentro da célula.
Descobrindo um freio molecular em falta
Os autores começaram comparando a atividade genética em tumores que permaneceram dentro do olho com aqueles que já haviam se tornado invasivos. Usando um conjunto de dados público de sequenciamento de RNA de amostras de retinoblastoma, identificaram milhares de genes cuja atividade diferia entre os dois grupos e então se concentraram em importantes “reguladores” do m6A. Isso inclui enzimas que adicionam ou removem m6A e proteínas “leitoras” que interpretam a marca. Entre dez reguladores principais, encontraram que um leitor, YTHDC1, estava consistentemente mais baixo em tumores invasivos. Ao examinar amostras de 50 crianças e realizar testes laboratoriais em tecido tumoral, confirmaram que os níveis de YTHDC1 — tanto seu RNA quanto a proteína — estavam reduzidos nos cânceres mais agressivos.
Colocando YTHDC1 à prova
Para ver o que YTHDC1 realmente faz, a equipe manipulou seus níveis em duas linhagens humanas de células de retinoblastoma. Quando reduziram YTHDC1 usando ferramentas genéticas, as células se multiplicaram mais rapidamente e foram melhores em atravessar membranas artificiais que imitam barreiras teciduais — sinais de um tumor mais invasivo. Em camundongos, células sem YTHDC1 formaram tumores maiores e mais pesados. O contrário também foi observado: forçar as células a produzir YTHDC1 extra retardou seu crescimento e reduziu sua capacidade de migrar e invadir. Esses experimentos sugerem que YTHDC1 age como um supressor tumoral, ajudando a conter os comportamentos mais perigosos do retinoblastoma.
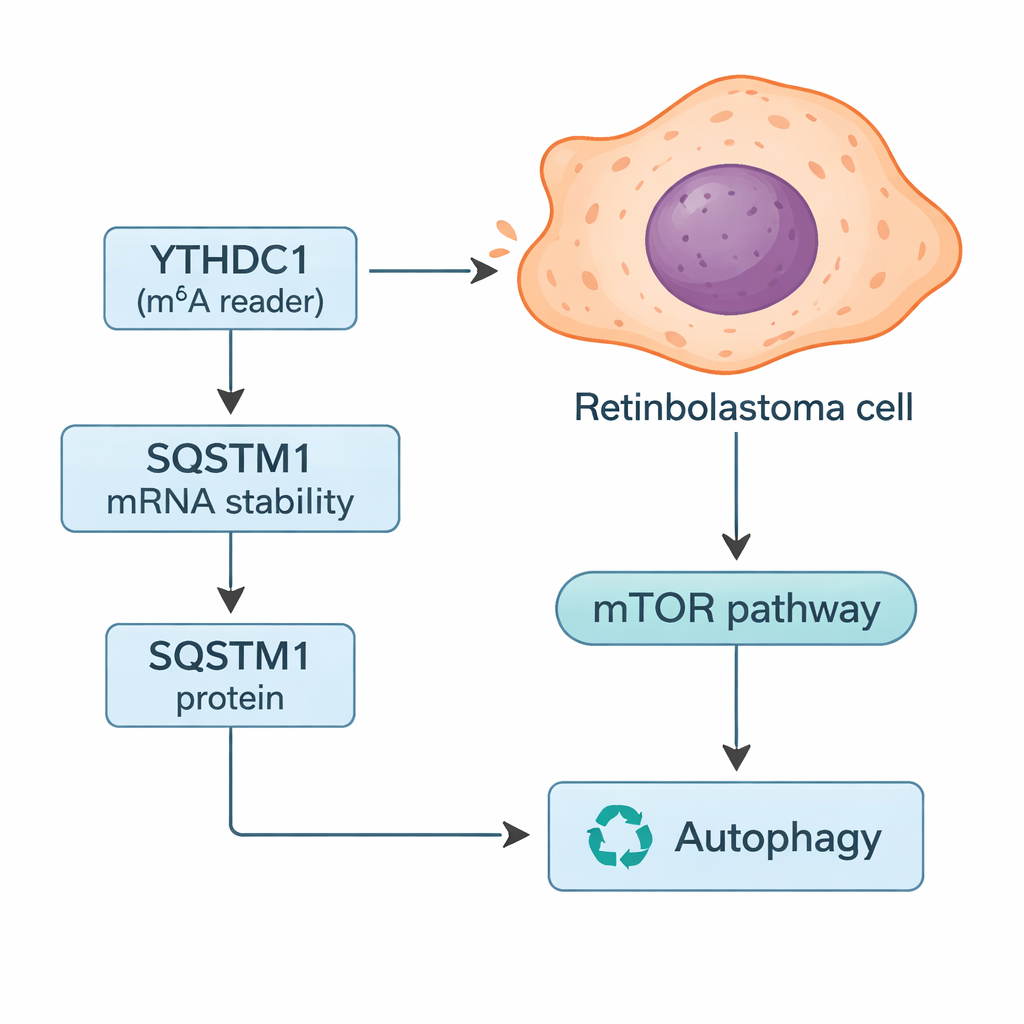
Como YTHDC1 controla o sistema de reciclagem da célula
Ao aprofundar, os pesquisadores buscaram genes específicos cujas mensagens pudessem ser controladas por YTHDC1. Ao combinar buscas em bancos de dados com seus dados tumorais, concentraram-se em SQSTM1, uma proteína mais conhecida como p62. SQSTM1 ajuda a gerenciar a autofagia, o sistema de reciclagem celular que degrada componentes danificados e pode fornecer combustível quando os recursos são escassos. O estudo mostrou que YTHDC1 se liga fisicamente ao RNA de SQSTM1 e o estabiliza, permitindo que mais proteína SQSTM1 seja produzida. Quando YTHDC1 foi reduzido, os níveis de SQSTM1 caíram e seu RNA decaiu mais rapidamente. Silenciar SQSTM1 isoladamente fez com que as células de retinoblastoma crescessem e invadissem mais, e apagou parcialmente os efeitos protetores observados quando YTHDC1 era superexpresso, posicionando SQSTM1 como um intermediário-chave nessa via.
Autofagia, energia e agressividade tumoral
Como SQSTM1 é central para a autofagia, a equipe testou como alterar YTHDC1 e SQSTM1 afetava esse processo de reciclagem. Usando uma combinação de marcadores fluorescentes e medidas de proteínas, descobriram que reduzir tanto YTHDC1 quanto SQSTM1 aumentou o “fluxo” autofágico — mais material celular estava sendo direcionado para e através do sistema de reciclagem. Também observaram mudanças na via mTOR, um importante controlador sensível a nutrientes que normalmente mantém a autofagia sob controle. Com menos SQSTM1, a atividade de mTOR diminuiu, consistente com a ativação da autofagia. No retinoblastoma invasivo, os autores propõem que a redução de YTHDC1 leva a sinais mais fracos de SQSTM1, atenua a atividade de mTOR e aumenta a autofagia, o que ajuda as células tumorais a sobreviver ao estresse e a se espalhar.
O que isso significa para tratamentos futuros
Para um público não especializado, a mensagem principal é que este estudo identifica uma cadeia de eventos dentro das células de retinoblastoma — YTHDC1 controlando SQSTM1, que por sua vez molda a maquinaria de reciclagem celular — que influencia o quão agressivo o câncer se torna. Quando essa cadeia é enfraquecida, os tumores crescem mais rápido e invadem mais. Embora ainda reste muito trabalho antes que essas descobertas possam alcançar a clínica, a via oferece novas ideias para terapia: restaurar a função de YTHDC1, estabilizar SQSTM1 ou ajustar a autofagia e a atividade de mTOR pode um dia complementar as quimioterapias existentes. Para crianças afetadas por esse câncer ocular, estratégias direcionadas assim poderiam ajudar a limitar a disseminação tumoral, preservando mais visão e reduzindo efeitos colaterais do tratamento.
Citação: Ding, J., Sun, J., Wang, J. et al. YTHDC1 modulates the malignant phenotype of retinoblastoma via SQSTM1-mediated autophagy. Sci Rep 16, 6292 (2026). https://doi.org/10.1038/s41598-026-36833-3
Palavras-chave: retinoblastoma, YTHDC1, SQSTM1, autofagia, via mTOR