Clear Sky Science · pt
Sistema de defesa contra fagos do tipo RexAB codificado por profagos em Pseudomonas putida
Seguranças ocultos vivendo dentro das bactérias
Bactérias são constantemente caçadas por vírus chamados fagos, que podem dizimar populações microbianas inteiras. Este estudo investiga como vírus “adormecidos” já escondidos no DNA de uma bactéria podem agir secretamente como seguranças, sacrificando células infectadas para salvar o restante. Entender essas estratégias naturais de defesa é importante para terapias com fagos, biotecnologia e também para manter microrganismos industriais funcionando de forma confiável.
Vírus que mudam de inimigos para aliados
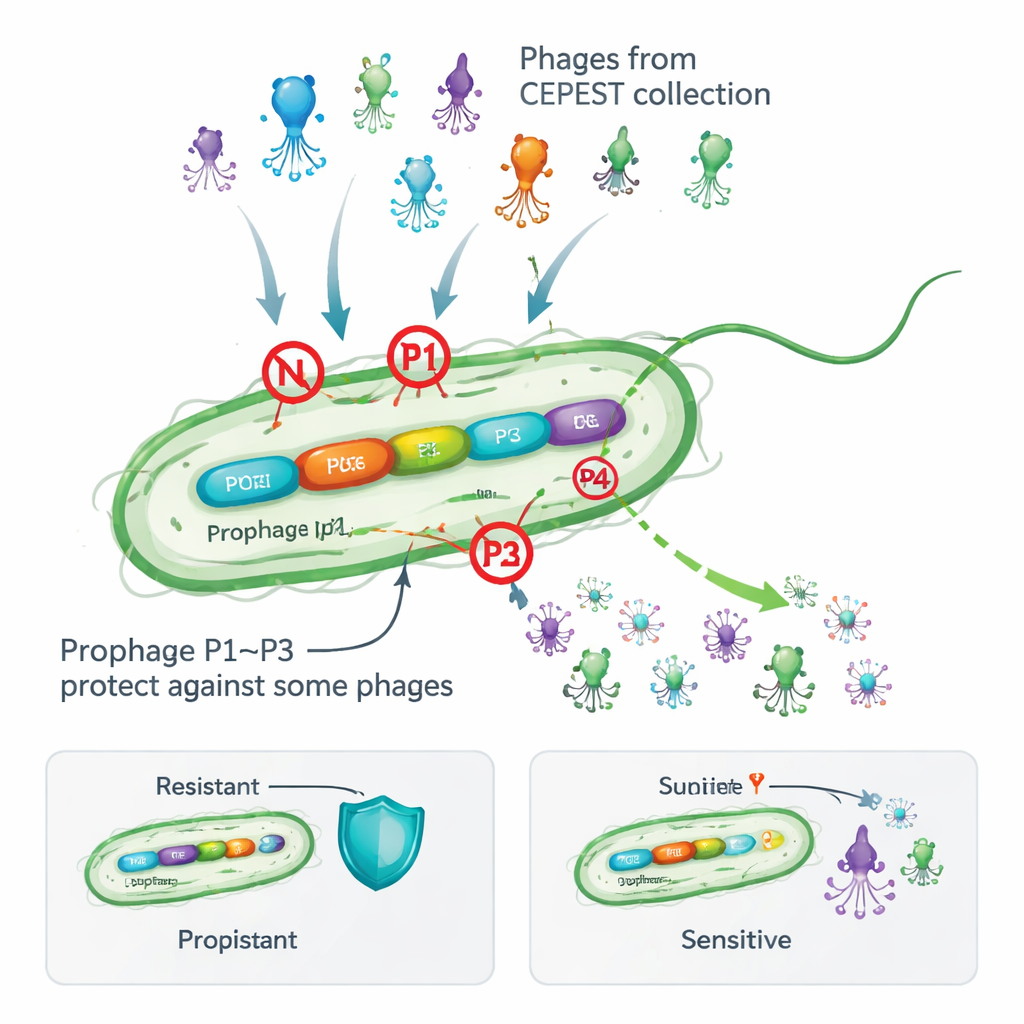
Muitas bactérias carregam fagos temperados em uma forma dormente chamada profago, integrados em seus cromossomos. À primeira vista isso parece arriscado: esses passageiros virais podem despertar e danificar a célula hospedeira, além de tornar o genoma mais volumoso. Ainda assim, levantamentos de milhares de genomas bacterianos mostram que a maioria das espécies mantém tais profagos, o que sugere que eles oferecem vantagens. Trabalhos anteriores com a bactéria do solo Pseudomonas putida mostraram que remover seus quatro profagos crípticos (não‑produtivos) tornou as células mais vulneráveis ao ataque por uma coleção experimental de fagos chamada CEPEST. Isso indicou que os profagos carregavam armas anti‑fago, mas os genes e mecanismos exatos eram desconhecidos.
Três vírus residentes conferem proteção direcionada
Os autores analisaram a contribuição de cada profago deletando‑os um a um e testando quão bem 26 fagos diferentes do CEPEST conseguiam formar placas em monocamadas bacterianas. Descobriram que os profagos chamados P1, P2 e P3 oferecem proteção, mas apenas contra grupos particulares de fagos, enquanto P4 parece neutro. P1 sozinho pode reduzir a infecção por alguns fagos em cerca de mil vezes, P2 oferece proteção mais modesta e P3 é espetacularmente eficaz — mas somente contra certos fagos gigantes “jumbo”. Na maioria dos casos, um único profago explica o padrão de resistência observado, embora para alguns fagos múltiplos profagos pareçam cooperar. Esses resultados mostram que mesmo profagos “silenciosos” podem atuar como um escudo personalizado, ajustado a ameaças virais específicas.
Localizando um alarme molecular em duas partes
Focando na proteção forte e relativamente ampla fornecida por P1, a equipe deletou sistematicamente blocos de genes de P1 até que a defesa desaparecesse. Afinando a busca, descobriram que perder apenas dois genes vizinhos, PP_5643 e PP_5644, tornava as células tão sensíveis quanto se todo o profago P1 tivesse sido removido. Ferramentas bioinformáticas revelaram que PP_5643 se assemelha a RexA, uma proteína de ligação ao DNA conhecida de estudos clássicos do fago lambda, enquanto PP_5644 parece uma proteína de membrana com várias hélices que poderia formar um poro, semelhante a RexB. Juntos, esse par corresponde a um tipo bem conhecido de sistema de “infecção abortiva”: uma vez detectado um fago específico, a célula infectada interrompe deliberadamente seu próprio crescimento para que o vírus não possa se multiplicar e se espalhar para os vizinhos.
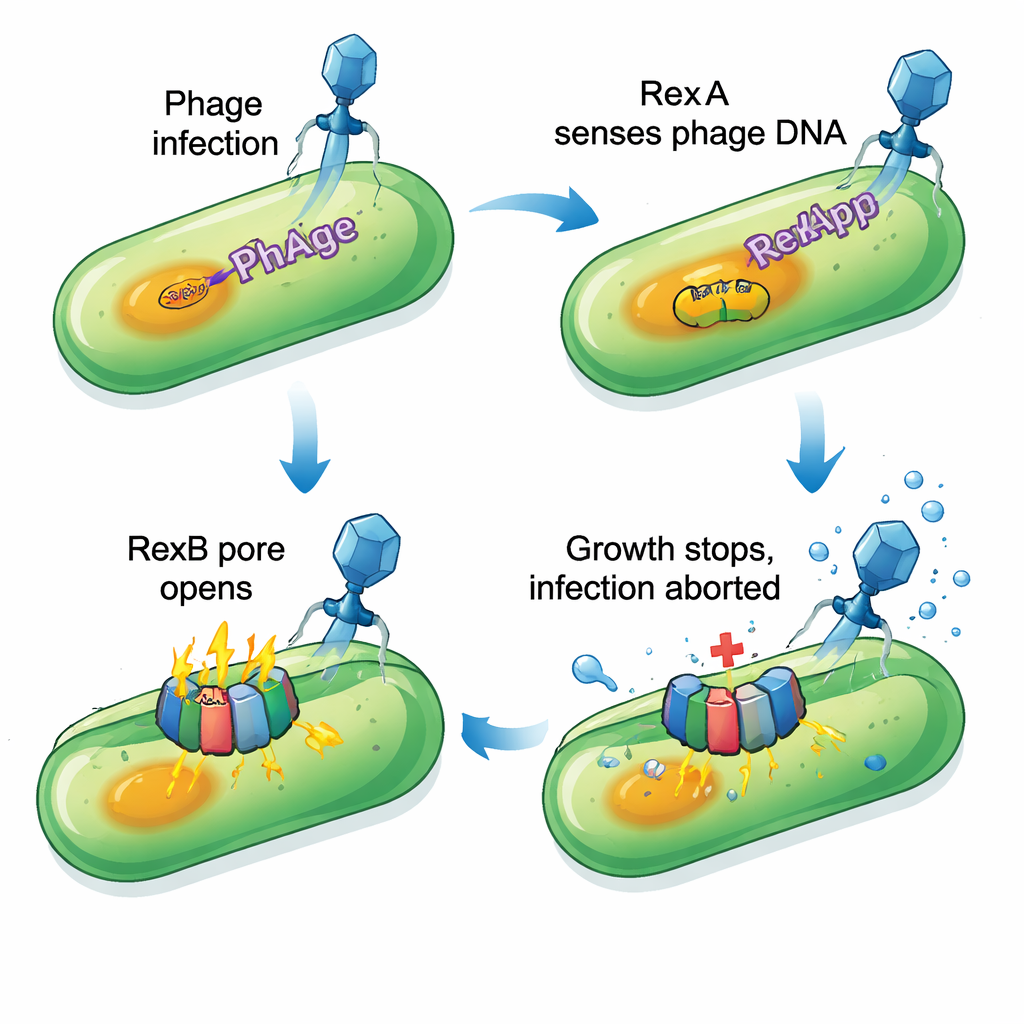
Como a defesa sabota células infectadas
Experimentos confirmaram que a versão P1 de RexA (chamada RexApp) liga‑se ao DNA sem grande preferência por sequência exata, o que a torna bem adequada para detectar estruturas de DNA incomuns geradas durante a replicação viral. A proteína parceira RexBpp se integra na membrana celular. Quando RexApp é produzida artificialmente em excesso, células que ainda carregam o gene rexBpp exibem forte parada de crescimento e sinais de dano na membrana: corantes que normalmente não atravessam membranas intactas passam a entrar e pequenas quantidades de uma enzima citoplasmática vazam. Se rexBpp está ausente ou mutado, a superprodução de RexApp deixa de prejudicar as células. Isso indica que RexApp atua como gatilho, enquanto RexBpp é o efetor que danifica o envoltório celular. Curiosamente, a maioria das células afetadas não se rompe completamente; em vez disso, entram em um estado profundamente lento, quase estacionário, que parece incompatível com a multiplicação do fago.
Por que sacrificar algumas células pode salvar a população
O quadro que emerge é o de uma defesa altruísta: quando um fago sensível infecta P. putida, RexApp provavelmente detecta complexos DNA‑proteína virais e liga RexBpp, que compromete a membrana e interrompe abruptamente o crescimento. A célula infectada paga um preço, mas o ciclo de vida do fago é abortado e a comunidade bacteriana mais ampla é protegida. Sistemas do tipo RexAB foram encontrados até agora em apenas um punhado de fagos diferentes, mas compartilham a mesma lógica central — um sensor intracelular ligado a um efetor de membrana que pode rapidamente transformar uma célula produtiva em um beco sem saída para o vírus. Para as bactérias, manter profagos crípticos que carregam tais módulos de defesa pode compensar os custos de abrigar DNA viral, ajudando‑as a sobreviver em um mundo onde os fagos estão por toda parte.
Citação: Rosendahl, S., Kängsep, A., Ainelo, A. et al. Prophage-encoded RexAB-type phage defense system in Pseudomonas putida. Sci Rep 16, 5898 (2026). https://doi.org/10.1038/s41598-026-36734-5
Palavras-chave: defesa contra bacteriófagos, profago, Pseudomonas putida, infecção abortiva, sistema RexAB