Clear Sky Science · pt
Caracterização bioinformática e detecção automatizada de subpopulações de monócitos metabolicamente ativadas na dislipidemia
Por que células imunes ocultas importam para a saúde do coração
Problemas com colesterol costumam ser discutidos em termos de dieta, números em exames de sangue e risco de ataque cardíaco. Mas por trás desses indicadores, nosso sistema imunológico está mudando discretamente. Este estudo examina um grupo especial de glóbulos brancos no sangue de adultos jovens com LDL (“ruim”) alto. Essas células parecem tornar‑se “metabolicamente ativadas” e guardar memória de exposições anteriores a excesso de lipídios, potencialmente aumentando a inflamação das artérias — e o risco futuro de doença cardíaca. Entender esses tipos celulares ocultos pode ajudar médicos a detectar problemas mais cedo e a desenhar tratamentos mais precisos.
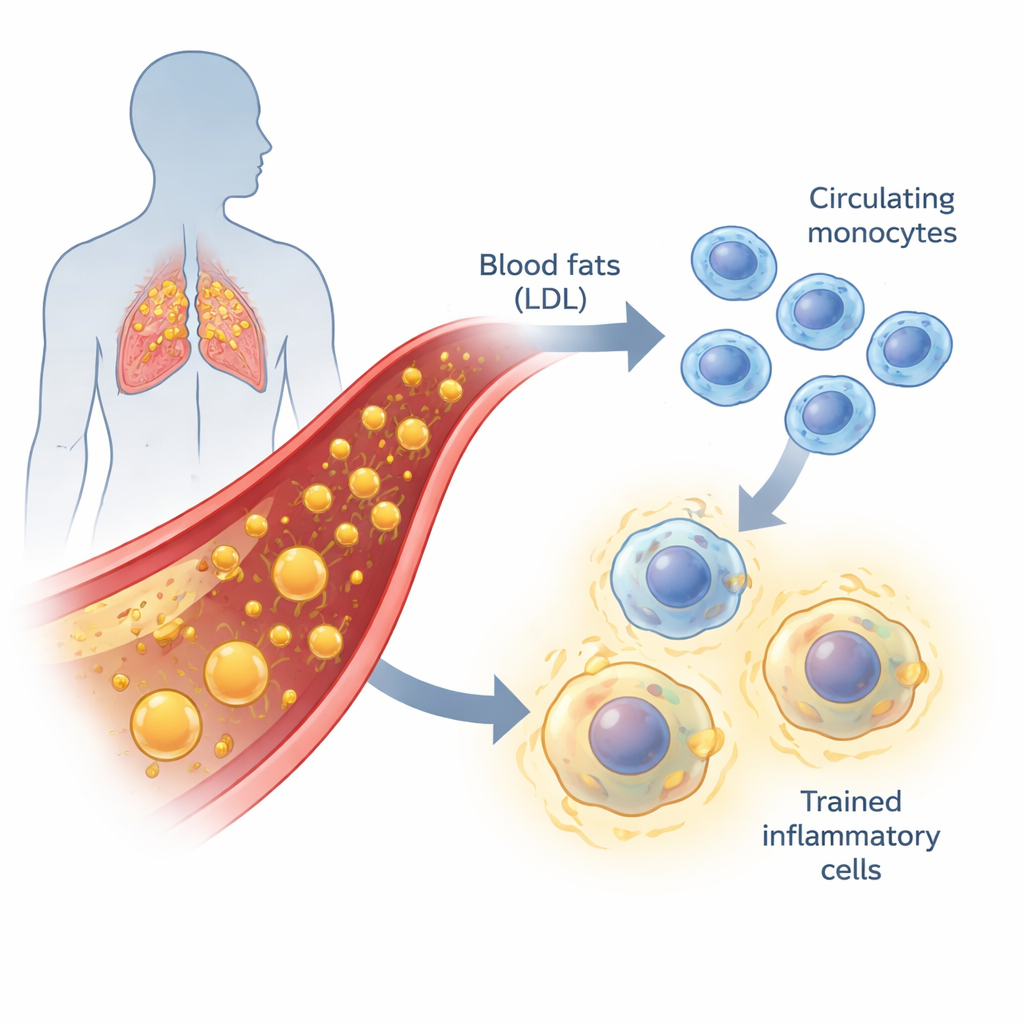
Lipídios no sangue e inflamação de baixo grau
A aterosclerose, o processo que leva ao entupimento das artérias, não é só gordura grudando nas paredes vasculares. É também uma doença inflamatória crônica e de curso lento. Quando o colesterol LDL está alto, especialmente em formas oxidadas, ele irrita o revestimento dos vasos. Monócitos — glóbulos brancos circulantes — e os macrófagos em que se transformam são recrutados para essas áreas e começam a engolir lipídios. Se esse processo de limpeza está mal regulado, as células viram “células espumosas” e contribuem para a formação de placas gordurosas. Tradicionalmente, os cientistas dividem monócitos sanguíneos em três grupos com base em marcadores de superfície, cada um com papéis diferentes em patrulhar vasos, desencadear inflamação ou manter a saúde tecidual.
Além dos rótulos simples: descobrindo novos tipos de monócitos
Os autores levantaram a hipótese de que alguns monócitos circulantes em pessoas com dislipidemia já poderiam estar reprogramados para um estado metabolicamente ativo, prontos para se tornar macrófagos prejudiciais. Para investigar, coletaram sangue de 23 adultos jovens com LDL alto e 17 participantes saudáveis com perfis lipídicos normais. Nenhum fazia uso de drogas redutoras de colesterol nem tinha outras doenças maiores, o que ajudou a isolar o efeito da dislipidemia. Usando citometria de fluxo, eles mediram não apenas marcadores clássicos de superfície, mas também proteínas envolvidas no manejo de lipídios e marcas químicas em histonas — pequenos carretéis proteicos que ajudam a controlar quais genes estão ativos em cada célula.
Algoritmos inteligentes para ler paisagens imunes complexas
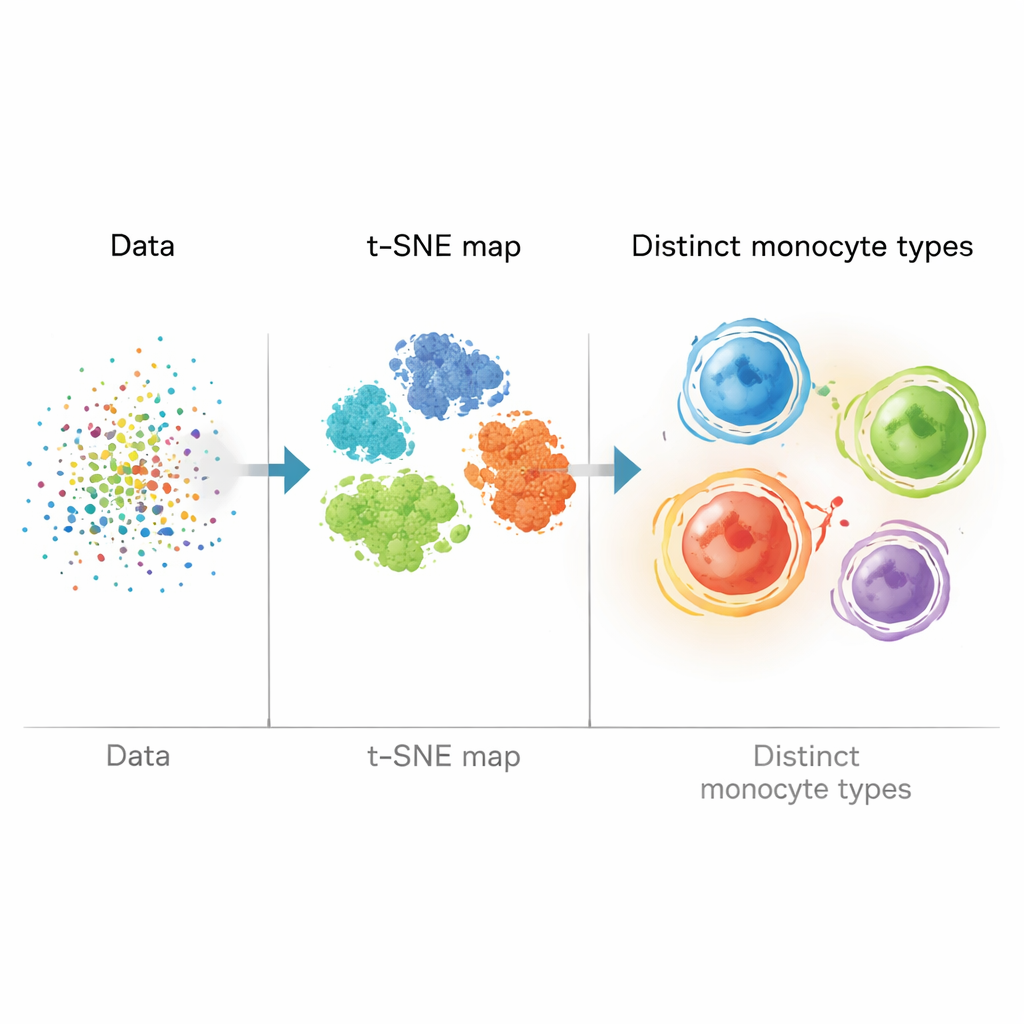
Em vez de depender apenas de “gates” manuais (desenho de limites a olho em gráficos de dois marcadores), a equipe construiu um pipeline bioinformático que tratou cada célula como um ponto em um espaço de alta dimensão. Eles limparam e padronizaram os dados e então usaram t‑SNE, um método matemático que transforma muitas medições de marcadores em um mapa bidimensional onde células semelhantes se agrupam. Em seguida aplicaram algoritmos de clusterização (X‑shift e FlowSOM) para agrupar automaticamente células com padrões de marcadores similares. Isso lhes permitiu ir além dos três tipos clássicos de monócitos e identificar quatro populações monociárias principais definidas por combinações de proteínas de manejo de lipídios (ABCA1, PLIN2, CD36) e pelos marcadores habituais CD14 e CD16.
Uma população inflamatória preparada na dislipidemia
Destas quatro, duas populações monociárias se destacaram. Uma em particular — caracterizada por CD14 alto, ausência de CD16 e forte expressão de ABCA1 com PLIN2 e CD36 variáveis — correspondeu ao perfil de monócitos “metabolicamente ativados” (MoMe). Em pessoas com dislipidemia, essa população MoMe e outro grupo relacionado foram significativamente mais abundantes do que em controles saudáveis. Ao examinar marcas epigenéticas — especificamente H3K4me3 e H3K27me3, que são marcas químicas em histonas associadas à atividade gênica — os pesquisadores encontraram níveis mais altos de H3K4me3 nas células MoMe de indivíduos dislipidêmicos. Essa marca está associada a genes que promovem inflamação, sugerindo que essas células têm uma forma de “memória” inata, ou imunidade treinada, após exposições repetidas ao LDL alto.
De células circulantes a macrófagos formadores de placa
Para entender o que esses monócitos podem se tornar nos tecidos, a equipe cultivou monócitos purificados em condições laboratoriais que mimetizam a síndrome metabólica, incentivando sua diferenciação em macrófagos. Novamente usaram análise avançada para identificar subgrupos de macrófagos e mediram suas marcas epigenéticas. Curiosamente, macrófagos derivados de doadores saudáveis muitas vezes exibiram níveis mais altos de marcas histônicas ativadoras do que aqueles provenientes de pacientes dislipidêmicos, sugerindo que o treinamento inflamatório pode se manifestar de forma diferente após a saída da corrente sanguínea. Embora o tamanho da amostra fosse modesto, os achados sustentam a ideia de que a exposição prolongada a lipídios sanguíneos em excesso remodela monócitos tanto no nível proteico quanto epigenético, predispondo‑os a respostas inflamatórias mais intensas.
O que isso significa para pacientes e cuidados futuros
Para leigos, a conclusão é que LDL alto não é apenas um problema de “excesso de gordura”, mas também de células imunes “reconfiguradas”. Este estudo mostra que, mesmo em adultos jovens, a dislipidemia está associada a uma população distinta de monócitos que parecem metabolicamente carregados e epigeneticamente preparados para alimentar a inflamação arterial. Ao combinar ferramentas computacionais poderosas com medições celulares detalhadas, os pesquisadores agora podem identificar esses tipos celulares de risco no sangue, muito antes de um ataque cardíaco ocorrer. No futuro, tais abordagens podem ajudar médicos a avaliar melhor o risco cardiovascular, monitorar se tratamentos estão revertendo o treinamento imune prejudicial e, em última instância, desenvolver terapias que atuem não só nos níveis de colesterol, mas também nas células imunes que respondem a eles.
Citação: Ramírez-Torres, R., Ramírez-Segovia, S.G., González-Huerta, M.J. et al. Bioinformatic characterization and automated detection of metabolically activated monocyte subpopulations in dyslipidemia. Sci Rep 16, 6170 (2026). https://doi.org/10.1038/s41598-026-36678-w
Palavras-chave: dislipidemia, monócitos, imunidade treinada, aterosclerose, citometria de fluxo