Clear Sky Science · pt
Diagnóstico da doença de Alzheimer com alta precisão por meio de modelagem de redes de Petri de vias de sinalização
Por que a detecção precoce de doenças cerebrais importa para todos nós
A doença de Alzheimer corrói lentamente a memória e a independência, muitas vezes bem antes de surgirem sintomas evidentes. As ferramentas diagnósticas atuais, como exames cerebrais e testes cognitivos, podem ser caras, de difícil acesso e pouco sensíveis nos estágios iniciais. Este estudo apresenta uma nova forma de ler a “fiação” molecular do corpo usando amostras de sangue ou cérebro e uma estrutura matemática chamada rede de Petri. O objetivo é simples, porém profundo: dizer, com altíssima precisão, se o padrão de atividade gênica de alguém se parece mais com o de uma pessoa saudável ou com o de uma pessoa com Alzheimer — idealmente cedo o suficiente para alterar o curso da doença.
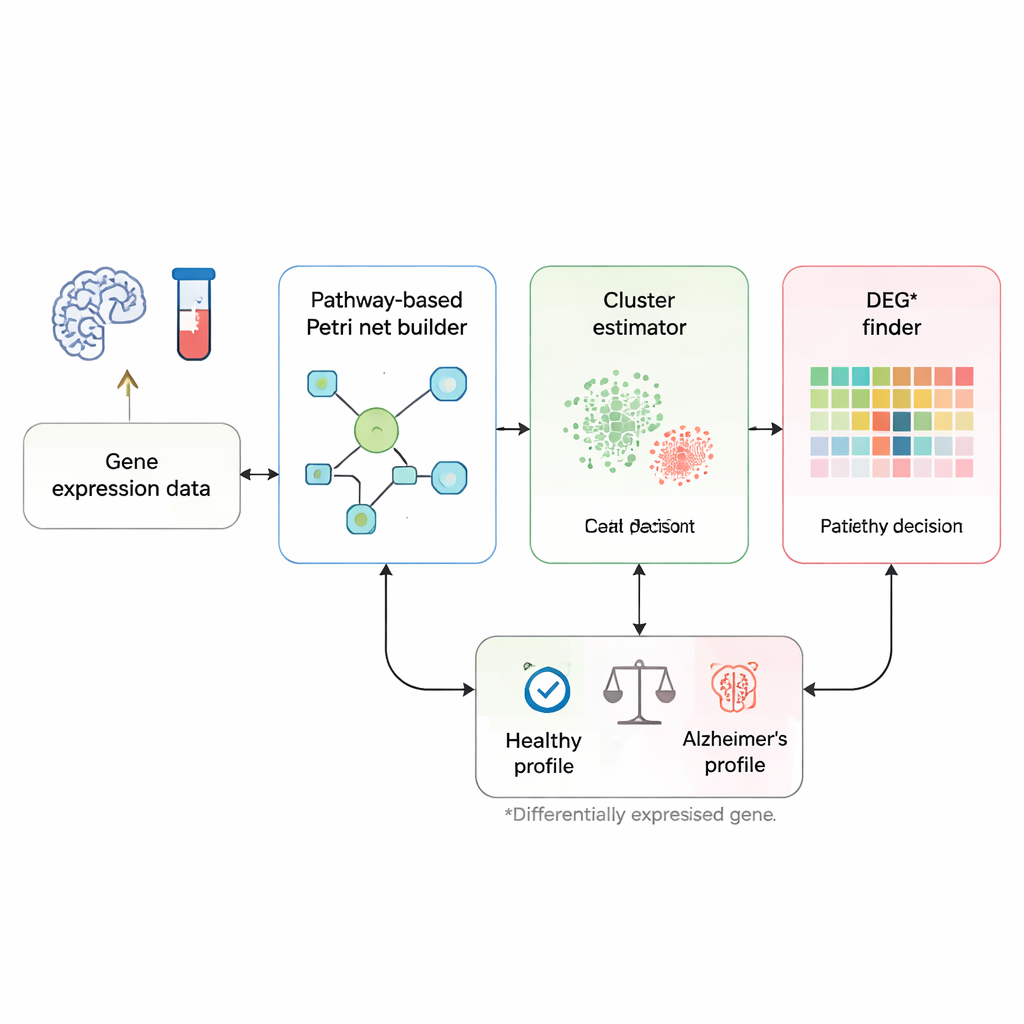
Lendo a doença nos “circuitos” de sinalização do corpo
Em vez de tratar cada gene como um marcador isolado, os pesquisadores focam em como os genes se comunicam ao longo de vias biológicas conhecidas associadas à doença de Alzheimer. Eles partem de um mapa de vias curado do banco de dados KEGG, que lista genes e as relações de ativação ou bloqueio entre eles. Essa via é transformada em uma rede de Petri — um tipo de diagrama de fluxo onde círculos representam genes, retângulos representam interações e pequenos tokens representam sinais que se movem pela rede. Quando um token viaja de uma extremidade da via até nós especiais de “doença”, isso representa uma cadeia de eventos gênicos que pode levar à morte de células cerebrais e à demência.
Da amostra de sangue a uma resposta sim-ou-não
O método começa com perfis de expressão gênica: medições que indicam quão ativos estão milhares de genes no sangue ou tecido cerebral de uma pessoa. Primeiro, um “estimador de cluster” personalizado compara uma nova amostra com amostras rotuladas previamente como saudáveis ou doentes, focando em genes já conhecidos por diferir entre esses grupos. Para cada gene desse conjunto, a ferramenta verifica quais amostras de treinamento têm níveis de expressão mais semelhantes e usa uma espécie de votação por vizinhança para dar à nova amostra um rótulo inicial como provável saudável ou provável doente. Essa etapa forma dois grupos de trabalho, ou clusters, de amostras: um que representa padrões típicos de saúde e outro que representa padrões típicos de Alzheimer.
Encontrando os genes mais informativos para cada pessoa
Em seguida vem uma etapa mais personalizada. Para um indivíduo dado, o método analisa gene a gene para ver onde seus níveis de expressão realmente se destacam. Para cada gene, compara-se o valor da pessoa com a faixa observada tanto no cluster saudável quanto no cluster de pacientes, usando estatísticas robustas que minimizam a influência de outliers ruidosos. Se a expressão de um gene estiver claramente dentro da faixa “doente” e fora da faixa saudável, ele é marcado como DEG* — um gene particularmente informativo para aquele indivíduo. Esses genes DEG* recebem tokens iniciais na rede de Petri, marcando onde a atividade anômala aparece pela primeira vez no circuito de sinalização.
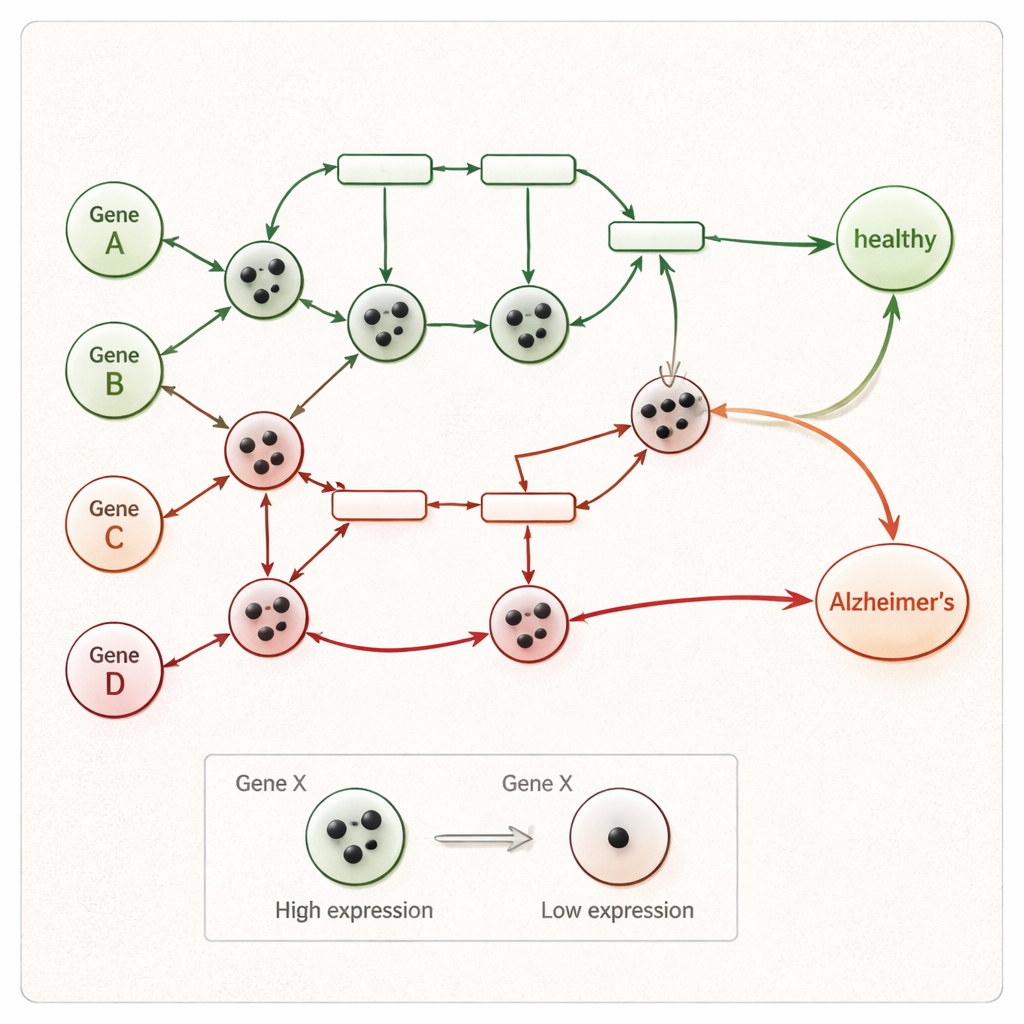
Deixando a rede rodar até um diagnóstico
Uma vez colocados os tokens, a rede de Petri é executada passo a passo. A cada passo, toda interação cujos genes de entrada tenham tokens suficientes “dispara”, movendo tokens para genes a jusante enquanto respeita regras de ativação e inibição. Isso continua até que nenhum movimento adicional seja possível. Se, ao final, pelo menos um token alcançar o nó final de doença da rede — representando processos como morte neuronal ou neurodegeneração — a amostra é classificada como Alzheimer; caso contrário, é rotulada como saudável. Como cada passo de disparo é registrado, os pesquisadores podem traçar um caminho claro desde a atividade gênica incomum de uma pessoa até um desfecho saudável ou doente, em vez de depender de um escore estatístico opaco.
Quão preciso é esse método na prática?
A equipe testou sua estrutura em diversos grandes conjuntos de dados públicos de expressão gênica, tanto de sangue quanto de tecido cerebral. Em dois conjuntos de dados sanguíneo amplamente usados, o método distinguiu corretamente pacientes com Alzheimer de indivíduos saudáveis em cerca de 98–99% dos casos, superando amplamente abordagens anteriores de aprendizado de máquina que frequentemente alcançavam apenas 65–81% de acurácia. Eles também mostraram desempenho robusto em outros conjuntos de dados de cérebro e sangue, mesmo quando o número de amostras era pequeno. Importante: ao contrário de muitos concorrentes, seu método não descartou amostras ruidosas ou de difícil interpretação; em vez disso, usa seu desenho interno para lidar com a variabilidade mantendo todos os dados na análise.
O que isso significa para futuros testes de Alzheimer
Para um leigo, a mensagem principal é que o estudo transforma genética complexa e diagramas de vias em um processo de decisão claro e passo a passo que pode ler sinais precoces da doença de Alzheimer a partir de uma amostra simples, potencialmente apenas do sangue. Ao modelar como genes anômalos trabalham em conjunto, e não apenas como se comportam isoladamente, a estrutura de redes de Petri fornece tanto alta precisão diagnóstica quanto uma “história” compreensível de como a doença pode se desenvolver em cada pessoa. Embora este trabalho ainda seja de pesquisa e não um teste clínico, aponta para ferramentas futuras que poderiam detectar Alzheimer mais cedo, orientar escolhas de tratamento e, eventualmente, ser adaptadas a outras doenças cerebrais e cânceres usando a mesma ideia subjacente.
Citação: Ebrahimian, H., Asadzadeh, F., Rahgozar, M. et al. Diagnosis of Alzheimer’s disease with high accuracy via Petri net modeling of signaling pathways. Sci Rep 16, 6457 (2026). https://doi.org/10.1038/s41598-026-36585-0
Palavras-chave: Diagnóstico de Alzheimer, expressão gênica, vias de sinalização, modelagem com redes de Petri, biomarcadores sanguíneos