Clear Sky Science · pt
Construção e validação inicial de uma rede gênica-chave para resistência à progesterona no câncer de endométrio com base em triagem CRISPR em todo o genoma
Por que alguns cânceres uterinos deixam de “ouvir” os hormônios
Para muitas pessoas com câncer de endométrio em estágio inicial que ainda desejam ter filhos, comprimidos hormonais que imitam a progesterona natural podem reduzir tumores preservando o útero. No entanto, até um terço desses cânceres nunca responde ou rapidamente desenvolve resistência, forçando pacientes a optarem por cirurgia ou tratamentos mais agressivos. Este estudo usa uma poderosa ferramenta de edição gênica para mapear quais genes fazem células do câncer de endométrio ignorarem a progesterona, apontando para exames e medicamentos futuros que poderiam manter essa terapia eficaz por mais tempo.
Usando tesouras gênicas para vasculhar o genoma inteiro
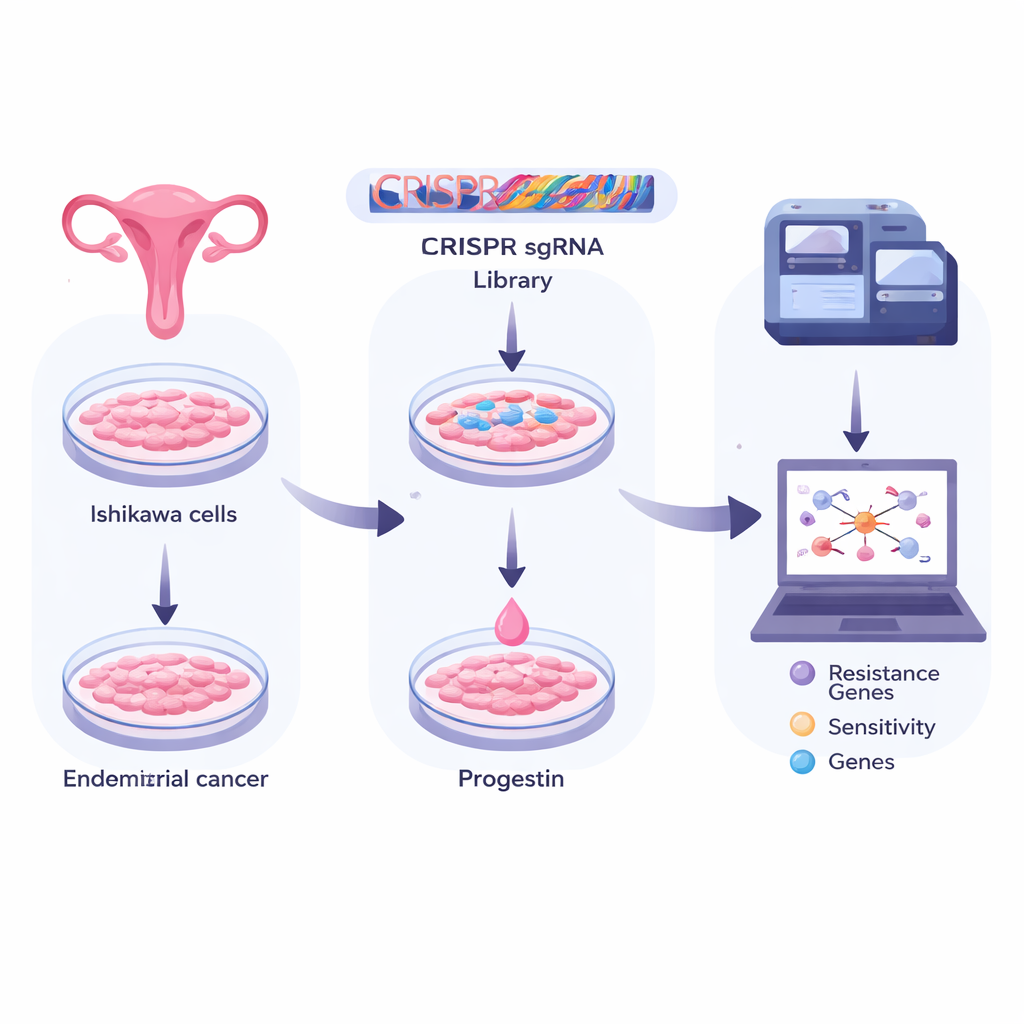
Os pesquisadores trabalharam com células Ishikawa, um modelo amplamente usado de câncer de endométrio. Eles infectaram milhões dessas células com uma biblioteca de “tesouras gênicas” CRISPR, cada uma programada para desligar um gene humano diferente. Isso criou um grande conjunto em que, em princípio, cada célula tinha um gene único desativado. A equipe então dividiu as células em grupos: um congelado como linha de base, um exposto apenas a um solvente inerte e outro tratado por muitos dias com uma progesterona sintética comum (medroxiprogesterona, ou MPA). Pelo sequenciamento profundo das marcas CRISPR que sobreviveram em cada grupo, foi possível ver quais nocautes gênicos ajudavam as células a sobreviver ou morrer sob o tratamento com progesterona.
Separando genes que ajudam ou atrapalham a resposta ao fármaco
Analisar esse volume de dados exigiu estatística sofisticada. A equipe aplicou dois métodos complementares, RRA e MLE, para classificar genes segundo o quanto protegiam as células da progesterona (genes de resistência) ou aumentavam a probabilidade de morte (genes de sensibilidade). Encontraram centenas de candidatos em cada direção. Muitos desses genes se agruparam em vias que lidam com a cópia e reparo do DNA, a produção e processamento de RNA e o metabolismo celular geral. Em outras palavras, a maquinaria básica que permite às células ler, manter e atuar sobre sua informação genética parece fortemente ligada a se as células do câncer de endométrio obedecem ao sinal de “parar de crescer” da progesterona.
Reduzindo a lista aos participantes mais importantes
Para evitar seguir pistas falsas, os cientistas cruzaram os acertos do CRISPR com um conjunto de dados anterior do próprio laboratório, no qual haviam comparado células cancerígenas comuns com uma linhagem tornada resistente à progesterona ao longo do tempo. Ao procurar genes que apareciam em ambas as triagens e mostravam mudanças consistentes, destilaram a lista para cinco genes que parecem promover resistência e vinte que parecem combatê‑la. Bancos públicos de dados de câncer mostraram que muitos genes que bloqueiam a resistência são mais ativos no tipo mais comum de câncer de endométrio, enquanto vários genes que promovem resistência se correlacionam com piores desfechos em pacientes, sugerindo que esses sinais importam em tumores reais, não apenas em culturas.
Testando genes-chave em células e em camundongos
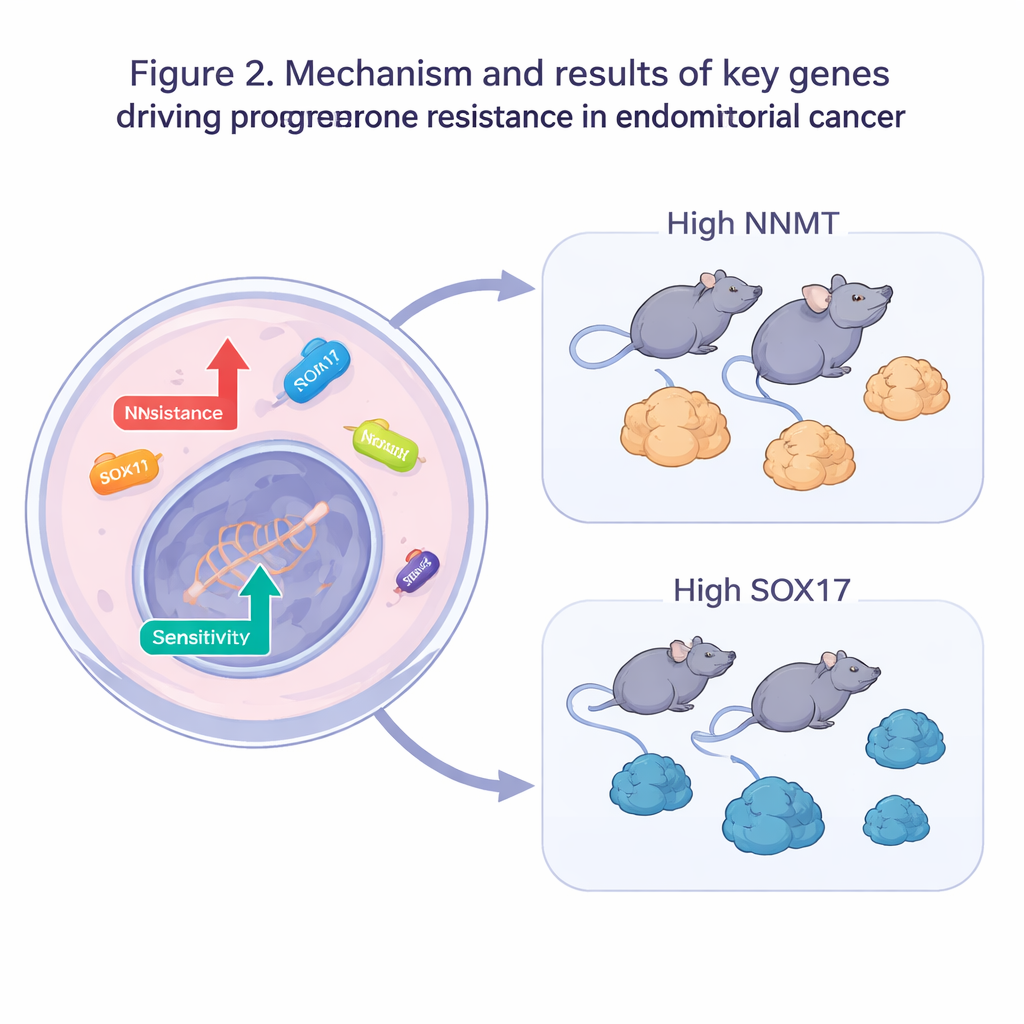
A equipe então passou de big data para experimentos práticos. Em células resistentes à progesterona, desligaram cada um dos cinco genes suspeitos de promover resistência ou aumentaram os cinco genes suspeitos de conferir sensibilidade. Quando essas células alteradas foram expostas à progesterona, muitas mais morreram e doses muito menores do fármaco foram necessárias para retardar o crescimento, confirmando que mexer em genes isolados pode restaurar a sensibilidade hormonal. Dois genes se destacaram: NNMT, envolvido no metabolismo celular, e SOX17, um gene que ajuda a controlar como as células se desenvolvem e se comportam. Em modelos de tumor em camundongos, aumentar a expressão de NNMT tornou os tumores menos responsivos à progesterona, enquanto elevar SOX17 fez tumores resistentes encolherem mais sob o mesmo tratamento.
O que essas descobertas podem significar para pacientes
Em termos simples, o estudo constrói um primeiro “diagrama de fiação” de como células do câncer de endométrio decidem se vão ou não obedecer à progesterona. Sugere que a resistência não é apenas perder o receptor de progesterona, mas também envolve mudanças mais profundas no manejo do DNA e do RNA e em genes de controle-chave como NNMT e SOX17. No futuro, exames de sangue ou de tecido que leiam essa rede gênica poderiam ajudar médicos a prever quem se beneficiará da terapia hormonal poupadora de fertilidade. Ainda mais promissor, medicamentos que reduzam genes de resistência ou aumentem genes de sensibilidade poderiam um dia ser combinados com progesterona para manter essa opção de tratamento mais suave eficaz para mais pessoas e por mais tempo.
Citação: Li, X., Wang, S., Qiu, Z. et al. Construction and initial validation of key gene network for progesterone resistance in endometrial cancer based on genome-wide CRISPR screening. Sci Rep 16, 8030 (2026). https://doi.org/10.1038/s41598-026-36534-x
Palavras-chave: câncer de endométrio, resistência à progesterona, triagem CRISPR, redes gênicas, terapia hormonal