Clear Sky Science · pt
Modificações m6A do hospedeiro moldam a microbiota que conduz à ferroptose específica de células como via causal para doenças respiratórias crônicas
Por que seus micróbios importam para seus pulmões
Problemas respiratórios crônicos, como asma e doença pulmonar obstrutiva crônica (DPOC), costumam ser atribuídos ao tabagismo, poluição ou alergias. Este estudo sugere um ator menos óbvio: os trilhões de micróbios que vivem em nosso intestino e na nossa pele. Usando dados genéticos em grande escala, os autores mostram que certos microrganismos podem não apenas acompanhar a doença pulmonar, mas também contribuir para causá‑la — atuando por meio de alterações químicas sutis em nossas células e de uma forma de dano celular dependente de ferro. Compreender essa rede oculta pode, no futuro, levar a novas formas de prevenir ou tratar doenças respiratórias crônicas, direcionando nossos micróbios e suas vias moleculares para estados mais saudáveis.
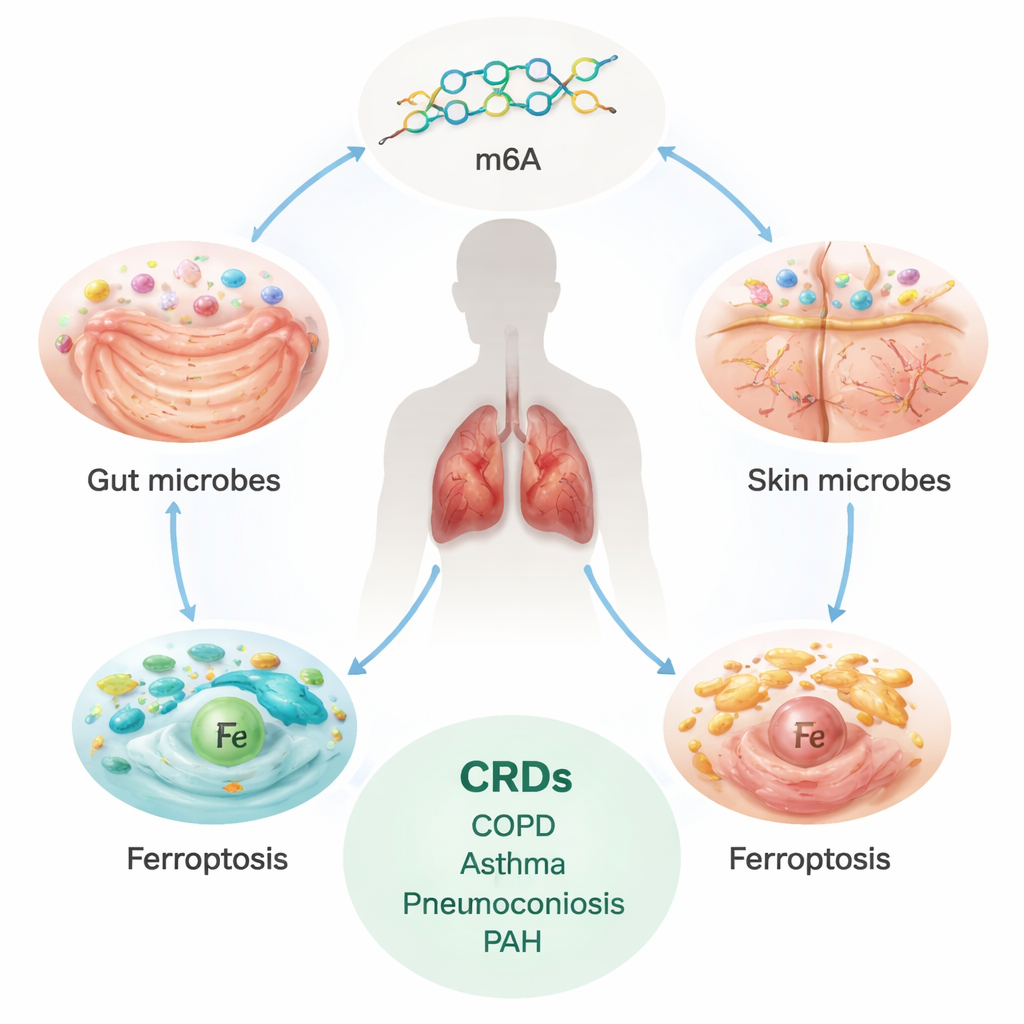
O fardo oculto das doenças pulmonares crônicas
Doenças respiratórias crônicas, incluindo DPOC, asma, doença pulmonar intersticial (DPI), pneumoconioses e hipertensão arterial pulmonar (HAP), afetam centenas de milhões de pessoas no mundo e causam milhões de mortes por ano. Essas condições muitas vezes progridem de forma lenta, porém implacável, ocasionando fibrose ou remodelamento dos pulmões e dos vasos sanguíneos e deixando as pessoas com falta de ar. Os tratamentos atuais atuam principalmente no controle dos sintomas; não interrompem nem reparam totalmente o dano subjacente. Isso tem levado os cientistas a buscar causas mais profundas, especialmente aquelas que possam ser modificadas antes que a doença se torne grave.
Vizinhos microbianos no intestino e na pele
Sabe‑se agora que o intestino e a pele abrigam comunidades microbianas complexas que ajudam a educar o sistema imune, moldar o metabolismo e manter defesas de barreira. Mas esses micróbios estão realmente impulsionando a doença pulmonar, ou simplesmente mudam à medida que as pessoas adoecem? Para desvendar causa e efeito, os pesquisadores usaram um método chamado randomização mendeliana, que aproveita diferenças genéticas naturais entre indivíduos como uma espécie de “experimento” vitalício. Eles combinaram dados genéticos sobre centenas de tipos de micróbios intestinais e cutâneos com dados sobre cinco grandes doenças pulmonares crônicas de estudos europeus de grande porte, testando se tendências hereditárias a níveis mais altos ou mais baixos de micróbios específicos se associam ao risco de cada doença.
Micróbios que ajudam ou prejudicam os pulmões
A análise identificou dezenas de micróbios intestinais que aumentavam ou diminuíam o risco de cada doença respiratória, muitas vezes em padrões específicos por condição. Por exemplo, certas bactérias intestinais pareciam proteger contra DPOC, asma ou HAP, enquanto outras elevavam as chances de DPI ou DPOC. Micróbios da pele mostraram associações mais modestas, mas ainda detectáveis, com algumas espécies ligadas a maior risco e outras a menor risco em diferentes condições. A equipe também inverteu a direção da análise, encontrando que o risco genético para DPOC, asma e outras doenças pulmonares, por sua vez, previa mudanças tanto na microbiota intestinal quanto na cutânea. Esse tráfego bidirecional sugere um ciclo de retroalimentação: micróbios podem contribuir para moldar a doença pulmonar, e a doença pulmonar pode remodelar nossos ecossistemas microbianos.
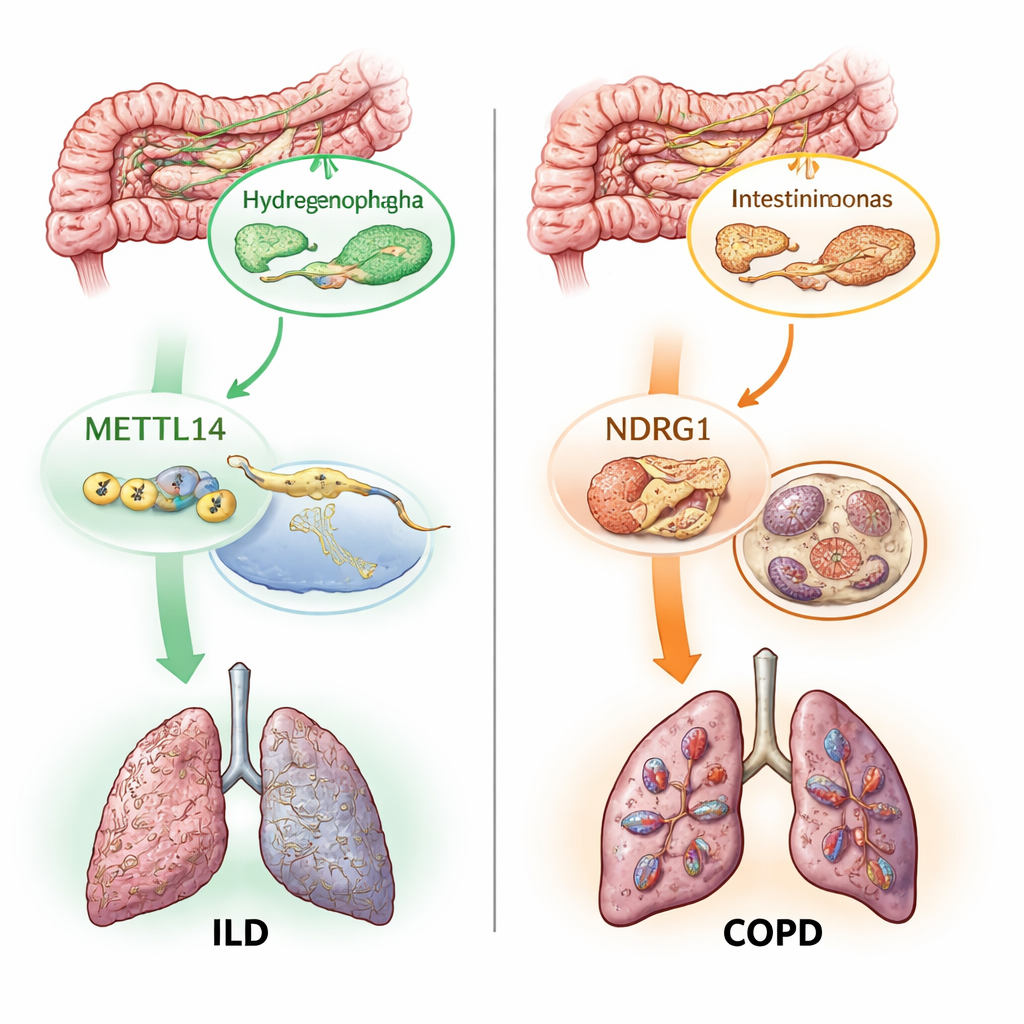
Dois interruptores moleculares: marcas de RNA e morte celular dependente de ferro
Além de mapear quais micróbios são importantes, os autores investigaram como esses parceiros microscópicos poderiam influenciar os tecidos pulmonares. Eles se concentraram em dois processos moleculares já suspeitos de participar do dano pulmonar. O primeiro, chamado modificação m6A, é uma pequena marca química adicionada ao RNA que regula como os genes são ativados ou silenciados. O segundo, ferroptose, é uma forma de morte celular dependente de ferro, impulsionada pela oxidação desenfreada de lipídios nas membranas celulares. Usando proxies genéticos para 19 genes relacionados à m6A e centenas de genes relacionados à ferroptose, testaram se alterações nessas vias se relacionam causalmente com doença pulmonar. Encontraram que um gene “writer” de m6A, METTL14, estava ligado a menor risco de DPI, e vários genes de ferroptose, incluindo NDRG1, foram associados a maior risco de DPOC, DPI e asma.
Conectando os pontos: de micróbios a células a doença
A parte mais inédita do trabalho foi traçar como essas peças se encaixam em cadeias de causa e efeito. Análises estatísticas de mediação sugeriram que parte do efeito protetor de METTL14 sobre a DPI passa por mudanças que ele induz em um micróbio intestinal particular chamado Hydrogenophaga. Em outro caminho, uma bactéria intestinal específica, Intestinimonas massiliensis, pareceu influenciar o risco de DPOC em parte ao ativar NDRG1 e o programa de morte por ferroptose. A equipe então verificou dados de tecido pulmonar humano e confirmou que tanto METTL14 quanto NDRG1 são expressos de forma diferente em amostras doentes em comparação com amostras saudáveis. Por fim, usando mapas genéticos de célula única de células imunes, localizaram o efeito prejudicial de NDRG1 na DPOC em um subconjunto de células imunes — um tipo de monócito — sugerindo que futuros medicamentos que tenham esse gene como alvo podem precisar agir de forma específica por tipo celular.
O que isso significa para tratamentos futuros
Para quem não é especialista, a mensagem-chave é que a saúde pulmonar não depende apenas do que respiramos, mas também dos micróbios que vivem em nós e dos interruptores moleculares que eles acionam dentro de nossas células. Este estudo não pode provar experimentalmente cada etapa, e é limitado principalmente a pessoas de ascendência europeia, mas oferece fortes pistas genéticas de que micróbios intestinais, marcas de RNA como m6A e morte celular dependente de ferro formam uma via conectada que leva ao dano pulmonar crônico. A longo prazo, essa linha de pesquisa pode inspirar novas estratégias que combinem terapias baseadas no microbioma com fármacos direcionados a METTL14, NDRG1 ou à ferroptose, visando não apenas aliviar sintomas, mas interromper os circuitos biológicos que fazem as doenças respiratórias crônicas progredirem.
Citação: Zhang, J., Liu, X., Liu, X. et al. Host m6A modifications shape microbiota that drives cell specific ferroptosis as a causal pathway to chronic respiratory diseases. Sci Rep 16, 5809 (2026). https://doi.org/10.1038/s41598-026-36513-2
Palavras-chave: microbioma intestinal, doença pulmonar crônica, asma e DPOC, epigenética do RNA, vias de morte celular