Clear Sky Science · pt
A fosforilação de cortactina por NEK7 modula a capacidade migratória de células que expressam EML4-ALK V3
Por que o movimento celular importa no câncer de pulmão
O câncer se torna perigoso quando as células aprendem a viajar. No câncer de pulmão não pequenas células, alguns tumores se espalham pelo corpo mais rápido que outros, e um dos culpados é uma proteína de fusão defeituosa chamada EML4-ALK. Uma versão particular, conhecida como variante 3 (V3), está associada a uma doença especialmente agressiva e a respostas pobres a drogas direcionadas. Este estudo faz uma pergunta básica, porém vital: o que permite que essas células cancerosas dirigidas por V3 mudem de forma e se movam com tanta eficiência, e podemos identificar as partes moleculares que tornam isso possível?
Uma variante de câncer de pulmão hiper-migratória
Os médicos já sabiam que apenas uma minoria dos cânceres de pulmão carrega a fusão EML4-ALK, mas pacientes cujos tumores expressam a forma V3 tendem a ter prognóstico pior do que aqueles com outras variantes. Ao microscópio, células que expressam V3 parecem diferentes: em vez de serem compactas e em forma de mosaico, esticam-se em formas longas e finas com protrusões alongadas, lembrando células em movimento. Trabalhos anteriores mostraram que esse comportamento depende de duas enzimas, NEK9 e NEK7, que atuam como interruptores moleculares nas células. No entanto, os alvos downstream cruciais desses interruptores — aqueles que remodelam diretamente o esqueleto interno da célula — não eram bem compreendidos.
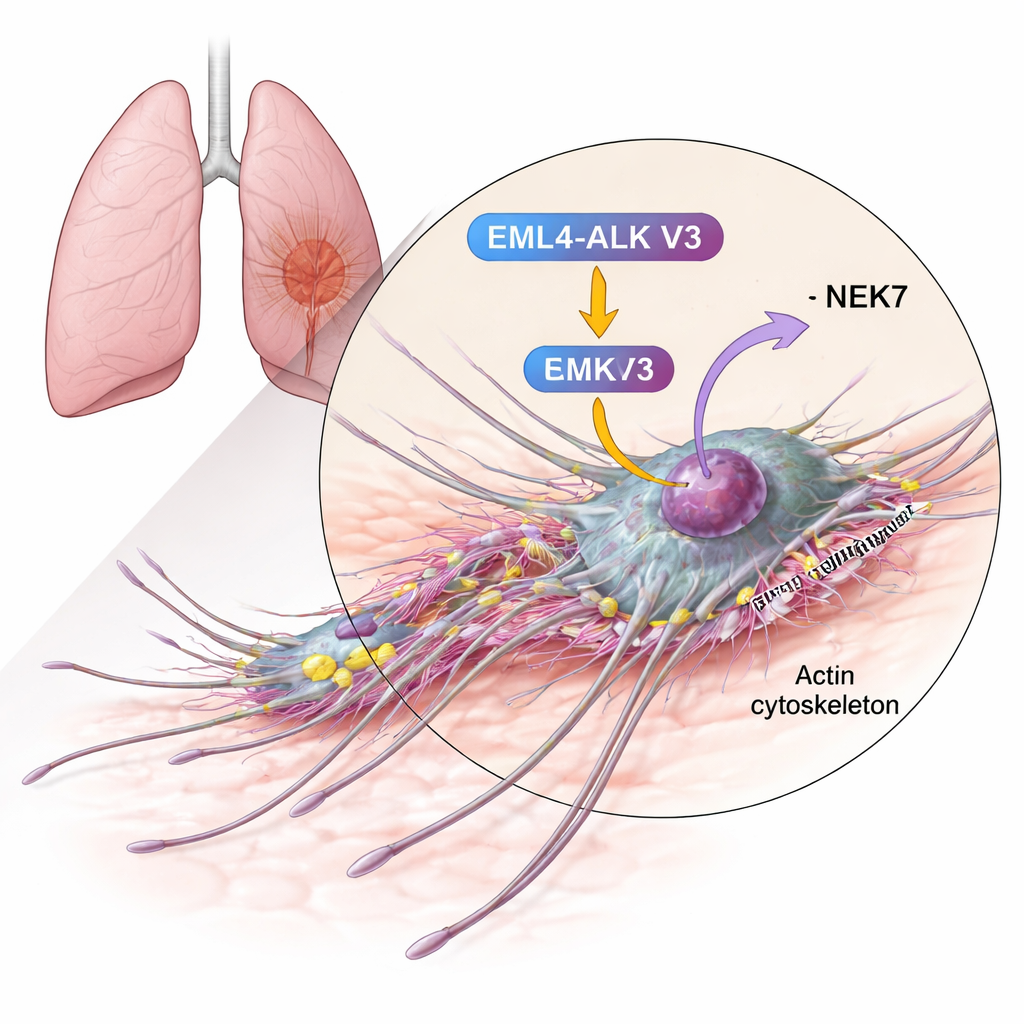
Ligando uma proteína de movimento a uma fusão agressiva
Os autores focaram na cortactina, uma proteína já conhecida por ser abundante em muitos cânceres invasivos e por ajudar a montar as redes de filamentos de actina que empurram a membrana celular para frente. Usando testes bioquímicos, demonstraram que a cortactina pode ser quimicamente modificada (fosforilada) por NEK6 e, ainda mais fortemente, por NEK7. As enzimas adicionam grupos fosfato a resíduos de serina específicos dentro da região de ligação à actina da cortactina — justamente o trecho que agarra as fibras de actina e estabiliza redes ramificadas. Quando NEK7 estava presente, a cortactina apresentava mais grupos fosfato e em mais sítios do que com NEK6, sugerindo que NEK7 é o regulador primário nesse contexto.
Desligar a cortactina interrompe a migração de células cancerosas
Para ver o que a cortactina realmente faz em células vivas, os pesquisadores a reduziram usando interferência por RNA em células geneticamente modificadas para ativar NEK9 ou NEK7, ou para expressar o próprio EML4-ALK V3. Em todas as três situações, as formas alongadas e mesenquimais impressionantes colapsaram: as células ficaram mais achatadas e arredondadas, perderam suas longas protrusões e formaram, em vez disso, fibras grossas e retilíneas de actina "stress fibers" cruzando a célula. Diversos ensaios de migração — desde o fechamento de “feridas” artificiais em uma monocamada celular até o acompanhamento de células individuais e a medição do movimento em direção a um sinal químico — mostraram que, sem cortactina, essas células altamente móveis desaceleraram drasticamente. Efeitos semelhantes foram observados em linhagens celulares de câncer de pulmão estabelecidas que carregam naturalmente EML4-ALK V3, ressaltando a relevância clínica da via.
Filamentos finos e pontas agudas na borda de avanço
Imagens de alta resolução em células epiteliais brônquicas revelaram um quadro ainda mais detalhado. Células que expressam EML4-ALK V3 produziram muitas extensões finas, por vezes ramificadas, semelhantes a filopódios nas suas protrusões. Nas pontas e nos pontos de ramificação dessas estruturas, cortactina, EML4-ALK V3, NEK7 e uma forma fosforilada da cortactina se agrupavam. Essa estreita colocalização sugere um “canteiro de obras” focalizado onde NEK7 modifica a cortactina para construir e manter as delicadas redes de actina ramificadas que ajudam a guiar a célula. Quando a cortactina foi removida, essas extensões intrincadas desapareceram e o crescimento invasivo de esferoides tumorais 3D em um gel circundante foi fortemente reduzido.
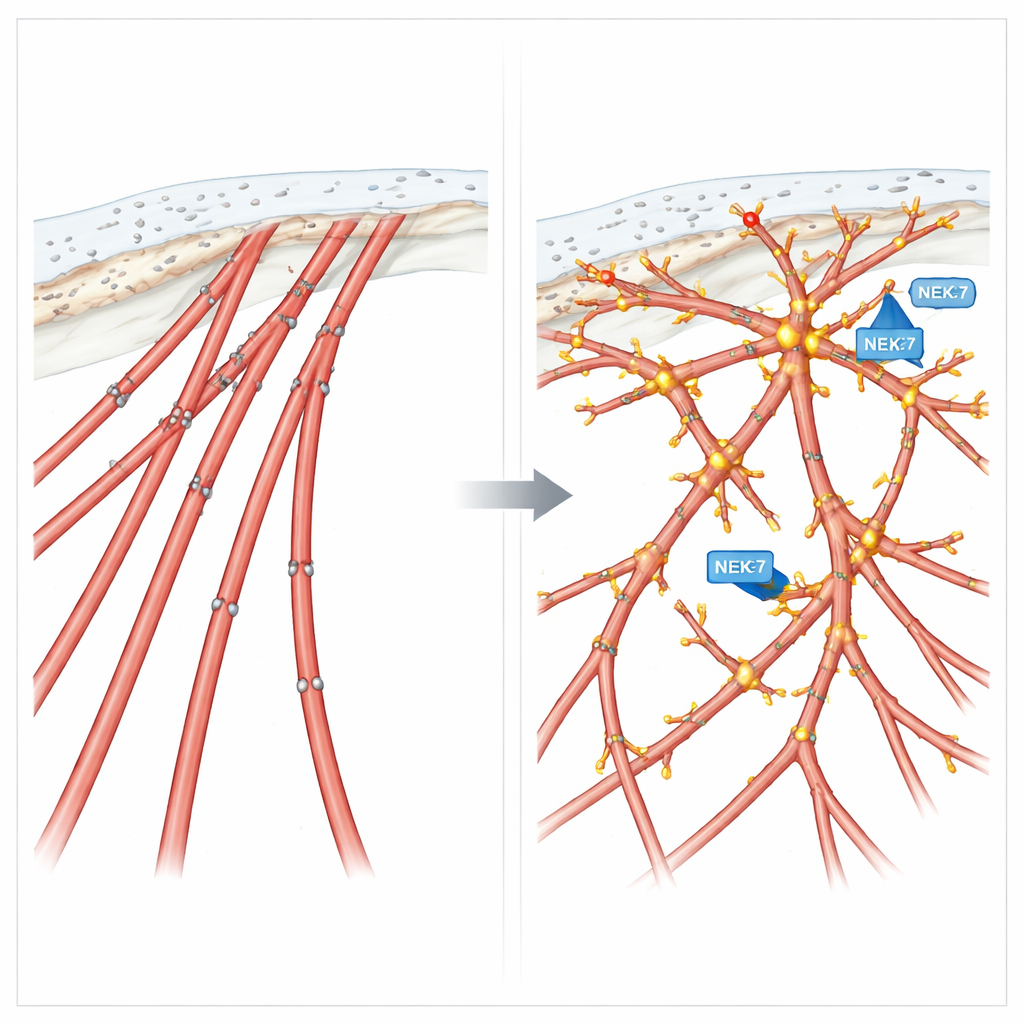
Fosforilação como um botão de controle da migração
Para testar como essas marcas químicas na cortactina influenciam o comportamento, a equipe criou duas versões projetadas da proteína: uma forma fosfo-mimética que imita fosforilação constante em quatro sítios-chave, e uma forma fosfo-nula que não pode ser fosforilada nesses sítios. Células que expressavam a versão mimética desenvolveram abundantes extensões tipo filopódio e mostraram migração dirigida aumentada, semelhante a células com NEK7 ativo ou EML4-ALK V3. Em contraste, células que expressavam a versão não fosforilável formaram fibras de stress rígidas, perderam essas finas extensões e moviam-se de maneira rápida, porém sem rumo — boas em perambular, ruins em seguir um sinal. Em culturas tridimensionais, essa cortactina fosfo-nula promoveu brotos invasivos desorganizados em vez de precisamente orientados.
O que isso significa para entender — e combater — a disseminação
Em termos simples, o estudo mostra que a agressiva variante de câncer de pulmão EML4-ALK V3 sequestra um sistema normal de modelagem celular. Ao ativar NEK7, ela causa a fosforilação da cortactina em sítios específicos dentro de sua região de ligação à actina. Essa modificação ajusta a cortactina para que ela possa construir estruturas de actina finamente ramificadas e extensões tipo filopódio que sustentam migração rápida, dirigida e invasão. Interromper a cortactina ou sua fosforilação inverte o sistema: as células ou mal se movem ou se movem de maneira caótica e sem direção. Essas percepções revelam uma cadeia molecular concreta — desde uma fusão que dirige o câncer, passando por NEK7, até a cortactina e o citoesqueleto de actina — que ajuda a explicar por que alguns cânceres de pulmão metastizam tão efetivamente, e apontam para novas maneiras de desacelerar ou desviar seu movimento.
Citação: Richardson, E.L., Knebel, A., Straatman, K.R. et al. NEK7 phosphorylation of cortactin modulates the migratory capacity of cells expressing EML4-ALK V3. Sci Rep 16, 6407 (2026). https://doi.org/10.1038/s41598-026-36484-4
Palavras-chave: câncer de pulmão não pequenas células, EML4-ALK V3, migração celular, cortactina, citoesqueleto de actina