Clear Sky Science · pt
Uma abordagem integrativa para identificar novas redes de interação miRNA-mRNA na cardiomiopatia por LMNA
Por que pequenos reguladores do coração importam
A cardiomiopatia dilatada é uma condição grave em que o coração aumenta de tamanho e enfraquece, frequentemente levando à insuficiência cardíaca, ritmos cardíacos perigosos e até morte súbita. Para muitas famílias, essa doença é hereditária, e alterações em um gene chamado LMNA são uma causa frequente. Este estudo faz uma pergunta aparentemente simples, mas com grandes consequências: em corações danificados por mutações em LMNA, quais genes são ativados ou silenciados, e quais pequenas moléculas de RNA estão puxando esses interruptores? Ao mapear essas conversas moleculares em detalhe, o trabalho aponta para novas formas de prever, monitorar e talvez um dia tratar essa forma agressiva de doença cardíaca.
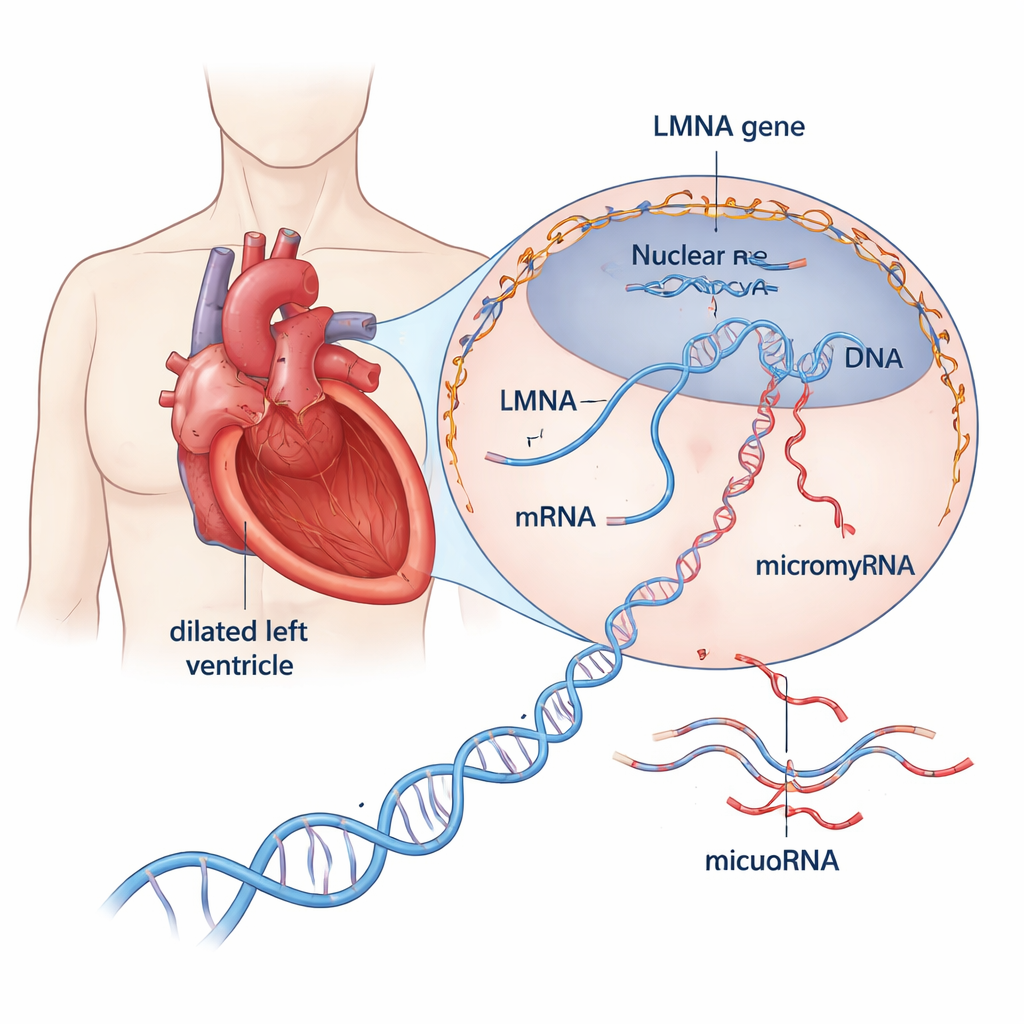
Uma visão mais próxima de uma doença cardíaca perigosa
A cardiomiopatia dilatada estica e afina a principal câmara de bombeamento do coração, enfraquecendo sua capacidade de impulsionar o sangue pelo corpo. Cerca de um terço a metade dos casos antes chamados de “idiopáticos” agora mostram ter uma base genética. Entre os mais de 30 genes envolvidos, o LMNA se destaca: variantes prejudiciais nesse gene respondem por aproximadamente 10% dos casos herdados e estão associadas à progressão rápida da doença, problemas de ritmo precoces e alto risco de morte súbita cardíaca. O LMNA produz proteínas estruturais que formam uma armação ao redor do DNA da célula, ajudando a manter a forma do núcleo e influenciando quais genes estão ativos. Ainda assim, como proteínas LMNA defeituosas conduzem o coração ao fracasso permanece pouco compreendido.
Seguindo as mensagens dentro de corações de camundongo
Para explorar isso, os pesquisadores usaram um modelo de camundongo portador de uma mutação LMNA bem conhecida (R249W) que desenvolve uma forma de cardiomiopatia dilatada semelhante à doença humana. Aos 50 semanas de idade — quando os camundongos apresentam ventrículos aumentados, função de bombeamento reduzida e cicatrizes fibróticas — a equipe extraiu tecido cardíaco e examinou dois tipos de RNA: RNA mensageiro (mRNA), que carrega instruções para produzir proteínas, e microRNA (miRNA), pequenas cadeias não codificantes que ajustam a atividade gênica bloqueando ou degradando mRNAs específicos. Usando sequenciamento de alto desempenho e filtros estatísticos rigorosos, identificaram 2.148 genes cuja atividade mudou em corações mutantes e 53 miRNAs que estavam aumentados ou reduzidos em comparação com camundongos saudáveis.
O que muda dentro das células cardíacas doentes
Quando os pesquisadores agruparam os genes alterados em vias biológicas, emergiram vários temas. Muitos dos genes alterados estavam ligados a como as células do músculo cardíaco se contraem, como elas se aderem entre si e à matriz de suporte ao redor, como os sinais elétricos se propagam pelo coração e como as células processam gorduras para gerar energia. Essas descobertas se alinham bem ao quadro clínico da doença relacionada ao LMNA: tecido rígido e fibrótico; condução elétrica perturbada que favorece arritmias; e equilíbrio energético comprometido. Análises de vias usando bancos de dados estabelecidos confirmaram enriquecimento em remodelação da matriz extracelular, canais iônicos dependentes de voltagem, comunicação tipo sináptica no coração e metabolismo de ácidos graxos — sugerindo que a mutação em LMNA perturba múltiplos sistemas interconectados em vez de um único passo defeituoso.
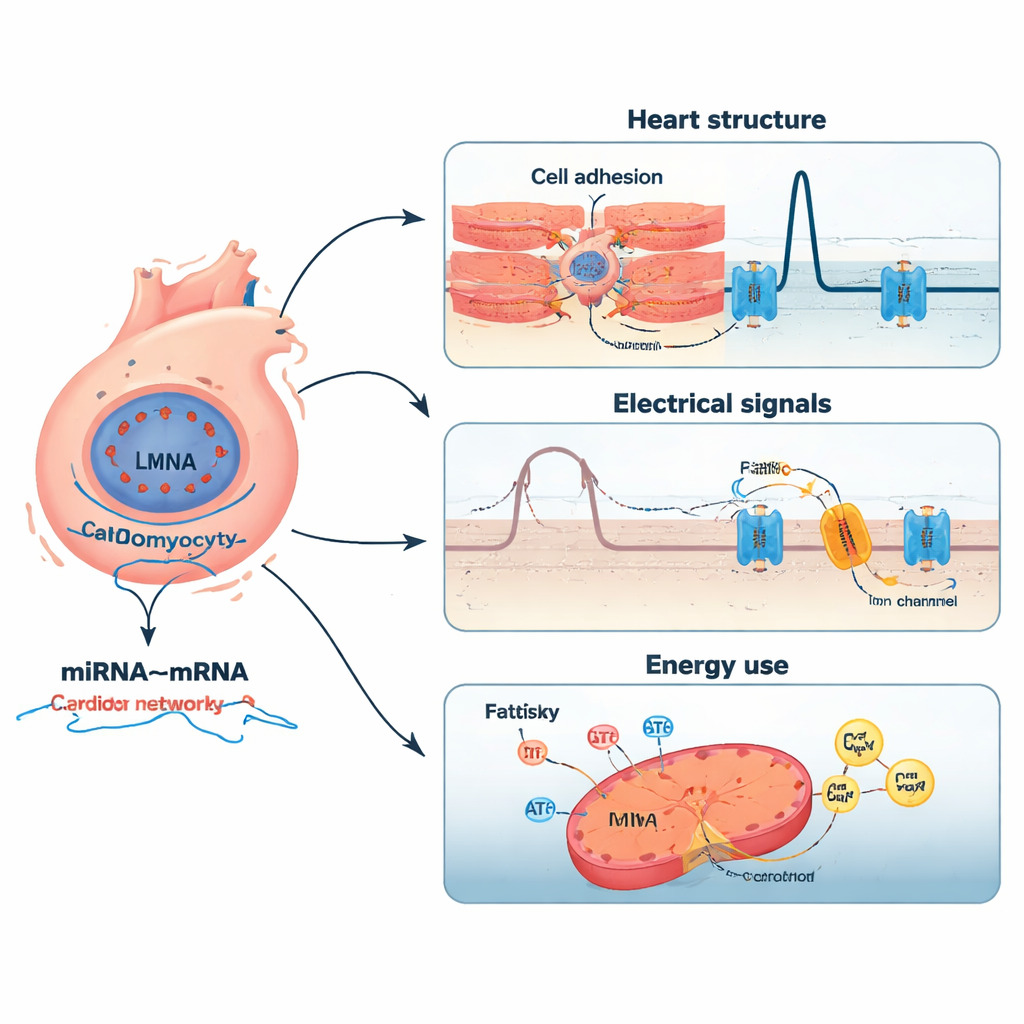
Redes de pequenos interruptores e seus alvos
O estudo avançou ao emparelhar miRNAs com seus prováveis alvos de mRNA. Usando análises de correlação e cruzamento com grandes bancos de dados de interações validadas experimentalmente, os autores montaram uma rede de alta confiança com 2.197 pares miRNA–mRNA envolvendo 12 miRNAs-chave. Alguns miRNAs estavam mais ativos e pareciam reprimir genes críticos para desenvolvimento cardíaco, manejo de cálcio e respostas ao estresse oxidativo. Outros estavam menos ativos, potencialmente liberando freios sobre genes envolvidos na adesão celular, inflamação e remodelamento da estrutura do coração. Por exemplo, um miRNA (miR-183-5p) foi ligado a um receptor na via de sinalização Wnt, que influencia a comunicação entre células, enquanto outro (miR-3473a) conectou-se a um canal de liberação de cálcio central para o ritmo cardíaco. Juntas, essas redes descrevem como mudanças sutis em pequenos reguladores de RNA podem amplificar o impacto de uma mutação em LMNA.
De mapas moleculares a futuras terapias
Para leitores não especialistas, a conclusão é que este estudo oferece um mapa detalhado de como uma mutação em LMNA reconfigura a fiação interna do coração no nível do controle gênico. Em vez de um único “gene ruim”, a doença reflete uma cascata de mensagens alteradas — muitas orquestradas por miRNAs — que afetam a estrutura do coração, a estabilidade elétrica e o uso de energia. Embora o trabalho tenha sido feito em camundongos e dependa fortemente de análises computacionais, ele destaca pares específicos miRNA–gene como candidatos promissores para futuros biomarcadores detectáveis no sangue ou terapias direcionadas. A longo prazo, ajustar esses pequenos interruptores de RNA pode ajudar médicos a prever melhor quem está em maior risco, monitorar a progressão da doença com mais precisão e projetar tratamentos mais personalizados para famílias afetadas pela cardiomiopatia relacionada ao LMNA.
Citação: Córdoba-Caballero, J., Martínez, F.B., Campuzano, O. et al. An integrative approach to identify novel miRNA-mRNA interaction networks in LMNA-cardiomyopathy. Sci Rep 16, 6110 (2026). https://doi.org/10.1038/s41598-026-36439-9
Palavras-chave: cardiomiopatia dilatada, gene LMNA, microRNA, regulação gênica, insuficiência cardíaca