Clear Sky Science · pt
A atividade antitumoral de QAL333 e modelagem preditiva: análise integrada transcriptômica-bioinformática revela citotoxicidade seletiva e determinantes de sensibilidade
Por que esse novo candidato a fármaco é importante
Fármacos contra o câncer costumam funcionar bem para alguns pacientes e falhar em outros, em grande parte porque os tumores diferem em sua arquitetura interna. Este estudo apresenta um composto recém-desenvolvido, QAL333, que parece atingir certos cânceres colorretais com muito mais eficácia do que outros, poupando muitas células normais. Igualmente importante, os pesquisadores mostram como padrões de atividade gênica nas células tumorais podem ajudar a prever quem tem maior probabilidade de se beneficiar, apontando para estratégias de tratamento mais precisas e personalizadas.
Um ataque focado em tipos tumorais específicos
A equipe começou testando QAL333, uma molécula sintética relacionada a uma família de compostos já conhecida por danificar células cancerosas, em um amplo painel de 15 linhas celulares humanas de câncer e três linhas não cancerosas. Eles descobriram que células de câncer colorretal, especialmente uma linha chamada SW620, eram altamente sensíveis, com o fármaco as matando em doses relativamente baixas. Em contraste, células de câncer de mama triplo-negativo foram muito mais resistentes e exigiram doses mais de dez vezes maiores, difíceis de serem alcançadas de forma segura. Curiosamente, nem todas as células não cancerosas reagiram da mesma maneira: algumas foram sensíveis, mas outras, como uma linha de células renais amplamente usada, mostraram-se surpreendentemente resistentes. Esse padrão indicou que os efeitos de QAL333 dependem mais da biologia interna da célula do que de ela ser rotulada como “câncer” ou “normal”.
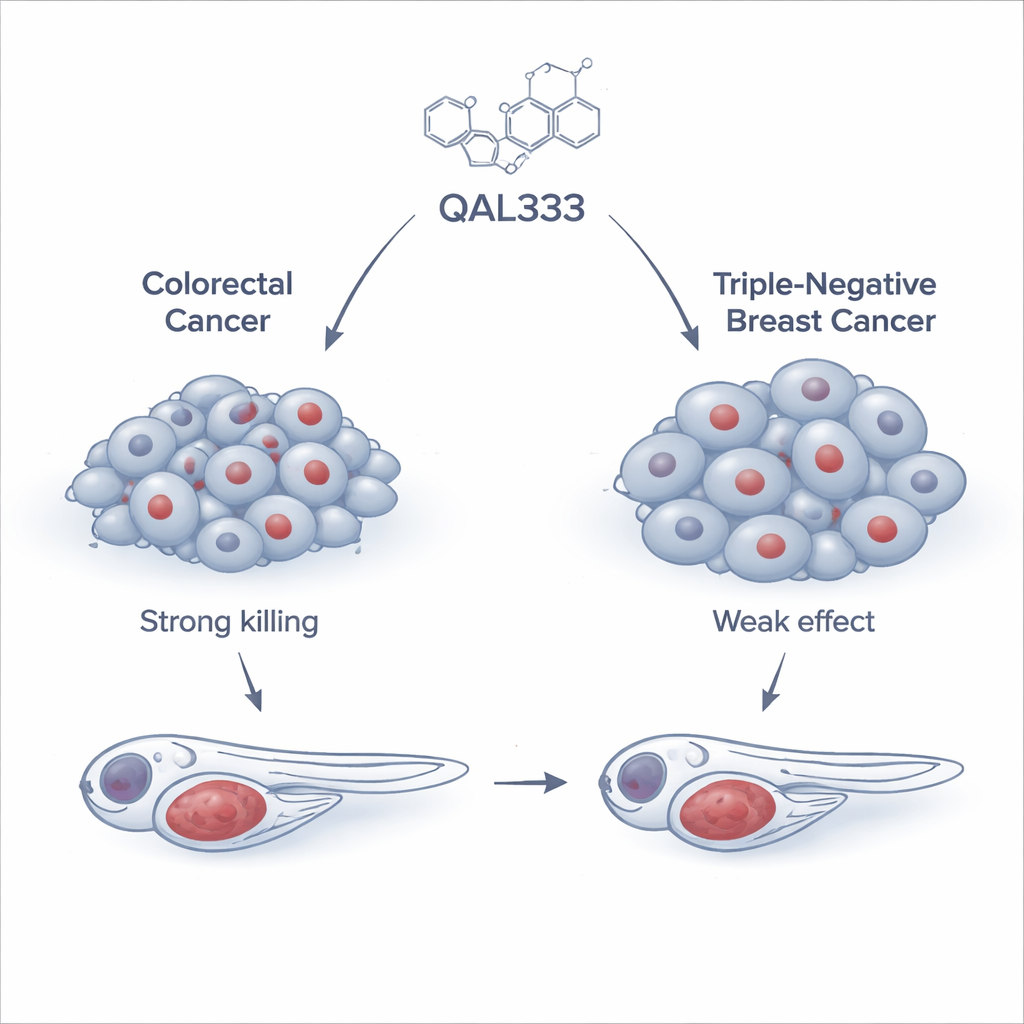
Testando o fármaco em organismos vivos
Para verificar se os resultados promissores em cultura celular se manteriam em um organismo vivo, os pesquisadores recorreram ao zebrafish, um pequeno peixe transparente amplamente usado para modelar doenças humanas. Eles implantaram células humanas cancerosas marcadas fluorescentemente em embriões de zebrafish e trataram-nos com QAL333. Em peixes que carregavam células de câncer colorretal, o fármaco claramente retardou o crescimento tumoral, aproximando-se do efeito de uma combinação quimioterápica padrão utilizada na clínica. Em contraste, tumores formados a partir das células de câncer de mama triplo-negativo mal responderam, embora um fármaco comum para câncer de mama, paclitaxel, tenha funcionado bem no mesmo modelo. Esses testes in vivo reforçaram que a força de QAL333 está em um subconjunto de tumores, e não em todos os cânceres.
Observando dentro das células para entender como QAL333 atua
Para entender por que algumas células morrem e outras resistem, os cientistas mediram como milhares de genes alteraram seus níveis de atividade após o tratamento com QAL333. Em células colorretais sensíveis, genes-chave que impulsionam o ciclo de divisão e o crescimento celular foram reprimidos, e vias principais de sobrevivência foram atenuadas. Sinais ligados ao estresse oxidativo e a uma forma de morte celular distinta da apoptose clássica também foram alterados, sugerindo que QAL333 sobrecarrega sistemas já frágeis que gerenciam danos dentro dessas células. Células resistentes de câncer de mama, por outro lado, ativaram programas de estresse e inflamação controlados por fatores como NF-κB, conhecidos por ajudar as células a lidar com condições nocivas. Essa comparação lado a lado pintou um quadro de QAL333 sobrepujando defesas frágeis em algumas células enquanto outras montam uma resposta contrária eficaz.
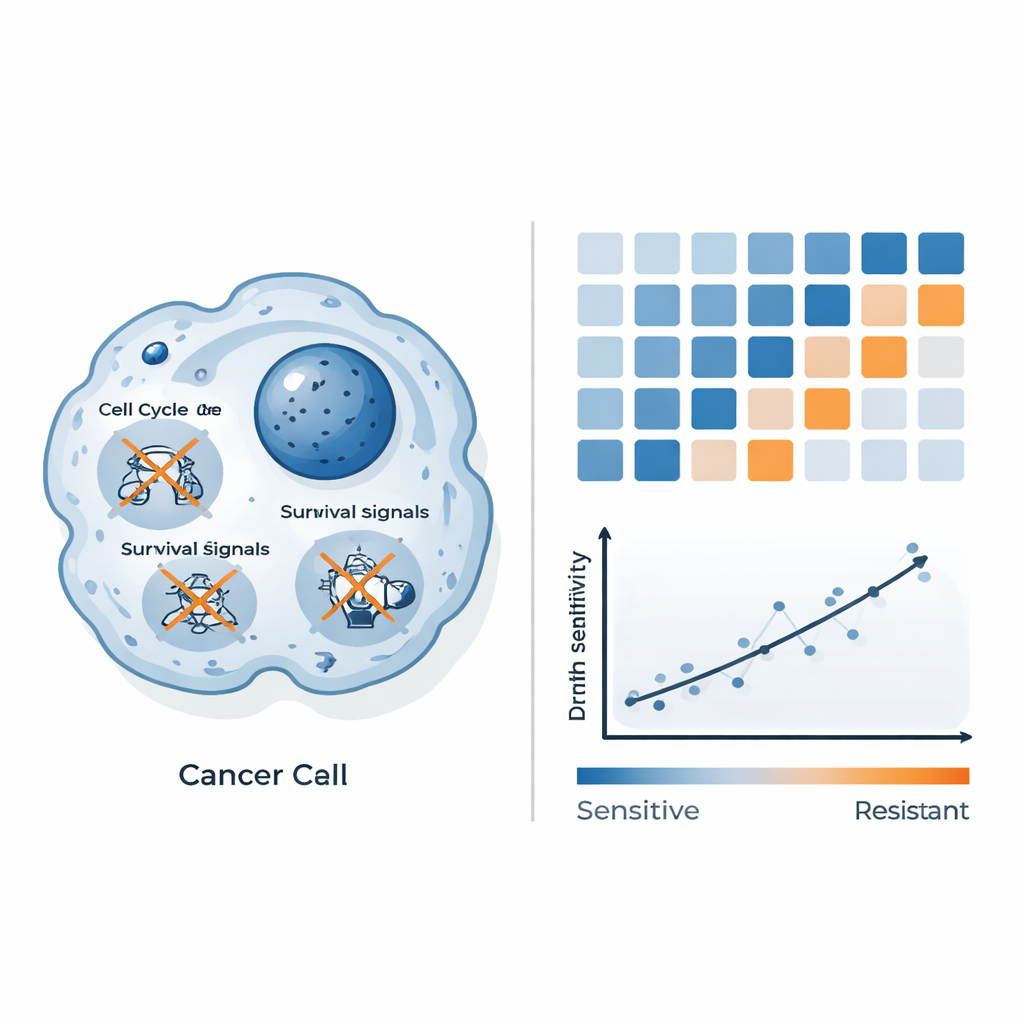
Usando padrões gênicos para prever quem responderá
Além de catalogar alterações gênicas, os pesquisadores perguntaram se esses padrões poderiam ser transformados em uma ferramenta preditiva prática. Eles combinaram dados de atividade gênica basal do painel de linhas celulares com sua sensibilidade medida ao fármaco e usaram aprendizado de máquina para buscar os sinais mais informativos. Em vez de confiar em genes isolados, agruparam genes em vias biológicas e criaram uma “pontuação de vias” combinada construída a partir de três sistemas: como as células processam energia e químicos (vias metabólicas), como organizam seu entorno (proteoglicanos e estruturas relacionadas no câncer) e como o seu citoesqueleto está arranjado. Essa pontuação composta acompanhou fortemente a quantidade de QAL333 necessária para matar cada linha celular: pontuações mais baixas alinharam-se com maior sensibilidade, e pontuações mais altas com resistência. Em outras palavras, a forma como essas redes estão ajustadas dentro de um tumor pode prever o quão bem QAL333 funcionará.
Pistas inesperadas de efeitos biológicos mais amplos
Embora o foco principal fosse o câncer, QAL333 também mostrou capacidade de interferir na “quorum sensing”, um sistema de comunicação que bactérias usam para coordenar comportamentos como a formação de biofilmes. Em doses minúsculas, o composto reduziu a formação de biofilme por uma bactéria associada à doença gengival e atenuou certos sinais inflamatórios em células imunes. Os autores tratam esses resultados como achados iniciais e exploratórios, mas sugerem que QAL333 ou moléculas relacionadas podem um dia ter usos além da terapia contra o câncer, por exemplo em infecções onde comunidades bacterianas são difíceis de erradicar.
O que isso pode significar para pacientes no futuro
No conjunto, o estudo posiciona QAL333 como um candidato a fármaco seletivo que atinge tumores colorretais vulneráveis enquanto poupa muitos outros tipos celulares, e o reúne com um roteiro para prever quais tumores têm maior probabilidade de responder. Se confirmado em modelos animais mais avançados e eventualmente em pacientes, um simples teste de expressão gênica poderia ajudar médicos a decidir quando QAL333 é uma boa opção, alinhando-se ao objetivo mais amplo de adequar o tratamento do câncer à arquitetura de cada tumor. Ao mesmo tempo, o trabalho ressalta que mesmo fármacos promissores têm limites: cânceres de mama e outros tumores resistentes podem exigir combinações inteligentes ou estratégias totalmente diferentes.
Citação: Kim, H.H., Im, S., Kim, J. et al. QAL333’s antitumor activity and predictive modeling: integrated transcriptomic-bioinformatic analysis reveals selective cytotoxicity and sensitivity determinants. Sci Rep 16, 5648 (2026). https://doi.org/10.1038/s41598-026-36430-4
Palavras-chave: câncer colorretal, terapia direcionada, expressão gênica, modelagem de sensibilidade a fármacos, xenotransplante em zebrafish