Clear Sky Science · pt
Da modelagem QSAR in-silico ao ensaio MTT in-vitro: validação experimental de novos candidatos ao uPAR para câncer de mama triplo-negativo (TNBC) e câncer de pele
Por que esta pesquisa importa
Cânceres como o carcinoma de mama triplo‑negativo e certos cânceres de pele são notoriamente difíceis de tratar porque se espalham rapidamente e frequentemente resistem às terapias padrão. Este estudo investiga um novo alvo promissor na superfície das células tumorais — chamado uPAR — e mostra como a combinação de desenho de fármacos por computador com experimentos de laboratório pode revelar novos candidatos a medicamentos que podem retardar ou impedir a disseminação desses tumores agressivos.
Uma porta que ajuda o câncer a se espalhar
Para um tumor se tornar letal, suas células precisam se desprender do local original, degradar o tecido circundante, entrar na corrente sanguínea e colonizar órgãos distantes. O uPAR é um ajudante chave nesse processo. Ele fica na superfície da célula cancerosa e atua com proteínas parceiras para ativar enzimas que dissolvem a estrutura de suporte ao redor, facilitando a movimentação e a invasão celular. O uPAR é encontrado em níveis especialmente altos em células de câncer de mama triplo‑negativo e em certos cânceres de pele, e sua abundância está associada a crescimento mais rápido, maior invasividade e piores desfechos clínicos. Por isso, o uPAR é um alvo atraente — embora até agora pouco explorado — para fármacos anticâncer.
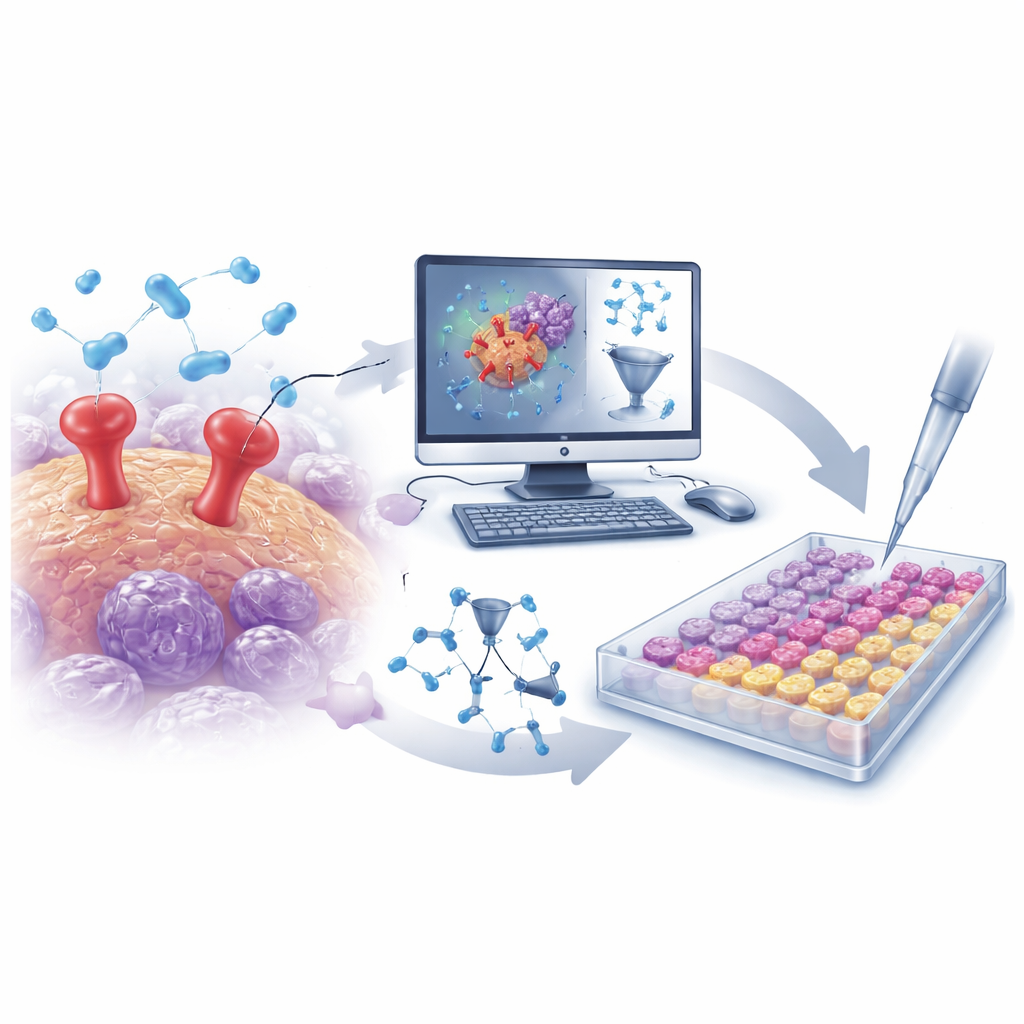
Minerando grandes dados químicos com algoritmos inteligentes
Os pesquisadores começaram reunindo uma grande coleção de mais de 500 moléculas conhecidas por bloquear o uPAR a partir de um banco de dados público. A estrutura de cada molécula foi traduzida em milhares de descritores numéricos que capturam características como tamanho, forma, distribuição de carga e flexibilidade. Com esses dados, a equipe construiu um modelo de relação quantitativa estrutura‑atividade (QSAR) — um tipo de ferramenta matemática que aprende quais características estruturais tendem a tornar uma molécula um inibidor mais potente do uPAR. Após validação cuidadosa para evitar sobreajuste, o modelo mostrou alto poder preditivo em compostos não vistos, destacando várias características chave que fortaleciam ou enfraqueciam o bloqueio do uPAR. Esses insights guiaram a busca por moléculas novas e melhor projetadas.
De triagens virtuais a tubos de ensaio reais
Munida do modelo QSAR treinado, a equipe fez uma triagem virtual de uma biblioteca focalizada de cerca de 30.000 moléculas direcionadas a proteases. O modelo rapidamente reduziu esse vasto conjunto a um pequeno grupo de prováveis inibidores de uPAR. Em paralelo, simulações de docking computacional foram usadas para avaliar quão bem cada candidato poderia se encaixar no sítio de ligação do uPAR, e simulações de dinâmica molecular testaram se esses complexos docked permaneceriam estáveis ao longo do tempo. Dessa campanha in‑silico combinada, emergiram duas moléculas de destaque: D685‑0061, apontada pelo modelo QSAR como altamente potente, e C878‑1660, destacada pelo docking e simulação por formar interações especialmente estáveis com o uPAR.
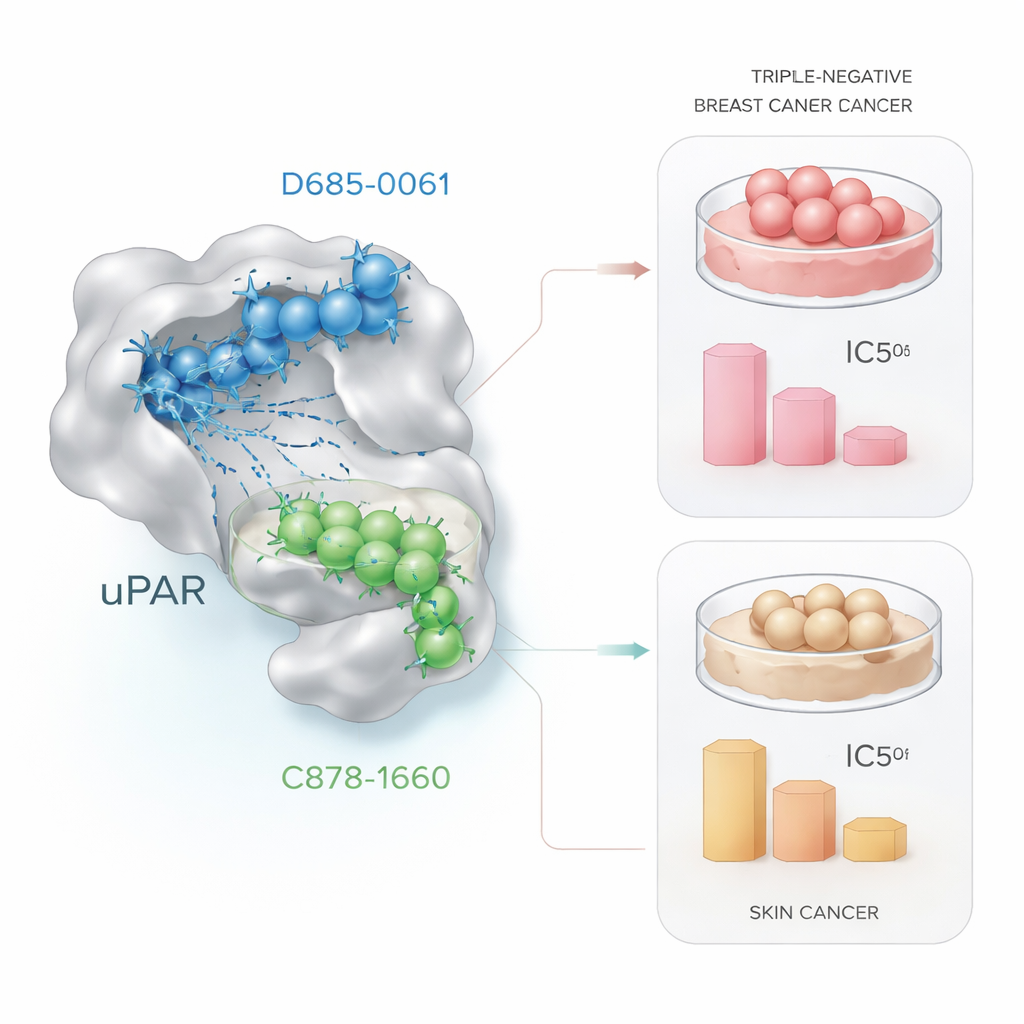
Testando os candidatos em células cancerosas
Promessas computacionais só têm sentido se se traduzirem em efeitos biológicos reais. Para verificar isso, os pesquisadores expuseram células cancerosas vivas a doses crescentes das duas moléculas candidatas e mediram a sobrevivência celular usando um método laboratorial padrão chamado ensaio MTT. Em células de câncer de mama triplo‑negativo (MDA‑MB‑231), D685‑0061 matou as células de forma mais eficiente, reduzindo a viabilidade à metade em torno de 21 micromoles, enquanto C878‑1660 exigiu cerca de quatro vezes essa concentração. Ao microscópio, células tratadas com D685‑0061 mostraram sinais claros de morte celular programada, como arredondamento, descolamento da superfície e fragmentação. Em contraste, em células de câncer de pele (A431), C878‑1660 foi o agente mais eficaz, alcançando 50% de morte celular em cerca de 19 micromoles comparado a aproximadamente 28 micromoles para D685‑0061, novamente com dano visível dependente da dose.
O que isso significa para tratamentos futuros do câncer
Este trabalho não entrega um novo fármaco imediato, mas fornece dois pontos de partida promissores e, tão importante quanto, um roteiro poderoso para encontrar mais. Ao ligar modelagem de big data, simulações 3D e experimentos celulares cuidadosos, o estudo mostra que o uPAR pode ser direcionado seletivamente com pequenas moléculas que lesionam células agressivas de câncer de mama e de pele. D685‑0061 e C878‑1660 agora servem como compostos lideres que químicos podem refinar para aumentar potência, melhorar segurança e otimizar o perfil farmacocinético. Em prazo mais longo, fármacos desenvolvidos a partir dessa abordagem poderiam ajudar a bloquear a disseminação de cânceres conduzidos pelo uPAR, transformando alguns dos tumores mais perigosos de hoje em doenças mais manejáveis.
Citação: Badukle, H., Jawarkar, R.D., Shah, U. et al. From in-silico QSAR modeling to in-vitro MTT assay: experimental validation of novel uPAR leads for triple-negative breast cancer (TNBC) and skin cancer. Sci Rep 16, 5786 (2026). https://doi.org/10.1038/s41598-026-36406-4
Palavras-chave: inibidores de uPAR, câncer de mama triplo-negativo, câncer de pele, desenho de fármacos assistido por computador, ensaio de viabilidade celular MTT