Clear Sky Science · pt
Um estudo por teoria do funcional densidade da adsorção de ciclofosfamida e purinethol em uma estrutura triazina covalente (CTF-2) para aplicações em entrega de fármacos
Por que uma quimioterapia mais inteligente importa
Os medicamentos de quimioterapia salvam vidas, mas frequentemente agem como um holofote em vez de um foco — atacando células saudáveis junto com as cancerígenas. Isso pode causar efeitos colaterais sérios, desde fadiga e infecções até danos a órgãos. O estudo discutido aqui explora um material ultrafino e altamente poroso chamado estrutura triazina covalente (CTF-2) como uma “esponja inteligente” capaz de transportar dois fármacos anticâncer de longa data — ciclofosfamida e purinethol — de forma mais segura e eficiente até os locais necessários, e então liberá‑los em condições semelhantes às do tumor.
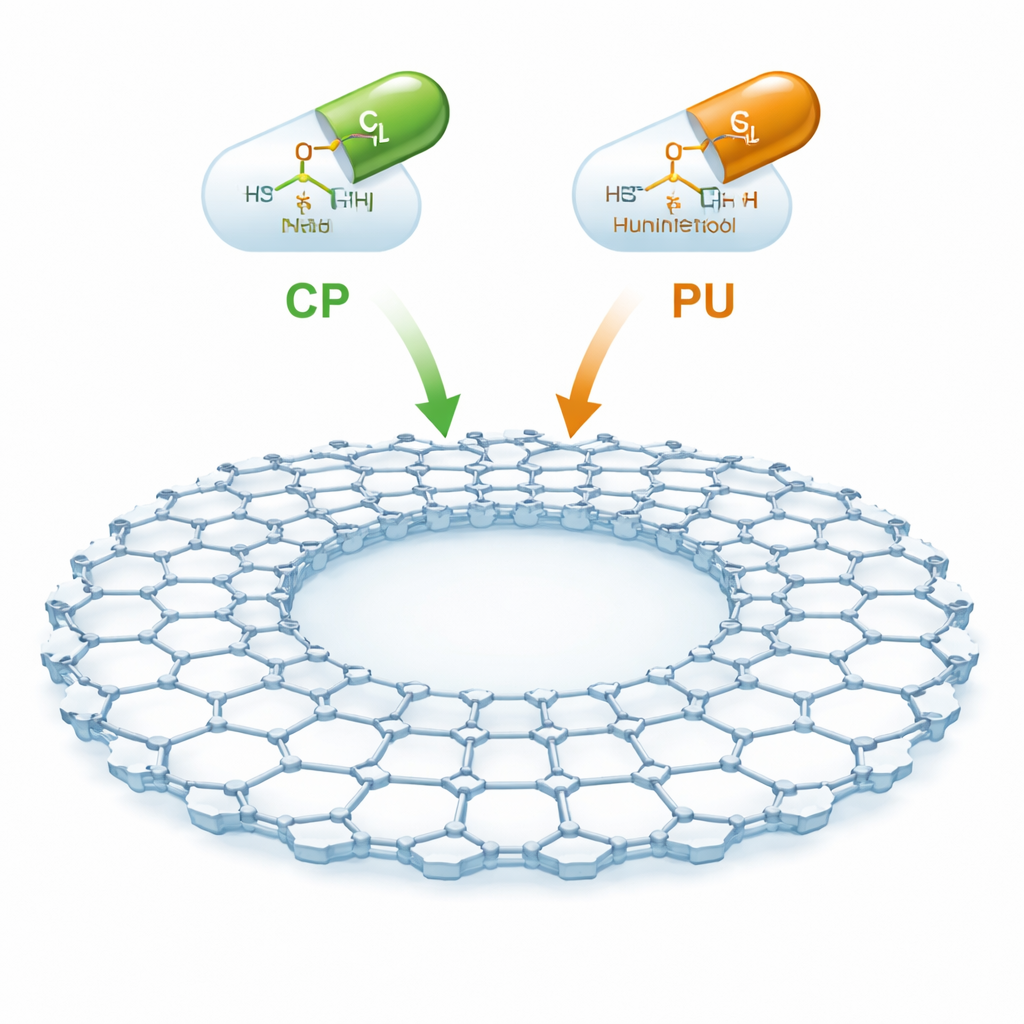
Um novo tipo de esponja molecular
CTF-2 é um material sintético construído a partir de anéis de carbono e nitrogênio ligados em uma rede plana, semelhante a uma folha, com uma grande cavidade central e muito espaço aberto. Por ser fino, estável e repleto de poros, oferece uma enorme área interna para aprisionar moléculas de fármacos. Os autores focaram em dois medicamentos importantes contra o câncer: ciclofosfamida, amplamente utilizada em cânceres hematológicos e tumores sólidos, e purinethol (também chamado de mercaptopurina), usado contra leucemias e algumas doenças inflamatórias intestinais. A ideia é ancorar esses fármacos suavemente na superfície do CTF-2 para que possam ser transportados pela corrente sanguínea e liberados de forma mais seletiva, reduzindo os danos ao tecido saudável.
Investigando o invisível com experimentos computacionais
Em vez de trabalhar em um laboratório úmido, a equipe usou cálculos computacionais avançados em nível quântico (teoria do funcional da densidade e métodos relacionados) para avaliar quão fortemente cada fármaco se fixaria ao CTF-2 e o que mantém os complexos unidos. Eles otimizaram as geometrias do CTF-2 com cada fármaco, mediram as distâncias entre átomos nos pontos de contato e calcularam quanta energia é liberada quando um fármaco adere à estrutura. Para a ciclofosfamida, a energia de adsorção calculada foi de cerca de −1,04 elétron-volt, um pouco mais forte que os −0,82 elétron-volt encontrados para o purinethol. Esses valores, que permanecem claramente favoráveis mesmo após correções por artefatos técnicos e simulações com água como solvente, indicam que ambos os fármacos se ligam com firmeza suficiente para serem carregados, mas não tão fortemente que não possam ser liberados posteriormente.
Forças suaves realizando trabalho importante
O estudo mostra que a “cola” entre os fármacos e o CTF-2 não é uma ligação química forte, mas uma teia de forças não covalentes e suaves. Usando análises especializadas da densidade eletrônica — basicamente mapas de onde os elétrons compartilhados residem — os pesquisadores descobriram que atrações de van der Waals (as mesmas forças fracas que permitem aos geckos subir paredes) e interações eletrostáticas leves predominam. Essas interações ocorrem em distâncias curtas, porém não ligantes, entre átomos de hidrogênio, nitrogênio, oxigênio, enxofre e carbono presentes nos fármacos e na estrutura. Cálculos adicionais que decompõem a atração total em diferentes componentes confirmaram que forças eletrostáticas e de dispersão (van der Waals) fornecem a maior parte do puxão estabilizador, enquanto forças repulsivas evitam que o fármaco afunde demais ou se ligue de forma irreversível.
Sinais de carregamento estável e liberação ajustável
A equipe também examinou como os elétrons se redistribuem quando os fármacos estão sobre o CTF-2 e como isso altera propriedades elétricas básicas. Eles observaram pequenas, porém claras, transferências de carga entre cada fármaco e a estrutura e um leve estreitamento da lacuna de energia que separa estados eletrônicos ocupados dos vazios. Isso implica que a reatividade e a condutividade do material são sutilmente moduladas ao carregar os fármacos, uma característica útil para futuras aplicações de detecção ou teranósticas. Crucialmente, quando simularam o ambiente mais ácido encontrado próximo a tumores adicionando prótons extras, a ligação calculada enfraqueceu e as distâncias de contato aumentaram. Em termos simples, as simulações sugerem que o CTF-2 pode segurar os fármacos em condições sanguíneas normais, mas tende a liberá‑los mais facilmente em ambientes ácidos semelhantes aos tumorais — exatamente o comportamento desejado para entrega direcionada.
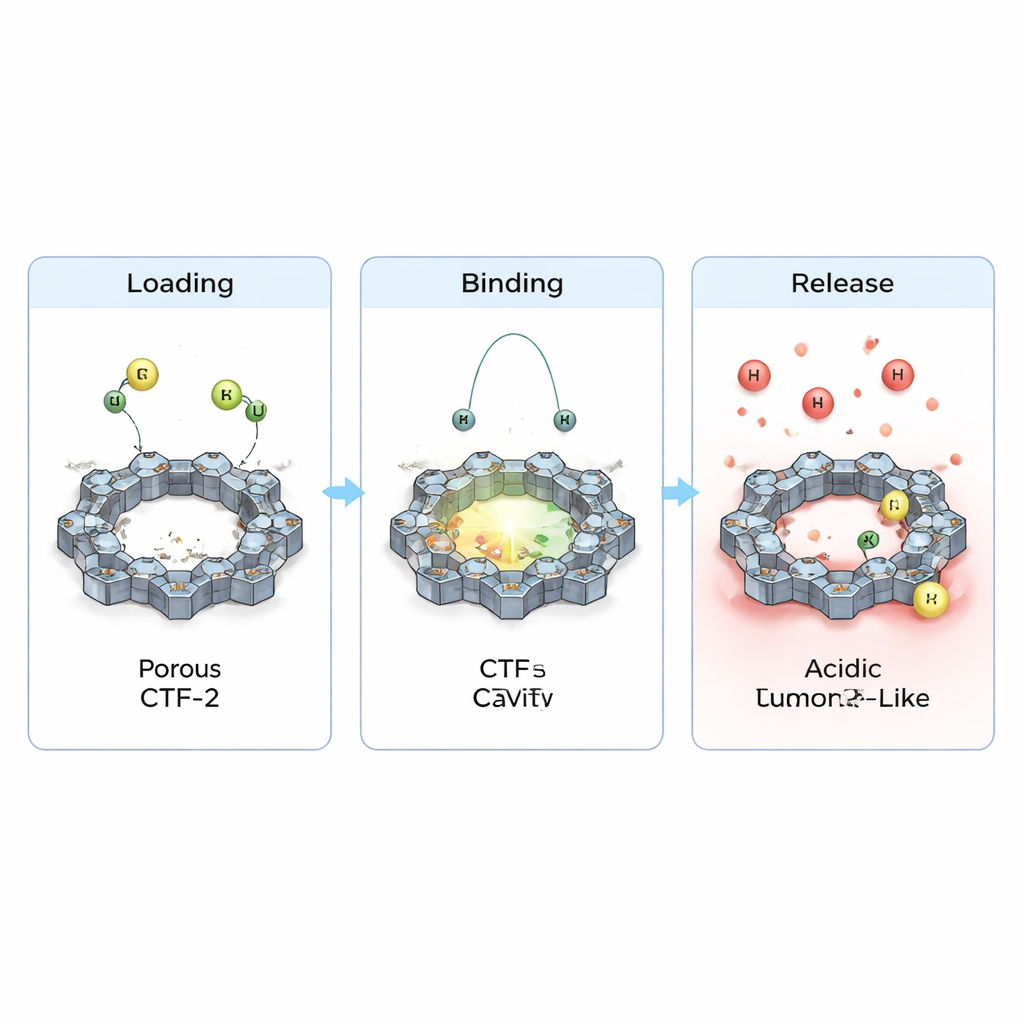
O que isso significa para tratamentos futuros do câncer
Em conjunto, esses cálculos pintam o CTF-2 como um transportador promissor para ciclofosfamida e purinethol: ele pode acomodá‑los em sua superfície porosa de maneira estável, protegê‑los durante a circulação e então liberá‑los quando a química local mudar ao redor de um tumor. Embora o trabalho seja teórico e precise de confirmação experimental, sugere que estruturas nitrogênio‑ricas finamente projetadas, como o CTF-2, poderiam ajudar a transformar medicamentos quimioterápicos antigos, porém eficazes, em fármacos mais inteligentes — entregando doses potentes onde são mais necessárias enquanto reduzem o dano colateral às células saudáveis.
Citação: Tariq, T., Yar, M., Bayach, I. et al. A density functional theory study of cyclophosphamide and purinethol adsorption on a covalent triazine framework (CTF-2) for drug delivery applications. Sci Rep 16, 6125 (2026). https://doi.org/10.1038/s41598-026-36405-5
Palavras-chave: nanotransportador, entrega de fármacos, quimioterapia contra o câncer, estrutura triazina covalente, modelagem computacional