Clear Sky Science · pt
Um framework interativo de aprendizado profundo em cascata com refinamento por especialista para segmentação precisa de sub-regiões do estriado
Por que mapear regiões cerebrais minúsculas é importante
O estriado, uma pequena estrutura enterrada no interior do cérebro, desempenha papel central no movimento e na motivação e é fortemente afetado em transtornos como a doença de Parkinson. Médicos frequentemente usam exames de PET e ressonância magnética para medir alterações químicas nessa área, mas o estriado é dividido em muitas sub-regiões diminutas que são difíceis de ver e delinear com precisão. Este artigo apresenta um novo método assistido por computador, chamado StriaSeg‑iARM, que ajuda especialistas a traçar esses limites de forma mais precisa e eficiente, mesmo em pessoas cujos cérebros estão alterados pelo envelhecimento ou por doenças.
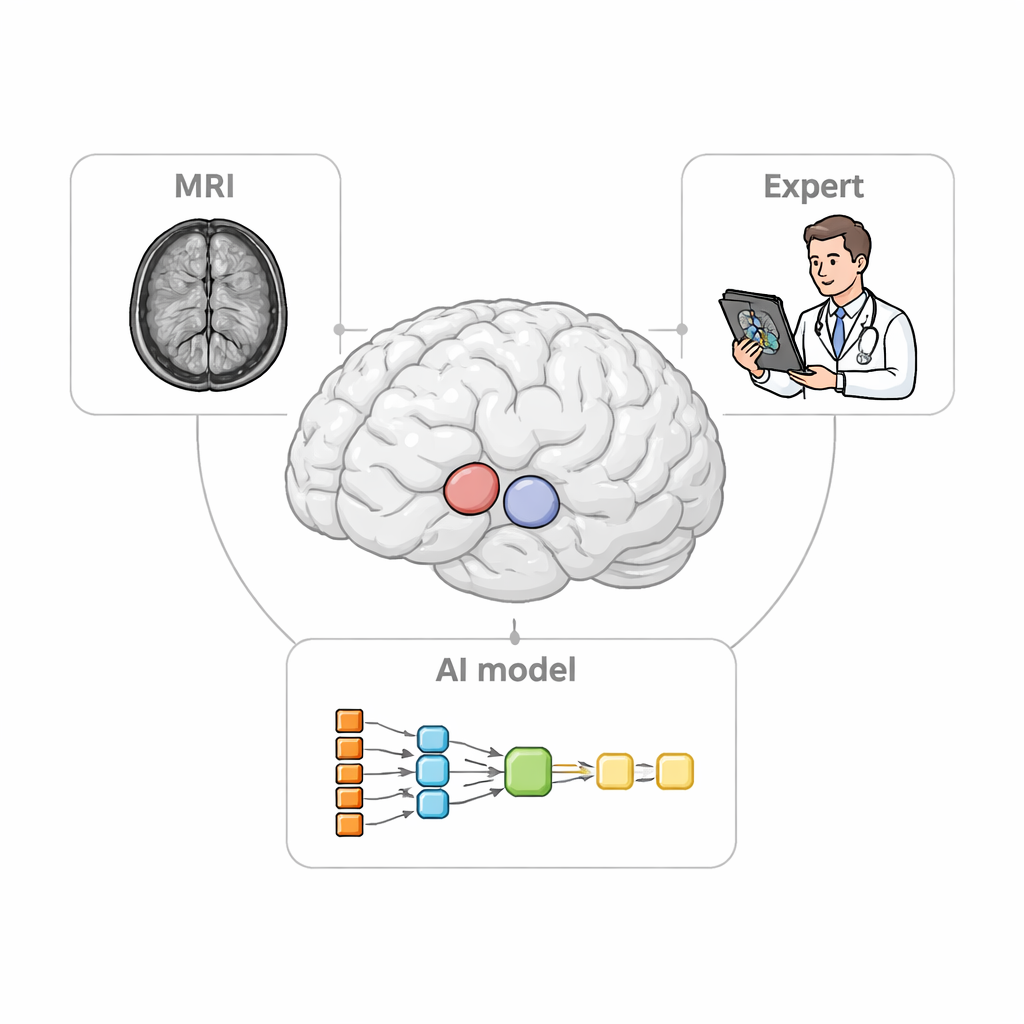
O problema clínico à vista de todos
Quando neurologistas avaliam condições como a doença de Parkinson, eles confiam em exames de PET para acompanhar como sinais relacionados à dopamina variam em diferentes partes do estriado. Para fazer isso corretamente, é preciso primeiro definir pequenas “regiões de interesse” tridimensionais na ressonância magnética, que servem como copos de medição para os dados de PET. Delinear manualmente essas regiões é um trabalho lento e tedioso e pode variar de um especialista para outro. Softwares existentes só conseguem localizar automaticamente as estruturas maiores e frequentemente têm dificuldades em pacientes cujos cérebros estão encolhidos ou distorcidos — uma situação comum em estágios avançados de doenças neurodegenerativas. Essas limitações podem borrar o padrão real de dano e enfraquecer o poder da imagem como ferramenta diagnóstica.
Um assistente mais inteligente em duas etapas
Os pesquisadores projetaram o StriaSeg‑iARM como um sistema de aprendizado profundo em duas etapas que opera diretamente no espaço cerebral de cada pessoa, em vez de forçar a imagem para um template padrão. Na primeira etapa, o programa localiza o estriado geral em uma ressonância magnética tridimensional. Na segunda etapa, divide essa estrutura em 12 sub-regiões definidas anatomicamente em ambos os lados do cérebro. Entre essas duas etapas reside a inovação-chave: um passo interativo no qual um especialista pode rapidamente checar e, se necessário, corrigir o contorno grosseiro produzido pela primeira etapa antes que a subdivisão mais fina seja executada. Essa abordagem combina a velocidade da automação com o julgamento de um observador humano treinado.
Treinamento e teste em cérebros do mundo real
Para ensinar o sistema a reconhecer o que procurar, a equipe reuniu centenas de exames de ressonância magnética de vários hospitais e tipos de aparelhos, e criou delineamentos manuais cuidadosos das 12 sub-regiões do estriado. Em seguida, testaram o modelo em dois conjuntos de dados externos que incluíam tanto RM quanto exames de PET relacionados à dopamina: um de pacientes com Parkinson relativamente no início e voluntários saudáveis, e outro de um grupo clínico mais idoso e mais gravemente afetado, com marcada atrofia cerebral e diagnósticos mistos. Nesses casos desafiadores, o StriaSeg‑iARM igualou consistentemente os traçados manuais dos especialistas melhor do que métodos tradicionais baseados em atlas e um modelo de aprendizado profundo de etapa única, apresentando maior sobreposição, contornos mais precisos e medidas de volume estáveis.
Medidas mais nítidas para exames de química cerebral
Como o objetivo final é quantificar sinais de PET, os autores também examinaram como diferentes métodos de segmentação afetaram as leituras de PET. Usando uma medida padrão de ligação do traçador em cada sub-região, compararam resultados automáticos com aqueles baseados em delineamentos manuais. O método baseado em atlas tendia a subestimar a ligação, especialmente em pacientes com alterações mais severas, enquanto o modelo profundo básico ainda mostrava viés perceptível em algumas regiões. Em contraste, os modelos em cascata — especialmente quando o passo de correção interativa era usado — produziram valores de PET que acompanharam de perto a referência dos especialistas, com viés e dispersão mínimos. A equipe demonstrou ainda que uma simples pontuação de incerteza da primeira etapa pode sinalizar cerca de um quarto dos casos mais difíceis onde o refinamento por especialista é realmente necessário, mantendo o restante totalmente automático.
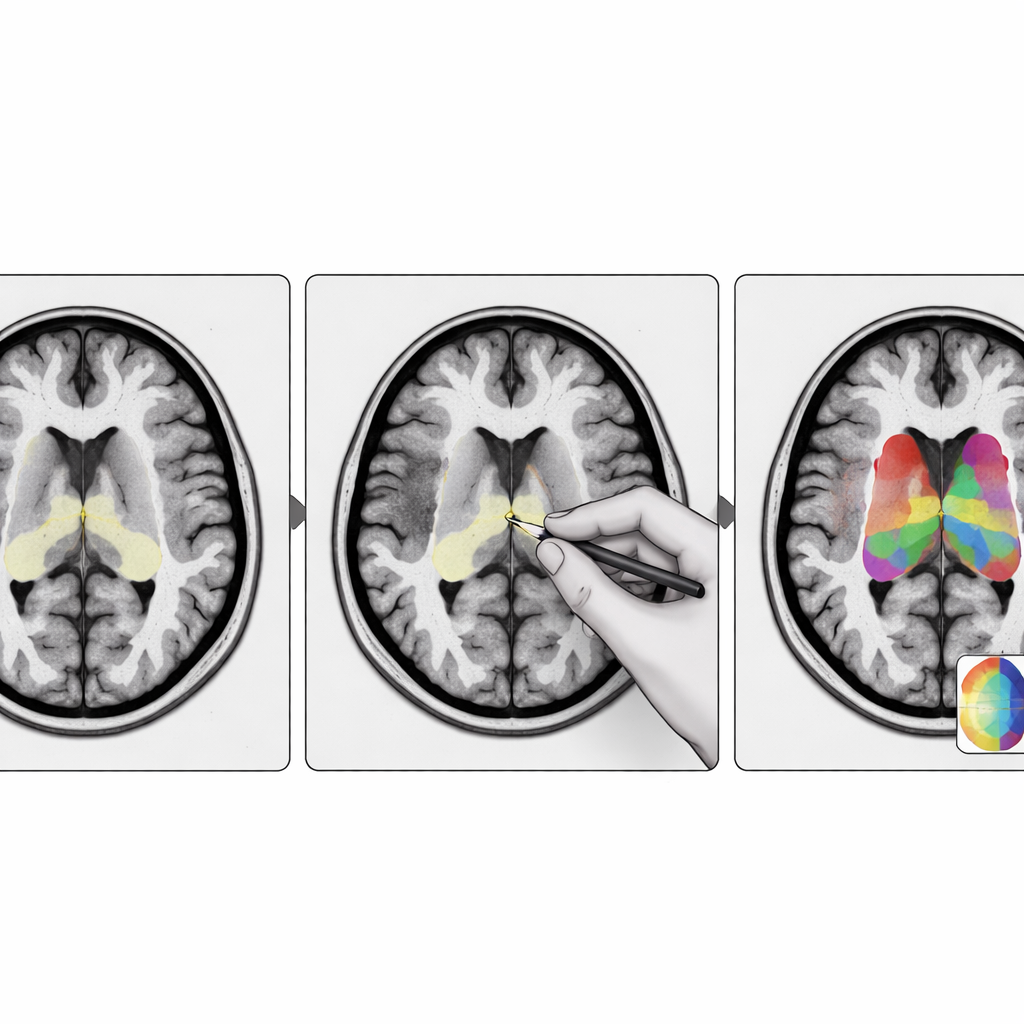
O que isso significa para pacientes e clínicos
Para não especialistas, a mensagem principal é que mapas digitais melhores de pequenas regiões cerebrais podem tornar exames químicos do cérebro mais confiáveis. O StriaSeg‑iARM fornece um framework flexível em que um modelo de aprendizado profundo faz a maior parte do trabalho, mas especialistas ainda podem intervir para corrigir casos difíceis sem precisar retrenar o sistema. Essa combinação de automação e supervisão especializada melhora a precisão das medidas usadas para diagnosticar e acompanhar distúrbios como a doença de Parkinson, e pode ser adaptada a outros órgãos e doenças onde estruturas pequenas e difíceis de ver guardam pistas vitais.
Citação: Kim, J., Kim, D., Kim, S. et al. An interactive cascaded deep learning framework with expert refinement for accurate striatal subregion segmentation. Sci Rep 16, 6550 (2026). https://doi.org/10.1038/s41598-026-36399-0
Palavras-chave: imagem na doença de Parkinson, segmentação do estriado, aprendizado profundo em radiologia, TAC PET e ressonância magnética cerebral, biomarcadores de doenças neurodegenerativas