Clear Sky Science · pt
Papel das modificações de histonas mediadas por MNX1 e da família de genes PBX na leukemogênese induzida por MNX1
Por que uma pequena falha genética importa para crianças doentes
A maioria das leucemias infantis hoje é tratável, mas uma forma rara chamada leucemia mieloide aguda (LMA) em lactentes continua especialmente letal. Muitos desses bebês compartilham o mesmo acidente genético: duas cromossomos trocam pedaços, transformando um gene silencioso do desenvolvimento chamado MNX1 em um motor hiperativo. Este estudo faz uma pergunta simples, porém crucial: uma vez que MNX1 é ativado, o que ele realmente faz dentro das células sanguíneas jovens para empurrá‑las na direção do câncer — e esse processo pode ser interrompido?
De células sanguíneas normais de bebês ao crescimento descontrolado
A leucemia surge quando células sanguíneas imaturas deixam de amadurecer e começam a se multiplicar descontroladamente. Em lactentes portadores da troca cromossômica t(7;12), o MNX1 torna‑se anormalmente ativo em células formadoras de sangue muito precoces encontradas no fígado fetal e na medula óssea. Os pesquisadores construíram um modelo de camundongo que imita essa situação: ativaram o MNX1 humano em células‑tronco sanguíneas fetais, transplantaram‑nas em camundongos e observaram a progressão dos animais de um estado pré‑leucêmico até leucemia plena. Ao comparar células nesses diferentes estágios com controles saudáveis, puderam traçar como o MNX1 reprograma os sistemas de controle internos da célula ao longo do tempo.
Como MNX1 reescreve o manual de instruções da célula
MNX1 é um fator de transcrição, uma proteína que se liga ao DNA e controla quais genes são ligados ou desligados. A equipe combinou vários métodos poderosos — espectrometria de massas, sequenciamento de RNA e perfilamento de cromatina — para ver com quais parceiros MNX1 trabalha e quais genes ele altera. Eles descobriram que o MNX1 se associa a enzimas que adicionam marcas químicas às proteínas histonas, as estruturas em forma de carretel ao redor das quais o DNA se enrola. Em particular, o MNX1 aumenta uma marca de “LIGADO” chamada H3K4me3 e reduz uma marca de “DESLIGADO” chamada H3K27me3 em pontos específicos do genoma. Essas mudanças afrouxam a estrutura local do DNA e facilitam que genes-chave relacionados ao crescimento sejam ativados.
Um impulso 'acende‑e‑vai' em um gene de controle crítico
Entre muitos genes afetados, um se destacou: Pbx1, parte da família PBX de proteínas que se ligam ao DNA e que há muito tempo estão associadas à leucemia. O estudo mostra que MNX1 se liga diretamente à região de controle do gene Pbx1, aumentando a marca de LIGADO e removendo a marca de DESLIGADO ali. Isso impulsiona a expressão de Pbx1 muito cedo, quando as células ainda estão apenas pré‑leucêmicas. Surpreendentemente, mais tarde — uma vez que a leucemia está estabelecida — o próprio MNX1 não está mais fortemente ligado naquele local, porém o gene Pbx1 continua ligado e suas marcas de histona permanecem na configuração pró‑crescimento. Isso sugere um mecanismo de “acende‑e‑vai”: o MNX1 visita brevemente regiões-chave da cromatina, deixa marcas epigenéticas duráveis e pode então se afastar enquanto o estado alterado continua alimentando a doença.
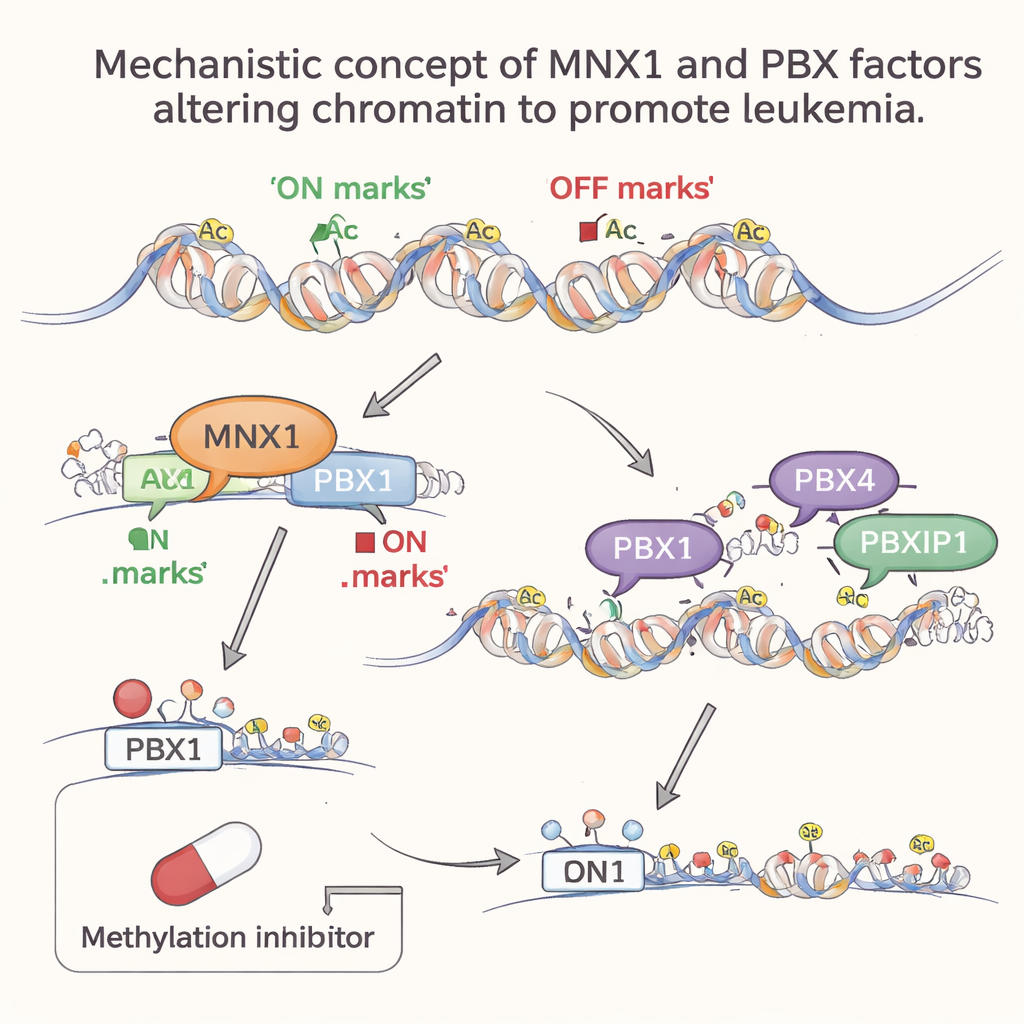
Auxiliares posteriores entram para consolidar o estado canceroso
À medida que a leucemia progride, outros membros da família PBX, PBX4 e PBXIP1, tornam‑se mais ativos, mas apenas nessa fase posterior. Análises em todo o genoma mostraram que os motivos de DNA preferidos por eles estão fortemente enriquecidos em regiões de cromatina aberta e ativa que foram remodeladas na esteira da atividade do MNX1. Em outras palavras, o MNX1 primeiro remodela o cenário da cromatina e ativa Pbx1; então PBX4 e PBXIP1 ocupam essas regiões recém‑acessíveis para reforçar programas gênicos anormais que promovem a divisão celular, bloqueiam o desenvolvimento sanguíneo normal e prejudicam a reparação do DNA. Esse envolvimento em etapas sugere uma divisão de tarefas: o PBX1 atua como um interruptor inicial dependente de MNX1, enquanto PBX4 e PBXIP1 ajudam a manter o programa leucêmico.
Bloqueando as marcas químicas que alimentam a leucemia
Como o MNX1 age por meio de enzimas que adicionam grupos metil às histonas, a equipe testou se um inibidor amplo de metiltransferases, a Sinefungina, podia interromper essa cadeia de eventos. Em células sanguíneas fetais pré‑leucêmicas que expressavam MNX1, a Sinefungina reduziu fortemente os níveis de Pbx1, compatível com o bloqueio da metilação específica do promotor da qual o MNX1 depende. Em contraste, os níveis de PBX4 e PBXIP1 mudaram muito pouco, condizendo com sua ativação posterior e indireta durante a progressão da doença. Em conjunto, esses resultados sustentam a ideia de que a LMA infantil com t(7;12) é impulsionada não apenas por um gene defeituoso, mas por uma cascata de alterações epigenéticas duráveis que o MNX1 desencadeia.
O que isso significa para tratamentos futuros
Para não especialistas, a mensagem principal é que este estudo mapeia uma reação em cadeia: um gene MNX1 hiperativo reconfigura as marcas químicas nas proteínas que empacotam o DNA, ativa PBX1 cedo e abre caminho para que PBX4 e PBXIP1 ajudem a trancar as células em um estado leucêmico. Como essas etapas dependem de padrões específicos de metilação de histonas, elas oferecem alvos claros e testáveis para drogas que interferem nessas marcas. A longo prazo, terapias direcionadas ao eixo MNX1–PBX ou às enzimas que colocam essas etiquetas epigenéticas podem ajudar a desligar as instruções defeituosas que impulsionam essa leucemia agressiva em lactentes, aumentando as chances de curas duradouras.
Citação: Malmhäll-Bah, E., Östlund, A., Nilsson, T. et al. Role of MNX1-mediated histone modifications and PBX gene family in MNX1-induced leukemogenesis. Sci Rep 16, 2593 (2026). https://doi.org/10.1038/s41598-026-36367-8
Palavras-chave: leucemia mieloide aguda infantil, MNX1, PBX1 PBX4 PBXIP1, metilação epigenética de histonas, translocação cromossômica t(7;12)