Clear Sky Science · pt
Redução da CDC25C suprime o crescimento do CHC via autofagia e apoptose induzidas por estresse mitocondrial
Por que este estudo sobre câncer de fígado importa
O câncer de fígado é um dos tipos mais letais no mundo, e muitos pacientes são diagnosticados tardiamente, quando cirurgia ou tratamentos padrão têm eficácia limitada. Este trabalho investiga um único “interruptor” celular — uma proteína chamada CDC25C — que parece impulsionar o crescimento do câncer hepático enquanto é menos crítica para células hepáticas saudáveis. Ao reduzir essa chave, os pesquisadores observaram que conseguem estressar e, por fim, eliminar as células tumorais por meio dos próprios sistemas de autolimpeza e autodestruição da célula, apontando para uma estratégia terapêutica promissora e mais seletiva.
Um interruptor de crescimento dentro dos tumores hepáticos
Toda célula precisa decidir quando se dividir e quando parar. A CDC25C é uma das proteínas-chave que impulsionam as células pelo ciclo de divisão. No câncer de fígado, esse interruptor frequentemente fica preso na posição “ligada”, ajudando os tumores a crescer e se espalhar. A equipe usou células de câncer de fígado de camundongo e células hepáticas normais de camundongo, bem como camundongos portadores de tumor, para reduzir artificialmente os níveis de CDC25C. Eles confirmaram, por testes genéticos e proteicos padrão, que a CDC25C foi fortemente reduzida no grupo experimental em comparação com os controles, estabelecendo um modelo sólido para estudar o que acontece quando esse interruptor de crescimento é diminuído.
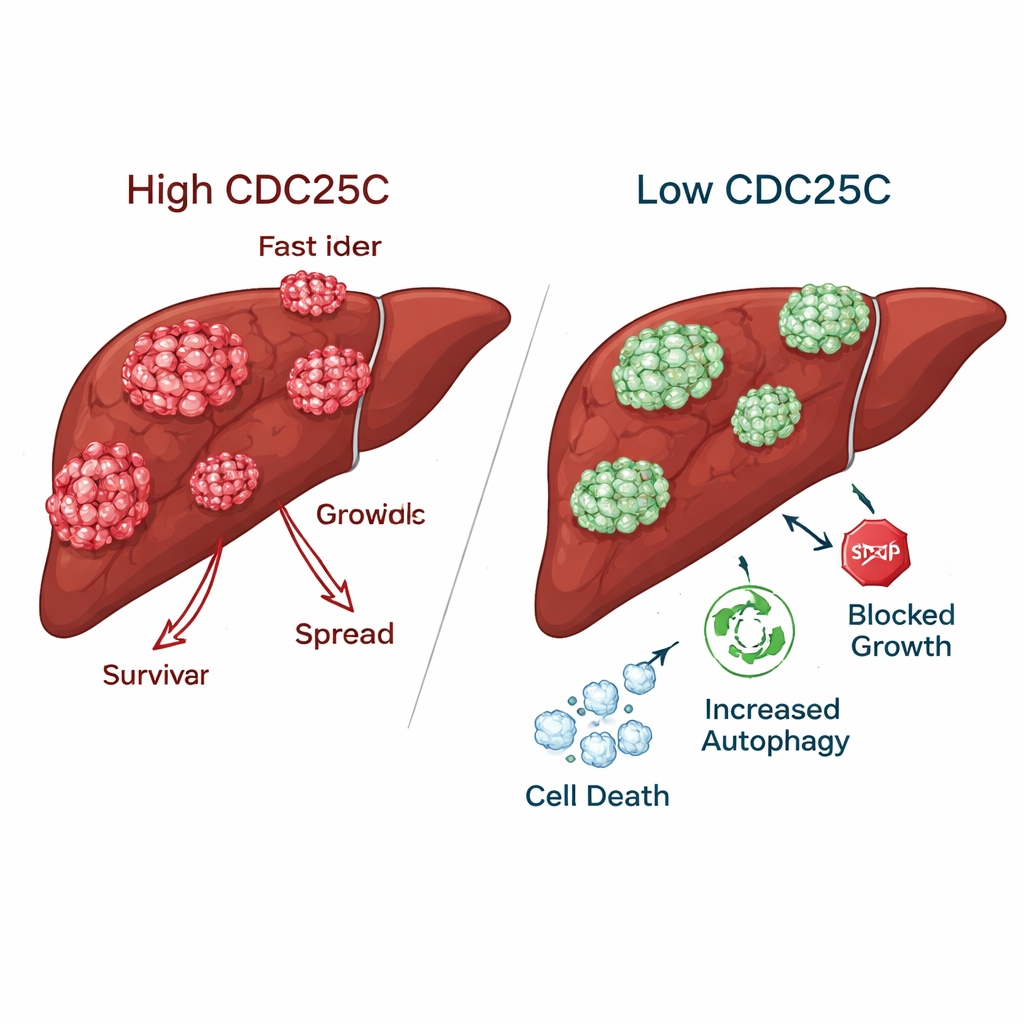
Freando o câncer sem prejudicar as células hepáticas saudáveis
Quando a CDC25C foi reduzida em células de câncer hepático, os tumores perderam muitas de suas características agressivas. As células cancerosas formaram muito menos colônias, migraram mais lentamente em “feridas” artificiais e foram menos capazes de atravessar e invadir barreiras em testes laboratoriais. Em contraste, células hepáticas normais mostraram crescimento e movimento melhores quando a CDC25C foi diminuída, sugerindo que o tecido saudável pode tolerar ou até se beneficiar da inibição da CDC25C. Em camundongos, tumores manipulados para reduzir CDC25C apresentaram níveis inferiores dessa proteína tanto em medidas de gene quanto de proteína, confirmando que o mesmo efeito ocorreu em animais vivos.
Estresse das usinas e a equipe de limpeza da célula
Ao observar as células com microscopia eletrônica, os pesquisadores viram que células cancerosas com baixa CDC25C continham mitocôndrias inchadas e danificadas — as pequenas usinas de energia da célula — juntamente com estruturas em forma de bolha chamadas autofagossomos, que indicam ativação do sistema interno de reciclagem celular, a autofagia. Em seguida, mediram sinais-chave de estresse mitocondrial: níveis de cálcio e espécies reativas de oxigênio (ROS), ambos aumentados em células cancerosas após a redução da CDC25C. Marcadores da resposta ao estresse mitocondrial, incluindo proteínas auxiliares como HSP60 e duas enzimas mitocondriais de “controle de qualidade”, também aumentaram, assim como CHOP, um fator relacionado ao estresse que conecta problemas mitocondriais a respostas celulares mais amplas. De forma marcante, esses sinais de estresse seguiram a direção oposta em células hepáticas normais, reforçando a ideia de que células cancerosas e saudáveis respondem de maneiras muito diferentes à perda de CDC25C.
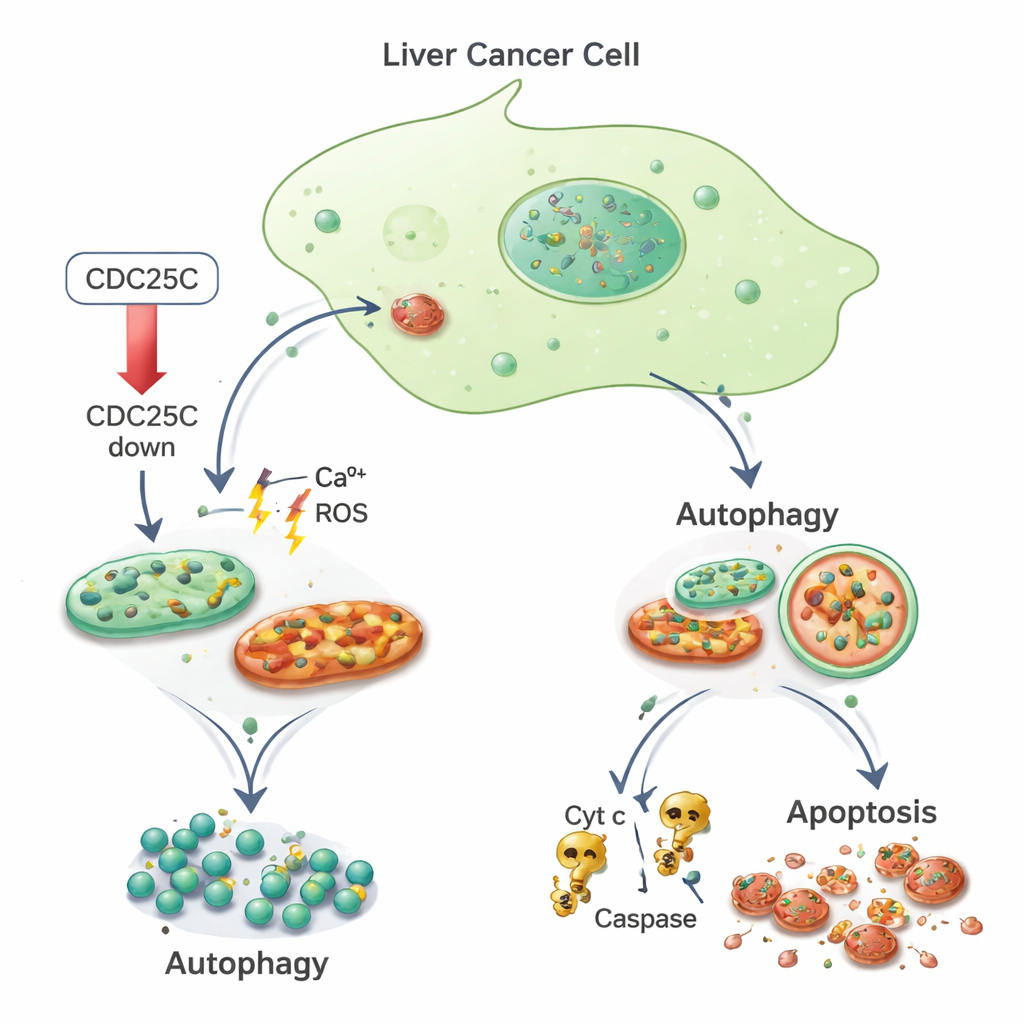
Do estresse à autodigestão e morte celular
A equipe perguntou em seguida como essas células cancerosas estressadas estavam lidando com a situação. Eles descobriram que marcadores de autofagia aumentaram tanto em células cancerosas quanto em células hepáticas normais quando a CDC25C foi reduzida. Proteínas como LC3 e p62, que refletem a formação e atividade dos autofagossomos, aumentaram, indicando que as células estavam reforçando sua maquinaria de limpeza. Ao mesmo tempo, apenas nas células cancerosas, o dano mitocondrial parece empurrar as células além do reparo e rumo à morte celular programada. Usando colorações fluorescentes e citometria de fluxo, os pesquisadores observaram mais células cancerosas com núcleos fragmentados e intensamente corados — uma marca da apoptose — e redução do potencial de membrana mitocondrial. Eles também encontraram níveis aumentados de citocromo c e das enzimas Caspase-3 e Caspase-9, componentes clássicos da via de morte conduzida pelas mitocôndrias. Células hepáticas normais, por sua vez, apresentaram menos apoptose sob as mesmas condições de redução da CDC25C.
O que isso pode significar para tratamentos futuros
Para um leitor leigo, a mensagem principal é que diminuir a CDC25C parece atingir as células do câncer de fígado em sua vulnerabilidade: sobrecarregando suas usinas de energia, forçando seus sistemas de reciclagem a operar em excesso e, finalmente, desencadeando uma autodestruição ordenada — ao mesmo tempo em que poupa, em grande parte, as células hepáticas normais. Os autores concluem que a CDC25C é mais do que um simples interruptor de crescimento; ela também molda como as células lidam com estresse, limpeza e morte. Como as células cancerosas dependem fortemente da CDC25C e respondem à sua perda com estresse mitocondrial fatal e apoptose, fármacos que visem essa proteína, ou suas vias de estresse a jusante, podem um dia oferecer uma forma mais seletiva de tratar o câncer de fígado com menos danos ao tecido hepático saudável.
Citação: Miao, X., Zheng, F., Mo, X. et al. CDC25C downregulation suppresses HCC growth via mitochondrial stress-induced autophagy and apoptosis. Sci Rep 16, 5631 (2026). https://doi.org/10.1038/s41598-026-36351-2
Palavras-chave: carcinoma hepatocelular, CDC25C, estresse mitocondrial, autofagia, apoptose