Clear Sky Science · pt
TET1 suprime a progressão do carcinoma hepatocelular ao modular as vias de sinalização PI3K/Akt
Por que uma enzima hepática importa para o câncer
O câncer primário de fígado, especialmente um tipo chamado carcinoma hepatocelular, está entre os cânceres mais letais no mundo. Muitos pacientes são diagnosticados tarde demais para cirurgia curativa, e os medicamentos disponíveis beneficiam apenas uma fração deles. Este estudo investiga uma molécula chamada TET1, uma enzima que edita marcas químicas no DNA, para responder a uma pergunta simples, porém vital: o TET1 ajuda os tumores hepáticos a crescer, e poderia se tornar um novo alvo para tratamento?
Um editor oculto em nosso DNA
Nossos genes são controlados não apenas pelo código do DNA em si, mas também por marcas químicas que ligam ou desligam genes. Uma marca comum é a metilação do DNA, que funciona como um dimmer na atividade gênica. O TET1 faz parte de uma família de enzimas que apagam ou remodelam essas marcas, ajudando as células a responder ao ambiente e a manter o funcionamento normal. Quando esse sistema falha, as células podem deslizar para estados patológicos, incluindo o câncer. Pesquisas anteriores mostraram que o TET1 pode tanto frear quanto acelerar o crescimento tumoral dependendo do tecido, mas seu papel exato no câncer hepático humano permanecia incerto e bastante debatido.
Os níveis de TET1 disparam em tumores hepáticos
Para descobrir o que o TET1 faz no câncer de fígado, os pesquisadores primeiro recorreram a grandes bancos públicos de genes e depois a amostras de pacientes. Em vários tipos de câncer, os níveis de TET1 foram incomumente altos em diversos tumores, incluindo o de fígado. Focando nos tumores hepáticos, eles compararam tecido tumoral com fígado não canceroso adjacente dos mesmos pacientes. Em oito pares pareados, a proteína TET1 foi consistentemente mais alta no tumor. Conjuntos de dados públicos de centenas de pacientes contaram a mesma história ao nível de RNA: os cânceres de fígado tinham mais TET1 do que fígados saudáveis ou fígados apenas com fibrose. Pacientes cujos tumores apresentavam TET1 mais alto tenderam a ter doença mais avançada e sobrevida global e livre de doença mais curtas, sugerindo que o TET1 está ligado tanto à agressividade tumoral quanto a um prognóstico pobre.
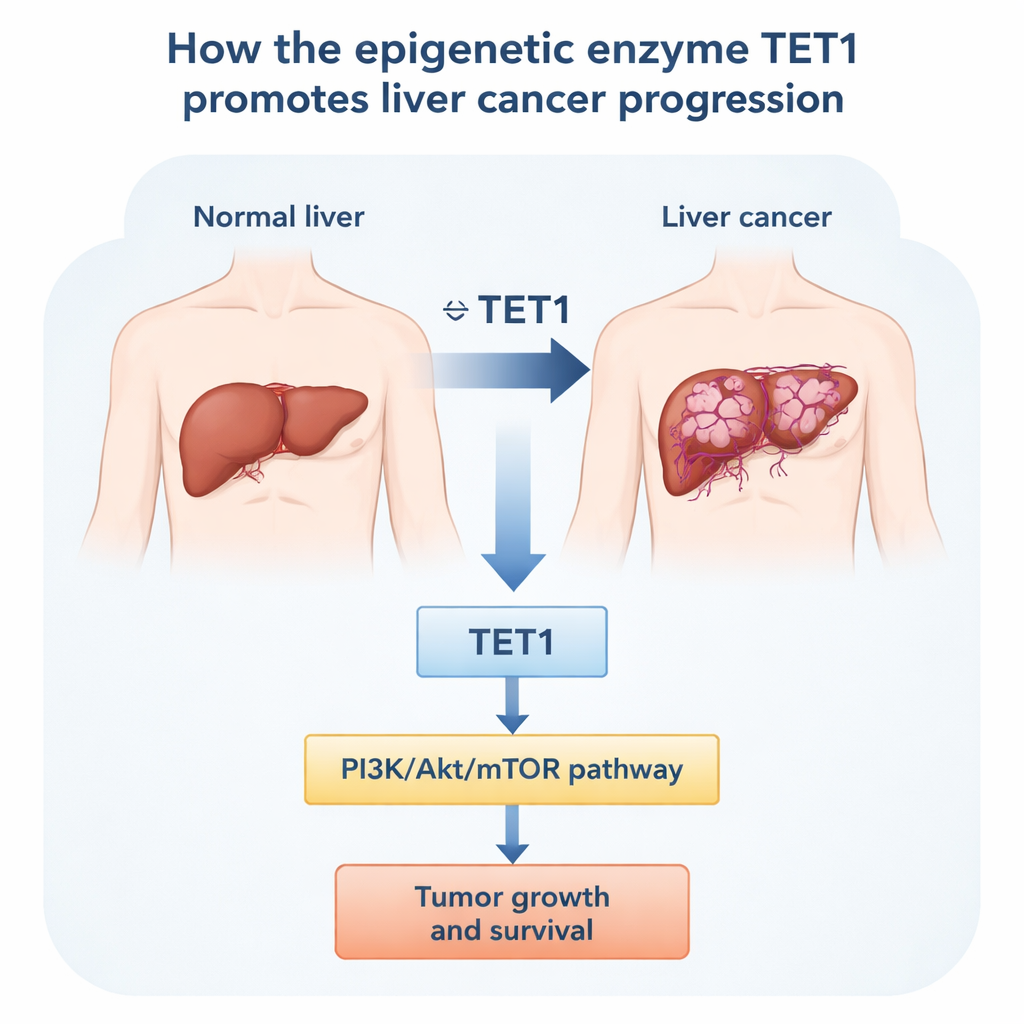
Reduzir o TET1 desacelera as células tumorais
Em seguida, a equipe perguntou o que ocorre quando o TET1 é reduzido dentro de células de câncer hepático cultivadas em laboratório. Usando pequenos fragmentos de RNA para silenciar o gene TET1, eles diminuíram dramaticamente os níveis de TET1 em várias linhagens humanas de câncer de fígado, inclusive emquelas com alterações relacionadas ao vírus da hepatite B. Uma vez suprimido o TET1, as células se dividiram mais lentamente, formaram menos colônias e exibiram sinais claros de estresse. Experimentos de citometria de fluxo revelaram que mais células ficaram retidas na fase inicial “G1” do ciclo celular, em vez de avançar para a divisão. Ao mesmo tempo, a fração de células passando por morte programada, ou apoptose, aumentou fortemente. Esses efeitos apareceram tanto em células típicas de câncer hepático quanto em uma linhagem positiva para HBV, indicando que o TET1 ajuda a sustentar a sobrevivência e o crescimento contínuo em diferentes contextos do câncer de fígado.
Uma via de crescimento sob o controle do TET1
Para descobrir como o TET1 exerce essa influência, os pesquisadores mapearam quais genes mudavam entre células hepáticas normais e células tumorais. Milhares de genes foram diferentes, e muitos deles se agruparam em circuitos bem conhecidos de crescimento e sobrevivência. Uma via se destacou: PI3K/Akt/mTOR, uma cadeia de sinalização central que muitos cânceres usam para aumentar o metabolismo, resistir à morte celular e tolerar terapias. Análises de banco de dados mostraram que os níveis de TET1 subiam em conjunto com componentes centrais dessa via e caiam em oposição à PTEN, um freio natural sobre a atividade PI3K/Akt. Quando o TET1 foi silenciado em células de câncer hepático, as formas ativadas, “fosforiladas”, de PI3K, Akt e especialmente mTOR diminuíram. Tratar as células com um inibidor químico que bloqueia a atividade da família TET reduziu igualmente a fosforilação de Akt e mTOR. Esses resultados sugerem que a atividade enzimática do TET1 — sua capacidade de remodelar marcas no DNA — alimenta a cascata PI3K/Akt/mTOR, inclinando o balanço em favor do crescimento e da sobrevivência em vez da contenção.
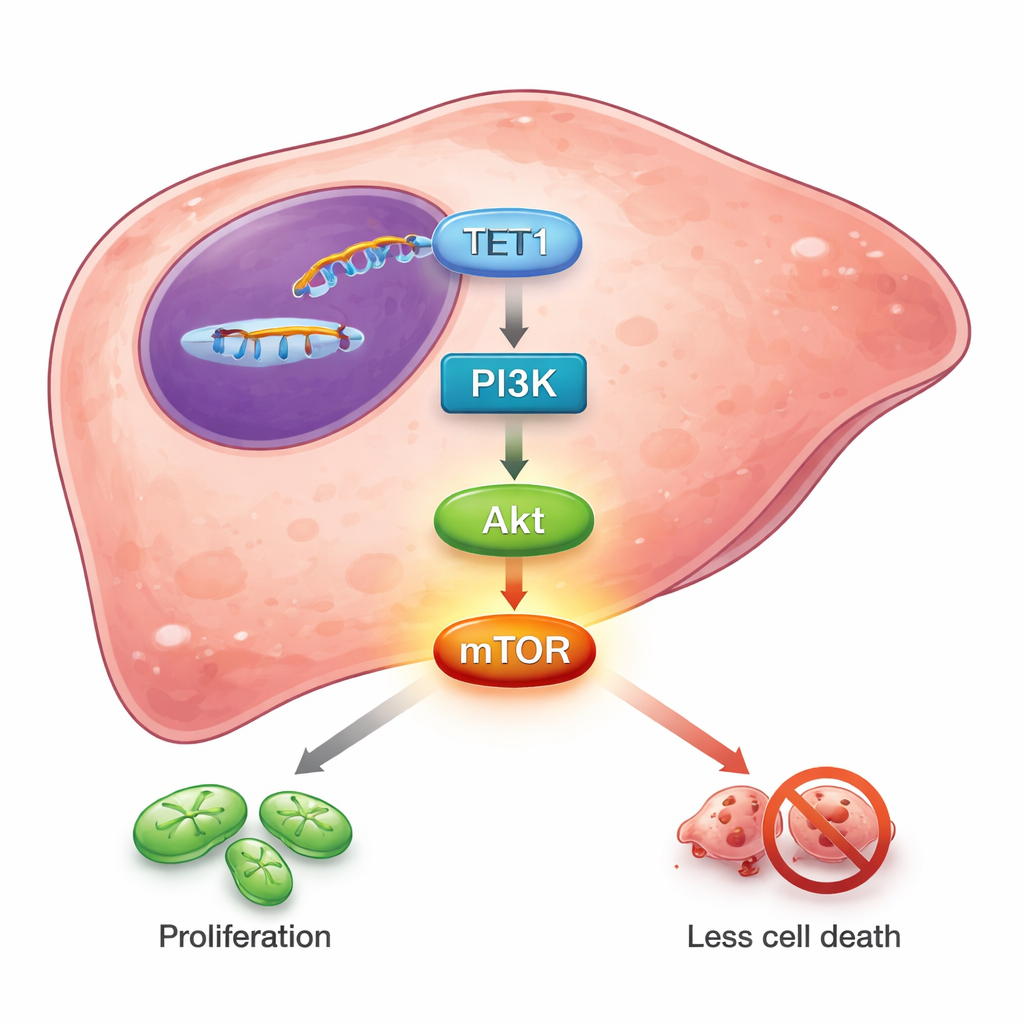
Do insight molecular a possíveis tratamentos
No conjunto, este trabalho pinta o TET1 como um aliado chave dos tumores hepáticos em vez de um guardião contra eles. TET1 elevado ajuda as células do câncer de fígado a proliferar e escapar da morte, em parte ao manter a via PI3K/Akt/mTOR ativada. Em pacientes, mais TET1 nos tumores anda de mãos dadas com doença mais avançada e piores desfechos. Para o leitor leigo, a mensagem é que uma enzima que edita silenciosamente marcas químicas no DNA pode influenciar fortemente se as células do câncer de fígado vivem ou morrem. Ao projetar drogas que inibam o TET1, ou ao combinar tais fármacos com terapias já direcionadas à via PI3K/Akt, tratamentos futuros podem conseguir cortar uma linha de suporte crucial para tumores hepáticos e melhorar a sobrevida de pessoas com essa doença desafiadora.
Citação: Qi, S., Chen, M., Ding, Z. et al. TET1 suppresses hepatocellular carcinoma progression by modulating the PI3K/Akt signaling pathways. Sci Rep 16, 5791 (2026). https://doi.org/10.1038/s41598-026-36334-3
Palavras-chave: câncer de fígado, TET1, epigenética, PI3K Akt mTOR, carcinoma hepatocelular