Clear Sky Science · pt
Superando a resistência de biofilme de Candida albicans a medicamentos via sinergia azol‑soforolipídio
Por que infecções fúngicas persistentes importam
Qualquer pessoa que já teve uma infecção por fungos persistente, um cateter central no hospital ou um implante médico está potencialmente em risco por Candida albicans, um fungo comum que pode se tornar perigoso quando forma comunidades difíceis de tratar chamadas biofilmes. Essas camadas viscosas protegem os microrganismos de muitos dos nossos melhores antifúngicos, permitindo que as infecções persistam e às vezes se tornem potencialmente fatais. O estudo descrito aqui busca uma nova forma de romper essas defesas, combinando medicamentos existentes com uma molécula natural semelhante a sabão produzida por leveduras.
Um escudo oculto em superfícies médicas
Candida albicans pode aderir a tecidos e dispositivos médicos e então se desenvolver em biofilmes estruturados — camadas densas de células mantidas por uma matriz autogerada de açúcares, proteínas e DNA. Dentro dessa fortaleza, o fungo reduz seu metabolismo e bombeia os medicamentos de volta para fora, de modo que fármacos que matam facilmente células livres têm pouco efeito sobre as que residem no biofilme. Drogas azóis como fluconazol e itraconazol são pilares da terapia antifúngica, mas contra biofilmes maduros frequentemente requerem doses muito mais altas, o que pode causar efeitos colaterais e ainda assim falhar em eliminar totalmente a infecção. Clínicos lidam cada vez mais com infecções que são simultaneamente baseadas em biofilme e resistentes, ressaltando a necessidade de moléculas auxiliares que possam enfraquecer o próprio biofilme.
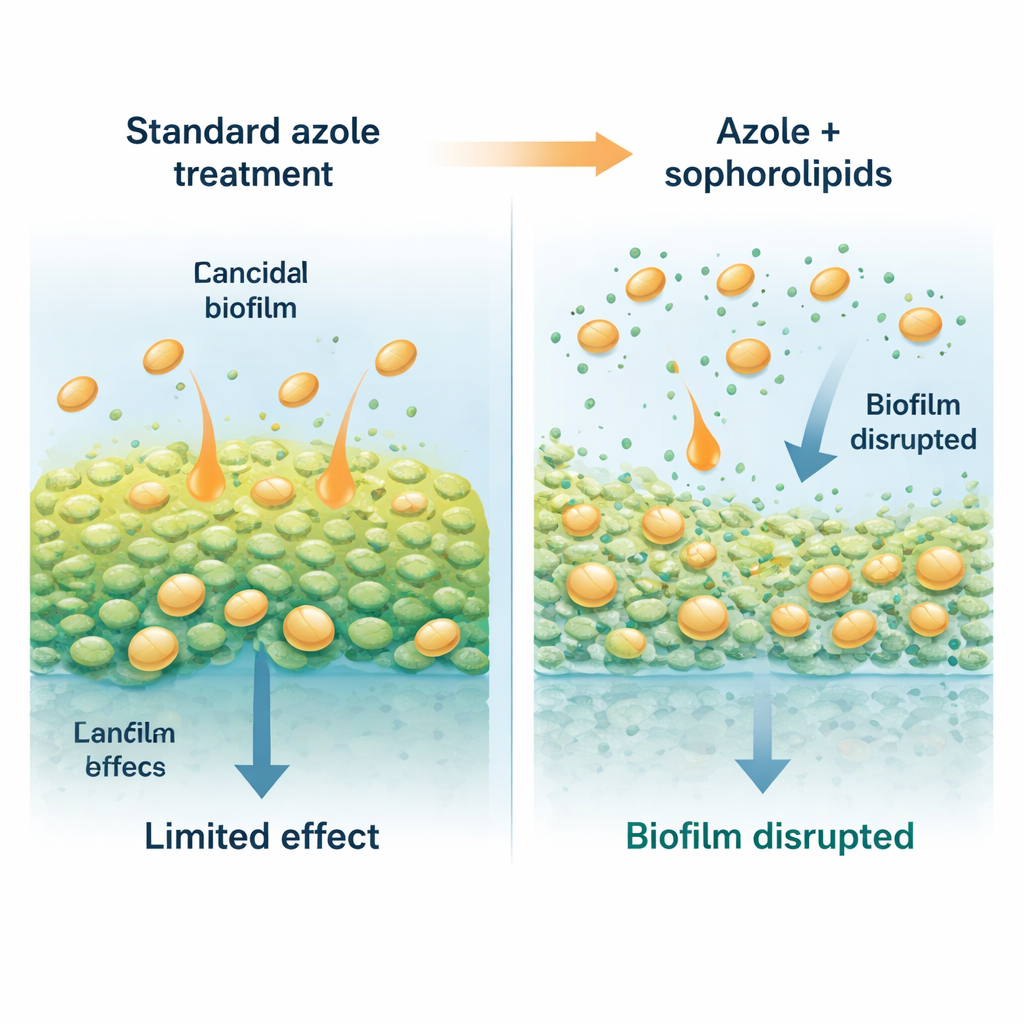
Auxiliares semelhantes a sabão de uma levedura benigna
Os pesquisadores recorreram aos soforolipídios, surfactantes naturais e biodegradáveis — moléculas que se comportam como detergentes muito suaves — produzidos por certas leveduras não patogênicas. Essas moléculas têm uma cabeça açucarada hidrofílica e uma cauda oleosa, permitindo que se posicionem em superfícies e interfacies. Neste estudo, usou‑se uma levedura chamada Starmerella riodocensis para produzir uma mistura de soforolipídios, que foi então purificada e analisada. Por si só, esses soforolipídios não mataram células de Candida em suspensão, mesmo em doses elevadas, mas interferiram fortemente na capacidade do fungo de formar e manter biofilmes. Biofilmes jovens, em formação, foram especialmente sensíveis, e até biofilmes estabelecidos de 24 horas puderam ser afinados e enfraquecidos quando expostos aos soforolipídios purificados.
Juntando forças com antifúngicos existentes
A questão central era se os soforolipídios poderiam melhorar a ação dos azóis padrão. A equipe testou combinações de soforolipídios com três azóis amplamente usados: fluconazol, itraconazol e cetoconazol. Quando expuseram biofilmes a essas misturas, descobriram que alguns pares fizeram mais do que simplesmente somar seus efeitos — agiram de forma sinérgica, isto é, a combinação foi mais potente do que se esperaria de cada componente isoladamente. A parceria de maior destaque foi itraconazol mais soforolipídios. Contra biofilmes difíceis e pré‑formados, a quantidade de itraconazol necessária para reduzir o biofilme pela metade caiu em até dezesseis vezes, enquanto a dose necessária de soforolipídio também diminuiu várias vezes em comparação ao uso isolado dos soforolipídios. As combinações com fluconazol e cetoconazol mostraram ganhos mais modestos, sugerindo que a natureza química de cada fármaco influencia o quanto ele se beneficia do "auxílio" do surfactante.
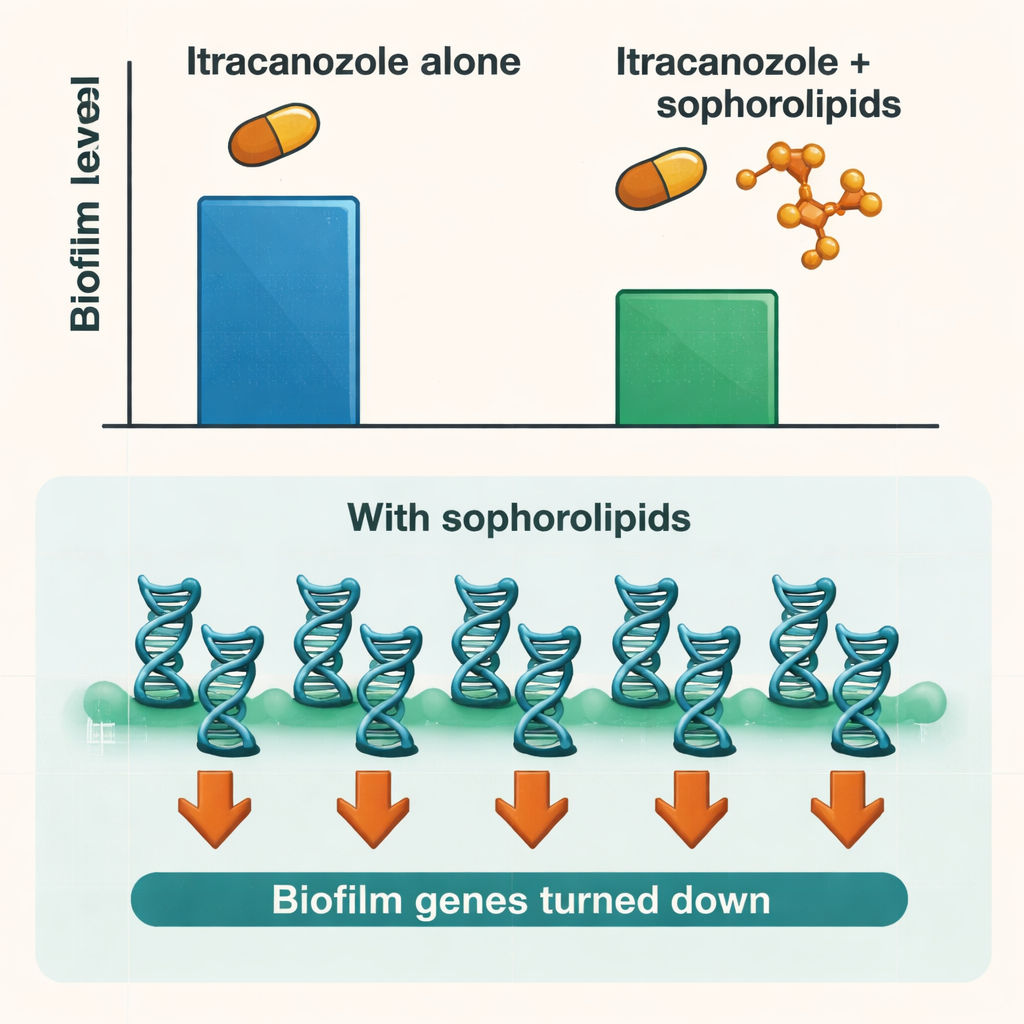
Silenciando o programa de biofilme do fungo
Para entender o que ocorria dentro das células fúngicas, os pesquisadores examinaram a atividade de genes-chave de Candida envolvidos na adesão a superfícies, no crescimento filamentoso e na construção da matriz do biofilme. O tratamento apenas com soforolipídios reduziu a expressão de muitos desses genes, especialmente os que controlam os passos iniciais de adesão e a transição de formas em levedura para formas filamentosas. Quando as células foram sincronizadas em uma fase específica do ciclo celular que favorece a formação de biofilme, os efeitos de silenciamento gênico foram ainda mais fortes. Isso sugere que os soforolipídios não simplesmente removem o biofilme; eles também perturbam o próprio programa biológico do fungo para construir e manter sua comunidade protetora.
Promessa de tratamentos mais suaves e eficazes
O estudo conclui que os soforolipídios de Starmerella riodocensis podem atuar como parceiros seguros e direcionados ao biofilme para os azóis, com a combinação itraconazol–soforolipídio sendo especialmente potente. Como os soforolipídios apresentam baixa toxicidade em células de mamíferos e enfraquecem principalmente a estrutura do biofilme e as redes gênicas em vez de envenenar diretamente o fungo, eles podem permitir que médicos usem doses menores de medicamentos convencionais enquanto ainda eliminam infecções persistentes em dispositivos e tecidos. Para os pacientes, esse tipo de terapia combinada inteligente pode, no futuro, traduzir-se em tratamentos que sejam ao mesmo tempo mais eficazes contra biofilmes resistentes de Candida e mais gentis com o resto do corpo.
Citação: Jayasekara, L.C.B., Watchaputi, K., Butkinaree, C. et al. Overcoming Candida albicans biofilm drug resistance via azole-sophorolipid synergy. Sci Rep 16, 5963 (2026). https://doi.org/10.1038/s41598-026-36278-8
Palavras-chave: biofilme de Candida, antifúngicos azóis, soforolipídios, sinergia de medicamentos, resistência antimicrobiana