Clear Sky Science · pt
Segmentação fraca de glândulas colorretais por aprendizado auto-supervisionado e pseudo-rotulagem baseada em atenção
Por que isso importa para o diagnóstico do câncer
Quando um patologista analisa uma biópsia de cólon ao microscópio, uma das pistas mais importantes sobre a gravidade do câncer é a forma e a organização de estruturas minúsculas em forma de tubo chamadas glândulas. Contornar cada glândula manualmente é lento, caro e difícil de padronizar entre hospitais. Este estudo mostra como a inteligência artificial pode aprender a traçar essas glândulas quase tão bem quanto especialistas humanos enquanto usa rótulos humanos muito menos detalhados, potencialmente acelerando e aprimorando o diagnóstico do câncer colorretal.
O desafio de desenhar cada contorno minúsculo
O câncer colorretal está entre os tipos mais comuns e letais no mundo, e a graduação de sua gravidade depende fortemente da aparência das glândulas. Em tecido saudável ou em estágio inicial, as glândulas parecem tubos circulares e bem definidos; em tumores agressivos tornam-se irregulares, fundidas ou quase irreconhecíveis. Computadores podem ser treinados para segmentar, ou “pintar”, cada glândula para permitir medições automáticas, mas sistemas tradicionais de deep learning exigem contornos pixel a pixel desenhados por patologistas especialistas. Em clínicas reais, o que é muito mais fácil de obter são rótulos simples ao nível da imagem, como se um bloco de tecido contém ou não glândulas, ou se é benigno ou maligno.
Ensinando uma IA a partir de lâminas não rotuladas e fracamente rotuladas
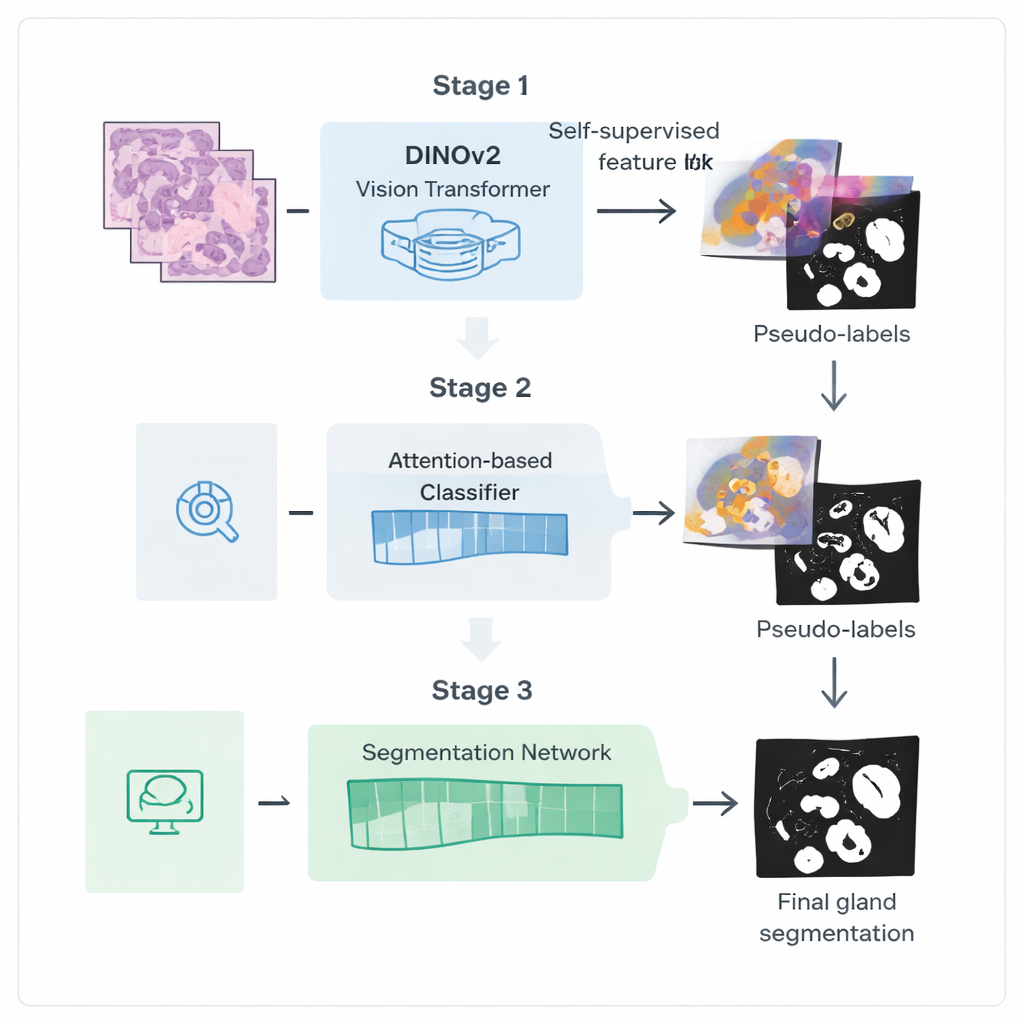
Os autores apresentam um pipeline de treinamento em três etapas projetado para extrair mais valor desses rótulos mais fracos. Primeiro, eles partem de um poderoso modelo de visão chamado DINOv2, originalmente treinado em fotografias naturais, e o expõem a milhares de imagens de biópsias colorretais não rotuladas. Ao pedir que o modelo relacione diferentes vistas do mesmo fragmento de tecido entre si, ele aprende características visuais afinadas com as cores e texturas de lâminas histológicas sem precisar de anotações. Essa etapa cria um “codificador” especializado que transforma imagens brutas em representações internas ricas que capturam estruturas semelhantes a glândulas.
Deixando a IA mostrar onde ela está olhando
Na segunda etapa, esse codificador é integrado a uma rede de classificação que precisa apenas de rótulos ao nível da imagem, como se há glândulas presentes. Um mecanismo de atenção dentro da rede aprende a atribuir pesos maiores às regiões da imagem que mais importam para sua decisão. Esses mapas de atenção destacam efetivamente onde a rede “acredita” que as glândulas estão localizadas. Os pesquisadores transformam esses mapas contínuos em máscaras binárias aproximadas usando mistura e limiarização, e então os limpam com uma técnica probabilística de suavização chamada Campo Aleatório Condicional (Conditional Random Field). O resultado é um conjunto de pseudo-rótulos refinados: contornos de glândulas gerados por computador que não são perfeitos, mas são bons o suficiente para orientar um modelo de segmentação mais especializado.
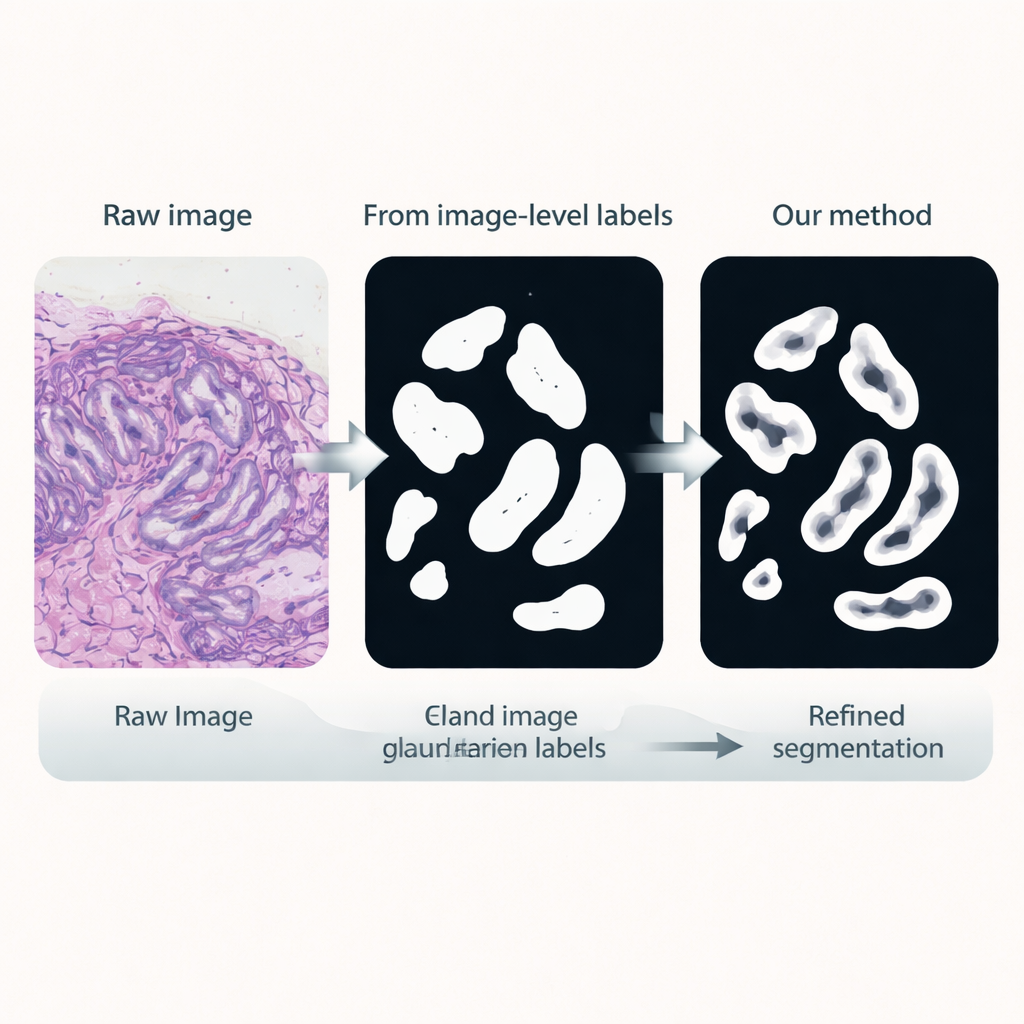
Afinando os limites das glândulas
Na terceira etapa, uma rede de segmentação dedicada é treinada usando esses pseudo-rótulos como substitutos das anotações manuais. Ela reutiliza o codificador ajustado finamente, mas adiciona uma cabeça decodificadora leve que converte as características de volta em uma máscara detalhada das glândulas. Crucialmente, a função de perda usada durante o treinamento dá atenção extra às bordas: erros que distorcem as arestas das glândulas são penalizados mais do que pequenos equívocos no interior. Esse treinamento sensível a contornos incentiva traços nítidos e anatomicamente realistas, essenciais para medir com precisão a forma e a separação das glândulas.
Quão bem isso funciona na prática?
A equipe testou seu método em dois benchmarks padrão de tecido colorretal. No conjunto GlaS, sua abordagem fracamente supervisionada não apenas superou outros métodos que também usam rótulos limitados, como em várias métricas se aproximou ou superou sistemas clássicos totalmente supervisionados que dependem de anotações completas a nível de pixel. Em um conjunto mais desafiador chamado CRAG, repleto de glândulas altamente irregulares e malignas, o desempenho caiu para todos os métodos, mas a nova estrutura ainda superou outros concorrentes com rótulos fracos e reduziu a diferença em relação aos modelos totalmente supervisionados. Estudos de ablação mostraram que cada componente — o fine-tuning auto-supervisionado, a pseudo-rotulagem baseada em atenção com pós-processamento e a perda sensível a contornos — contribuiu de forma significativa para os ganhos.
O que isso significa para ferramentas futuras de patologia
Para um leitor leigo, a principal conclusão é que este trabalho aponta para sistemas de IA capazes de fornecer mapas de alta qualidade e com contornos precisos de estruturas microscópicas de glândulas, confiando principalmente em rótulos simples ao nível da lâmina que já são comuns em arquivos hospitalares. Ao reduzir a dependência de contornos manuais demorados, a abordagem pode tornar a graduação baseada em imagens e a análise quantitativa avançadas mais viáveis em muitos centros, ajudando patologistas a diagnosticar o câncer colorretal de forma mais consistente e eficiente, e potencialmente se estendendo a outros tipos de tecido e estruturas no futuro.
Citação: Wen, H., Wu, Y., Huang, D. et al. Weakly supervised colorectal gland segmentation through self-supervised learning and attention-based pseudo-labeling. Sci Rep 16, 5771 (2026). https://doi.org/10.1038/s41598-026-36256-0
Palavras-chave: câncer colorretal, patologia digital, segmentação de glândulas, aprendizado fracamente supervisionado, visão auto-supervisionada