Clear Sky Science · pt
Vigilância genômica em todo o país de isolados de Klebsiella pneumoniae resistentes a carbapenêmicos e colistina em infecções sanguíneas na Tailândia (2020–2024)
Infecções sanguíneas letais em ascensão
Hospitais ao redor do mundo enfrentam uma tendência preocupante: bactérias comuns que antes sucumbiam aos nossos antibióticos mais potentes estão se tornando quase impossíveis de tratar. Este estudo foca na Klebsiella pneumoniae, um microrganismo capaz de invadir a corrente sanguínea e causar infecções potencialmente fatais, e rastreia como ela evoluiu na Tailândia para resistir até mesmo a medicamentos de último recurso. Entender onde esses super‑micróbios estão se espalhando e como escapam dos remédios é crucial para proteger pacientes, orientar as escolhas médicas e moldar políticas de saúde pública.
Rastreando um supermicrobo hospitalar por uma nação
Os pesquisadores analisaram 227 amostras de Klebsiella pneumoniae isoladas do sangue de pacientes em hospitais da Tailândia entre 2020 e 2024. Essas amostras vieram de uma rede nacional de vigilância que coleta rotineiramente dados sobre infecções resistentes a medicamentos. Testes laboratoriais mostraram que mais de 93% desses isolados sanguíneos eram resistentes a carbapenêmicos, uma classe poderosa de antibióticos frequentemente usada quando outras drogas falham. Preocupantemente, quase um terço das cepas resistentes a carbapenêmicos também era resistente à colistina, uma das últimas opções que os médicos recorrem quando nada mais funciona. Ao combinar testes farmacológicos padrão com sequenciamento genômico completo, a equipe pôde observar não apenas quais medicamentos falharam, mas também quais artifícios genéticos as bactérias usaram para sobreviver.
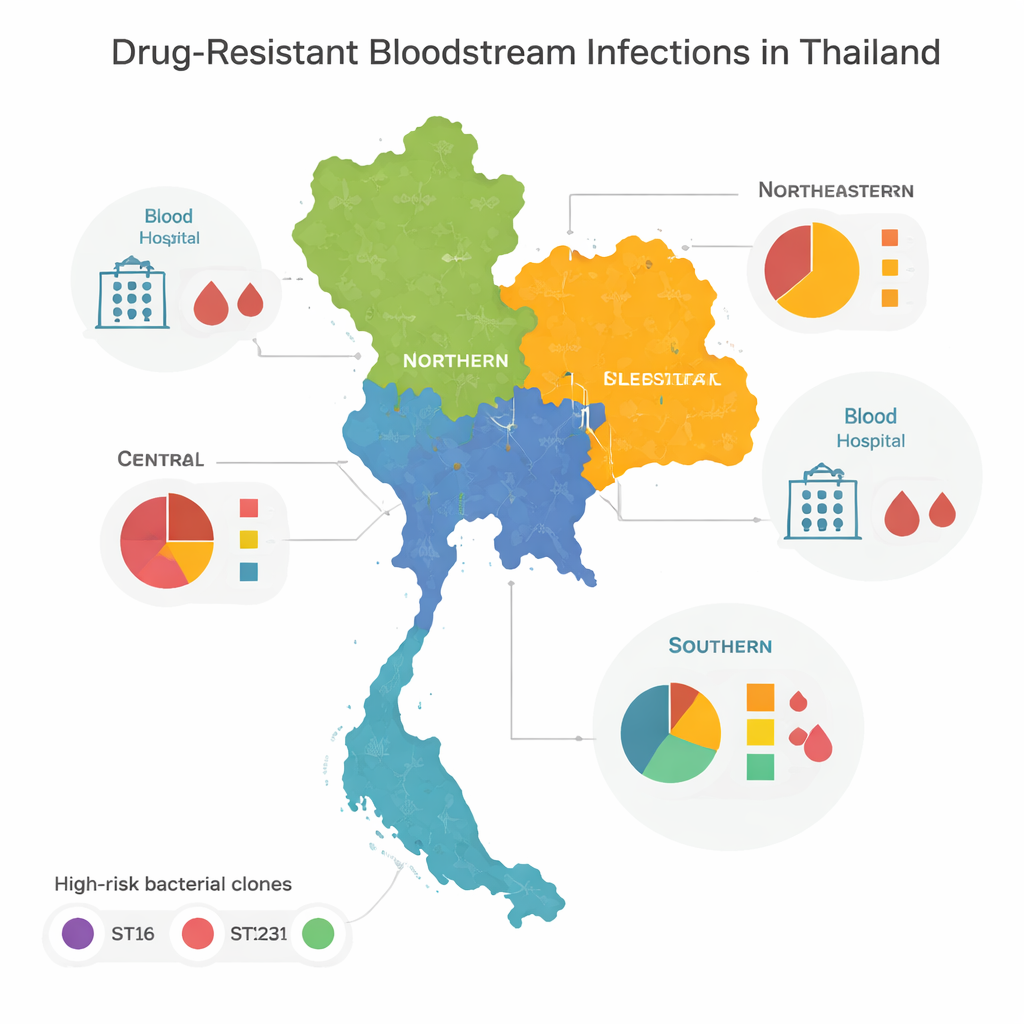
Clones de alto risco e padrões regionais
Ao comparar os genomas, a equipe descobriu que a maioria das bactérias resistentes pertencia a algumas famílias — ou clones — de “alto risco”, conhecidas globalmente por causar surtos hospitalares. Três em particular — chamadas ST16, ST147 e ST231 — dominaram no centro, norte e nordeste da Tailândia. Esses clones se espalharam amplamente pelas regiões, sugerindo movimento frequente de pacientes, equipes ou bactérias entre hospitais. O sul do país apresentou um quadro diferente: em vez de ser dominado por poucos tipos, abrigava uma grande variedade de linhagens bacterianas, muitas vistas apenas uma vez. Essa diversidade indica uma mistura mais complexa de surtos locais, fontes ambientais e movimento transfronteiriço, em vez de um ou dois clones avassaladores.
Como as bactérias ludibriam os antibióticos
O estudo revelou como essas bactérias acumulam múltiplos mecanismos de resistência. Muitas cepas ST16 e ST231 carregavam genes conhecidos como blaNDM e blaOXA, que produzem enzimas que degradam antibióticos carbapenêmicos antes que possam agir. Algumas também apresentavam alterações em sua membrana externa que reduzem a entrada de drogas, combinando‑se para criar resistência em níveis muito altos. Cepas ST231 frequentemente portavam um gene adicional, rmtF1, que bloqueia um importante grupo de medicamentos chamados aminoglicosídeos, reduzindo ainda mais as opções de tratamento. ST147 destacou‑se por sua flexibilidade genética: misturava diferentes genes de resistência e plasmídeos — pequenos anéis de DNA móveis — tornando‑se um potencial centro para disseminação de traços de resistência para outras bactérias.
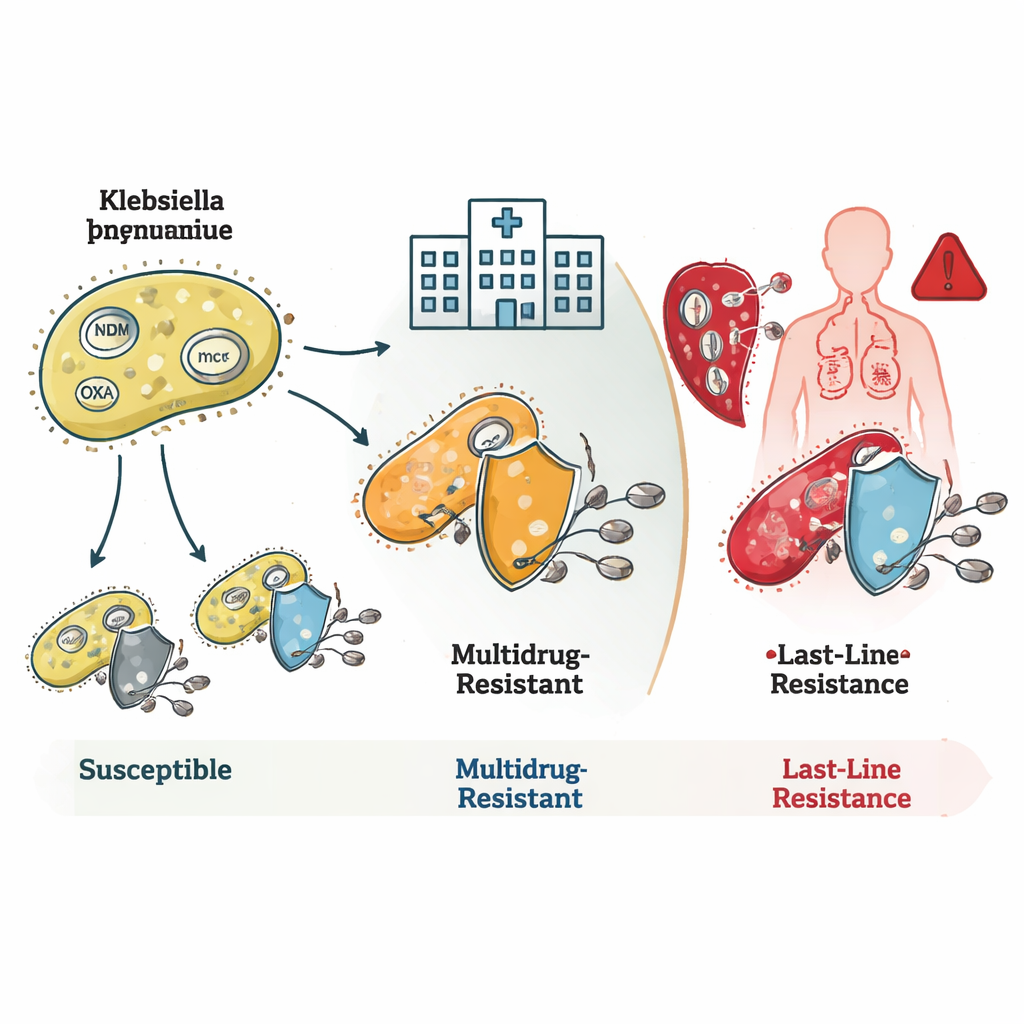
Falhas de última linha e perigos ocultos
A descoberta mais alarmante envolveu a resistência à colistina, um fármaco reservado para situações desesperadas. Algumas famílias bacterianas raras carregavam genes mcr, que podem saltar entre espécies em plasmídeos e causam diretamente resistência à colistina. Outras, especialmente dentro do clone ST16, eram resistentes à colistina mesmo sem portar quaisquer genes ou mutações de resistência conhecidos. Isso sugere que os cientistas ainda não mapearam completamente todas as maneiras pelas quais as bactérias podem neutralizar esse fármaco de última linha. A equipe também identificou cepas hipervirulentas — bactérias especialmente eficazes em causar doenças graves — incluindo uma linhagem que combinou alta virulência com resistência a todos os carbapenêmicos testados, uma mistura particularmente perigosa.
Por que a vigilância genômica importa
Para entender como alterações genéticas se traduziram em falha terapêutica no mundo real, os pesquisadores usaram modelos estatísticos para ligar genes de resistência específicos aos resultados dos testes laboratoriais. Genes como blaNDM‑1 e seus parentes próximos exibiram associações extremamente fortes com resistência a carbapenêmicos, confirmando seu papel central em provocar falhas de tratamento. Ainda assim, para a colistina, a maioria das bactérias resistentes não apresentava marcadores de resistência reconhecidos, apontando para mecanismos ocultos que ainda precisam ser descobertos. Os autores defendem que o uso rotineiro do sequenciamento genômico completo na vigilância hospitalar pode funcionar como um radar de alerta precoce, detectando clones emergentes de alto risco, rastreando seu movimento por regiões e fronteiras e orientando respostas rápidas de controle de infecção.
O que isso significa para pacientes e políticas
Para o público geral, a mensagem é dura, mas clara: algumas infecções sanguíneas na Tailândia agora são causadas por bactérias que resistem a quase todos os medicamentos disponíveis, e algumas famílias perigosas desses microrganismos estão se espalhando amplamente. Ao mesmo tempo, o estudo mostra que com as ferramentas certas — amostragem nacional, análise genética e compartilhamento rápido de dados — os sistemas de saúde podem antecipar essas ameaças e se adaptar. Ampliar a vigilância genômica, desenvolver testes moleculares rápidos e reforçar o controle de infecções pode ajudar a frear o avanço desses super‑micróbios e ganhar tempo para o desenvolvimento de novos tratamentos e vacinas.
Citação: Krobanan, K., Kamjumphol, W., Leethongdee, P. et al. Nationwide genomic surveillance of carbapenem- and colistin-resistant Klebsiella pneumoniae bloodstream isolates in Thailand (2020–2024). Sci Rep 16, 5853 (2026). https://doi.org/10.1038/s41598-026-36228-4
Palavras-chave: resistência antimicrobiana, Klebsiella pneumoniae, infecção na corrente sanguínea, vigilância genômica, assistência médica na Tailândia