Clear Sky Science · pt
Corantes distiril-BODIPY substituídos por piridínio e bromo para terapia fotodinâmica direcionada às mitocôndrias
Iluminando células cancerígenas por dentro
A terapia fotodinâmica é um tratamento contra o câncer que utiliza fármacos especiais ativados por luz para matar células tumorais, poupando em grande parte o tecido saudável. Este estudo explora uma nova família de corantes fluorescentes concebidos para se dirigirem às usinas de energia da célula — as mitocôndrias — e, quando iluminados com luz vermelho-escura, gerarem espécies reativas de oxigênio capazes de destruir células cancerígenas. O trabalho mostra tanto o potencial quanto os desafios de projetar esses corantes em nível molecular.
Por que mirar nas estações de energia da célula?
As mitocôndrias são cruciais para a produção de energia e ajudam a decidir se uma célula sobrevive ou morre. Células cancerígenas tendem a apresentar uma membrana mitocondrial mais carregada do que células normais, o que as torna mais atraentes para moléculas com carga positiva. Os pesquisadores aproveitaram isso ao ligar um grupo piridínio positivamente carregado a um arcabouço de corante fluorescente bem conhecido, chamado BODIPY. Esse projeto ajuda a direcionar os corantes para as mitocôndrias, onde reações químicas desencadeadas pela luz podem causar o dano máximo às células tumorais, limitando os efeitos danosos em outros locais.
Projetando corantes ativados por luz mais inteligentes
A equipe criou três corantes intimamente relacionados, chamados PyBHI, PyBMI e PyBBrI, que diferem principalmente pelo número de átomos de bromo que carregam (nenhum, um ou dois). Todos compartilham uma estrutura longa e estendida que desloca sua absorção e emissão de luz para a região do infravermelho próximo — uma janela útil onde a luz penetra mais profundamente no tecido. Em teoria, esses corantes poderiam usar dois caminhos internos diferentes para alcançar um estado excitado “triplete” que produz oxigênio singlete reativo: um impulsionado pelos pesados átomos de bromo e outro por uma mudança temporária de carga elétrica dentro da molécula. 
Quando a teoria encontra a realidade experimental
Apesar do projeto elegante, testes detalhados mostraram que os corantes não geraram oxigênio singlete com a eficiência desejada. Usando sondas químicas que perdem a cor ao reagir com oxigênio singlete, os pesquisadores mediram rendimentos muito baixos de geração de oxigênio para os três corantes, com apenas uma melhora modesta à medida que mais átomos de bromo eram adicionados. Experimentos com laser ultrarrápido revelaram o motivo: após a absorção de luz, os corantes rapidamente entram em estados deslocados de carga que, em grande parte, relaxam de forma inofensiva como calor em vez de se converterem ao estado triplete desejado. Nas versões bromadas, os átomos pesados ainda abrem uma via para o estado triplete, mas essa rota é muito mais lenta do que a perda concorrente de energia, limitando a eficiência global.
Diretamente às mitocôndrias tumorais em células vivas
A história muda em um contexto biológico. Em culturas de células humanas de mama (MCF-7) e de colo do útero (HeLa), os três corantes mostraram, por microscopia confocal, acumulação forte nas mitocôndrias, co-localizando-se com um corante mitocondrial padrão. Testes de toxicidade no escuro indicaram que os corantes são em grande parte inofensivos sem a luz. Sob irradiação por luz vermelha, entretanto, o corante dibromado PyBBrI causou morte substancial de células cancerígenas, com doses na faixa de nanomolar reduzindo pela metade a viabilidade celular. Os outros dois corantes foram muito menos eficazes. 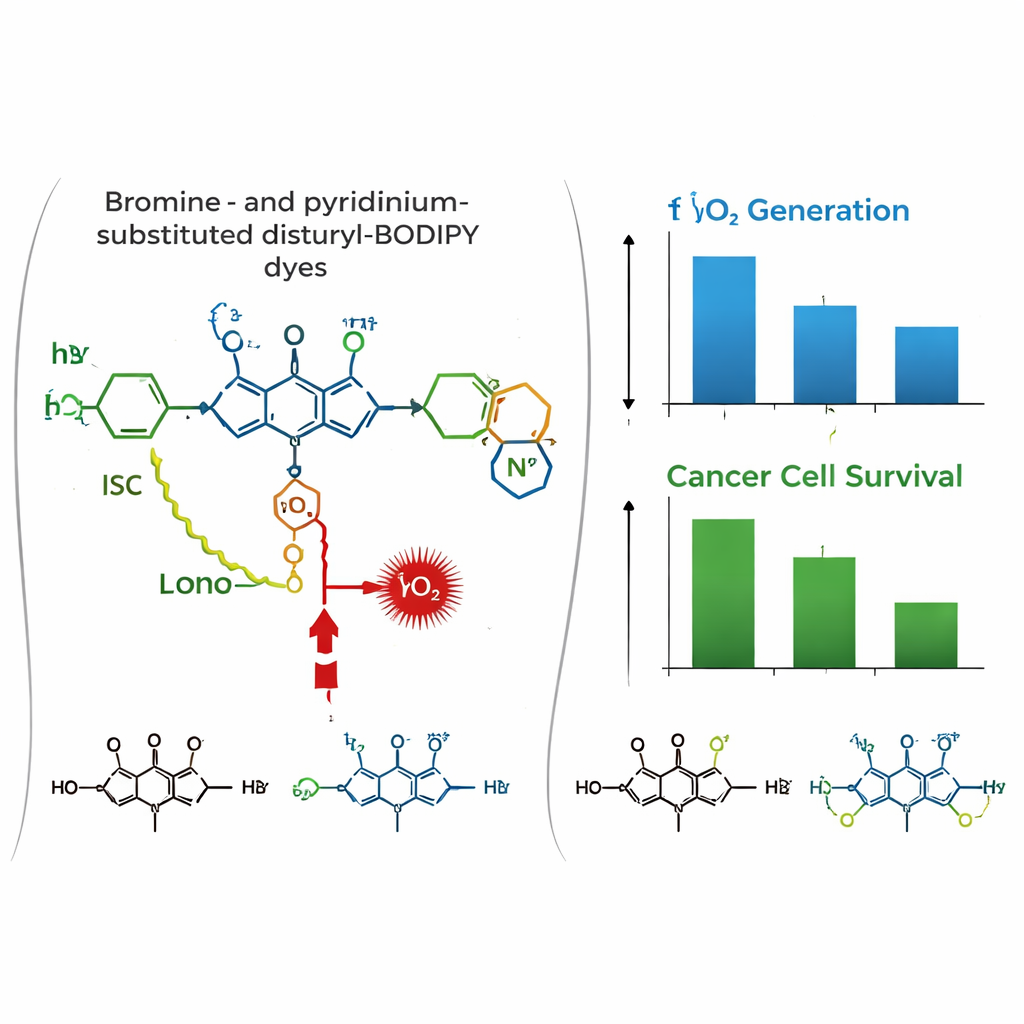
O que isso significa para terapias futuras contra o câncer
Para um público não especialista, a mensagem principal é que pequenas modificações químicas podem alterar drasticamente o comportamento de fármacos ativados por luz, e que seu desempenho em células reais pode ser melhor — ou pior — do que o previsto por medições básicas. Neste caso, o corante mais fortemente modificado, PyBBrI, mostrou apenas produção modesta de oxigênio reativo em tubo de ensaio, mas revelou-se altamente potente contra células cancerígenas uma vez que atingiu suas mitocôndrias. O trabalho destaca tanto a importância de direcionar fármacos a estruturas vulneráveis dentro das células cancerígenas quanto a complexidade de prever a eficiência fotodinâmica. Aponta o caminho para terapias de próxima geração, direcionadas às mitocôndrias, que usam luz no infravermelho próximo para “ativar” seletivamente a química letal exatamente onde ela é necessária.
Citação: Kim, C., Badon, I.W., Jo, J. et al. Pyridinium- and bromine-substituted distyryl-BODIPY dyes for mitochondria-targeted photodynamic therapy. Sci Rep 16, 6789 (2026). https://doi.org/10.1038/s41598-026-36213-x
Palavras-chave: terapia fotodinâmica, corantes direcionados às mitocôndrias, BODIPY, oxigênio singlete, células cancerígenas