Clear Sky Science · pt
TDP-43 citoplasmático causa comprometimentos comportamentais precoces sem neurodegeneração em um modelo de C. elegans específico para neurônios serotoninérgicos
Por que vermes minúsculos importam para grandes doenças cerebrais
Condições como esclerose lateral amiotrófica (ELA) e demência frontotemporal (DFT) roubam lentamente das pessoas a capacidade de se mover, falar e manter a personalidade. Um suspeito-chave nessas doenças é uma proteína chamada TDP-43, que se agrega no lugar errado dentro das células nervosas. Este estudo usa um verme minúsculo, Caenorhabditis elegans, para observar o que acontece em animais vivos quando a TDP-43 sai de seu local habitual e vai para o citoplasma da célula. Ao focar em um pequeno e bem compreendido conjunto de neurônios produtores de serotonina, os pesquisadores mostram como o comportamento pode se comprometer muito antes de os neurônios morrerem visivelmente — oferecendo uma janela para os estágios iniciais da doença, quando há maior chance de intervenção.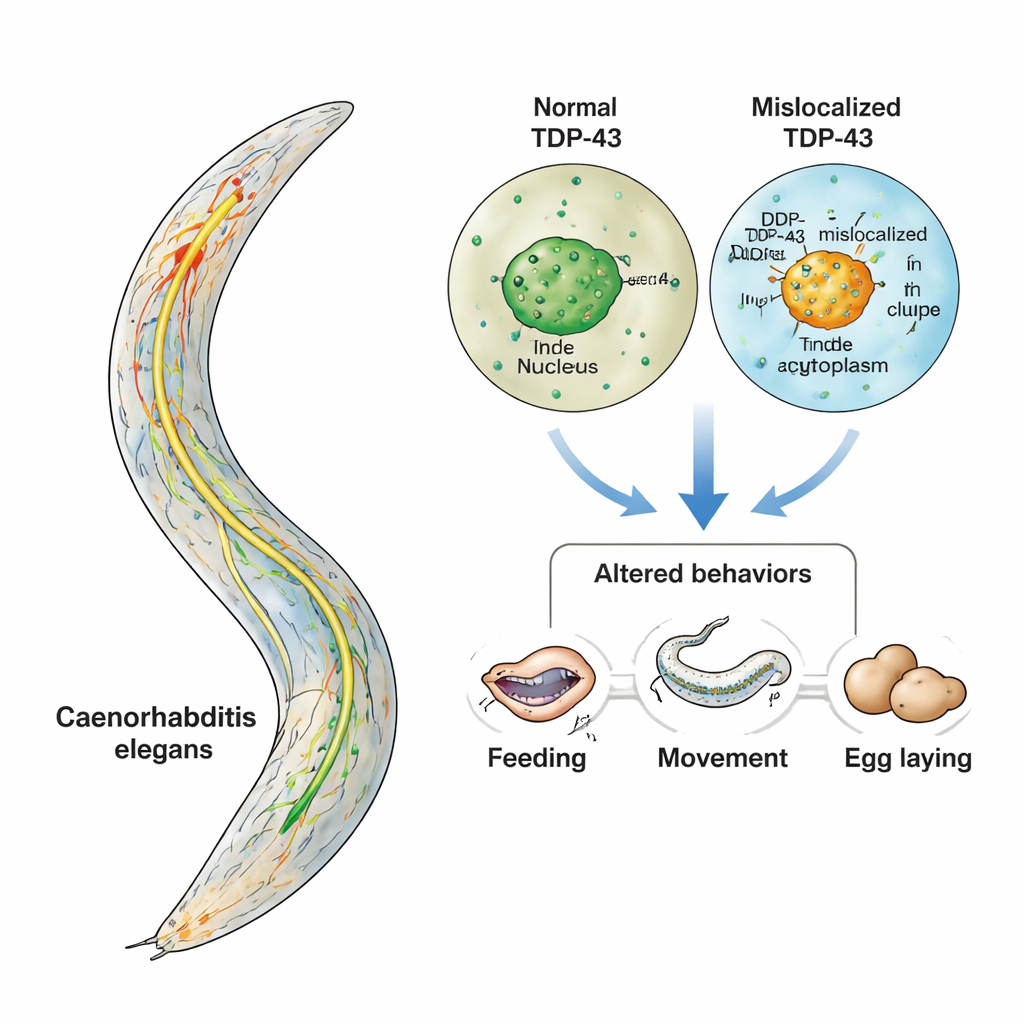
Uma proteína que se agrega e um mensageiro químico
A TDP-43 normalmente vive no núcleo, onde ajuda a controlar o RNA, as cópias de trabalho das instruções genéticas da célula. Na ELA e na DFT, contudo, a TDP-43 frequentemente sai do núcleo, acumula-se no citoplasma e forma agregados pegajosos. Ao mesmo tempo, evidências de pacientes e modelos em camundongos indicam que a serotonina, um mensageiro químico mais conhecido por seu papel no humor, também é afetada nessas doenças. Como a serotonina influencia muitos comportamentos — desde a alimentação até o controle do movimento — os autores fizeram uma pergunta focal: se a TDP-43 estiver mal localizada especificamente nos neurônios produtores de serotonina, esses neurônios falham de modo a alterar o comportamento, mesmo antes de degenerarem?
Reconfigurando um sistema nervoso simples
A equipe recorreu ao C. elegans, um verme microscópico cujo sistema nervoso inteiro, de 302 neurônios, foi cuidadosamente mapeado. Apenas três pares desses neurônios produzem serotonina, e cada par controla um comportamento bem definido: alimentação (bombeamento faríngeo), desaceleração ao encontrar alimento e postura de ovos. Usando ferramentas genéticas, os pesquisadores criaram vermes de modo que apenas esses neurônios serotoninérgicos produzissem TDP-43 humana. Uma linhagem produzia a forma normal, localizada no núcleo; outra produzia uma versão mutante sem sua “etiqueta de endereço” nuclear, forçando a TDP-43 a se acumular no citoplasma. Como todos os outros neurônios foram deixados intactos, quaisquer mudanças comportamentais podiam ser atribuídas diretamente a problemas neste único e diminuto circuito.
O comportamento falha antes dos neurônios morrerem
Em vários testes, os vermes alterados exibiram comportamentos anormais que refletiram de perto perda parcial ou severa de serotonina. Vermes com a versão citoplasmática da TDP-43 apresentaram bombeamento rítmico da alimentação mais lento, menor tendência a desacelerar ao encontrar alimento após jejum e redução na postura de ovos. Vermes expressando a TDP-43 normal, nuclear, também tiveram desempenho pior do que animais não modificados, mas não tão ruim quanto os com TDP-43 citoplasmática, revelando um gradiente claro de comprometimento. Crucialmente, quando os mesmos animais foram testados em um contexto em que a serotonina não é necessária — nadando em líquido — seu movimento foi normal. Isso mostrou que a maquinaria locomotora central estava intacta e que os defeitos eram específicos de comportamentos dependentes de serotonina, não de um declínio geral na saúde.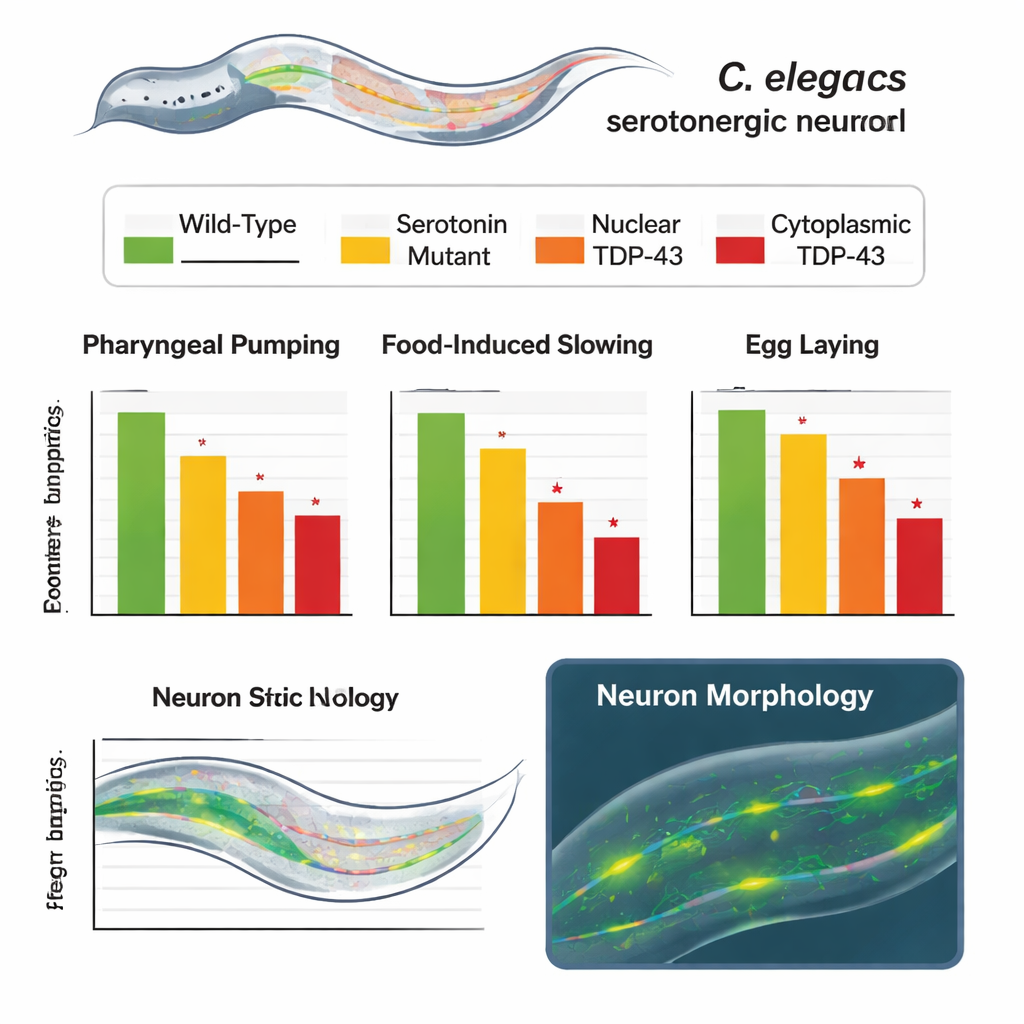
Dano oculto revelado por um teste farmacológico
Para descobrir se os neurônios afetados ainda estavam vivos e funcionais, os pesquisadores usaram fluoxetina, mais conhecida como Prozac, um medicamento que potencializa a sinalização da serotonina. Em vermes normais, a fluoxetina aumenta fortemente a postura de ovos. Nos vermes geneticamente alterados, a droga ainda aumentou a postura de ovos, mas a resposta foi atenuada — especialmente naqueles com TDP-43 citoplasmática. Esse padrão sugere que os neurônios serotoninérgicos ainda podiam liberar sinais, mas o faziam com menos eficiência. A imagem microscópica contou uma história semelhante: os neurônios produtores de serotonina pareciam estruturalmente normais, sem perda de corpos celulares ou distorções marcantes em seus ramos, e sua fluorescência geral — um proxy para a saúde celular — correspondia à dos vermes controle.
Sinais de alerta precoces e novas oportunidades
Em conjunto, os achados desenham um quadro em que a TDP-43 mal localizada pode perturbar gravemente o funcionamento dos neurônios de serotonina enquanto os deixa aparentemente intactos ao olhar. Nos vermes, o comportamento se altera — alimentação, ajuste de movimento e reprodução — antes de qualquer morte neuronal visível. Isso ecoa observações clínicas de que alterações sutis de comportamento e humor frequentemente precedem a perda óbvia de massa cerebral em doenças neurodegenerativas humanas. Ao oferecer um sistema simples e geneticamente manipulável onde defeitos precoces e específicos de circuito podem ser medidos com precisão, este modelo de verme pode ajudar cientistas a investigar como a TDP-43 atrapalha a função neuronal e testar terapias destinadas a resgatar neurônios durante essa janela vulnerável e pré-degenerativa.
Citação: Lacour, A., Vassallu, F., Romussi, S. et al. Cytoplasmic TDP-43 leads to early behavioral impairments without neurodegeneration in a serotonergic neuron-specific C. elegans model. Sci Rep 16, 6068 (2026). https://doi.org/10.1038/s41598-026-36138-5
Palavras-chave: TDP-43, neurônios de serotonina, C. elegans, ALS e DFT, neurodegeneração