Clear Sky Science · pt
O panorama transcriptômico de célula única do pulmão pediátrico com fibrose cística a partir de amostras respiratórias minimamente invasivas
Por que isso importa para crianças com fibrose cística
A fibrose cística é mais conhecida pelo muco espesso e pelas infecções pulmonares, mas por trás desses sintomas existe uma batalha complexa entre células imunológicas e o delicado revestimento das vias aéreas. Este estudo foca nessa batalha em crianças, célula a célula, usando pequenas amostras coletadas durante exames rotineiros dos pulmões. Ao mapear quais células estão presentes e quão ativas são, os pesquisadores mostram que padrões prejudiciais de inflamação começam cedo na vida e podem ser difíceis de reverter, mesmo com medicamentos modernos que corrigem o defeito gênico de base.
Espiando pulmões jovens, uma célula por vez
Para explorar o que acontece dentro dos pulmões das crianças, a equipe usou ferramentas minimamente invasivas durante broncoscopia flexível — procedimentos que esses pacientes já estavam realizando por motivos médicos. Eles escovaram suavemente a superfície interna da traqueia e dos brônquios e coletaram líquido de lavagem de regiões mais profundas do pulmão. Essas amostras vieram de duas crianças com fibrose cística (um bebê e um adolescente) e de três crianças sem a doença, pareadas por idade. Usando sequenciamento de RNA de célula única, uma técnica que lê quais genes estão ativados em milhares de células individuais, construíram um mapa de alta resolução das células imunes e das células que revestem as vias aéreas em cada pulmão infantil. 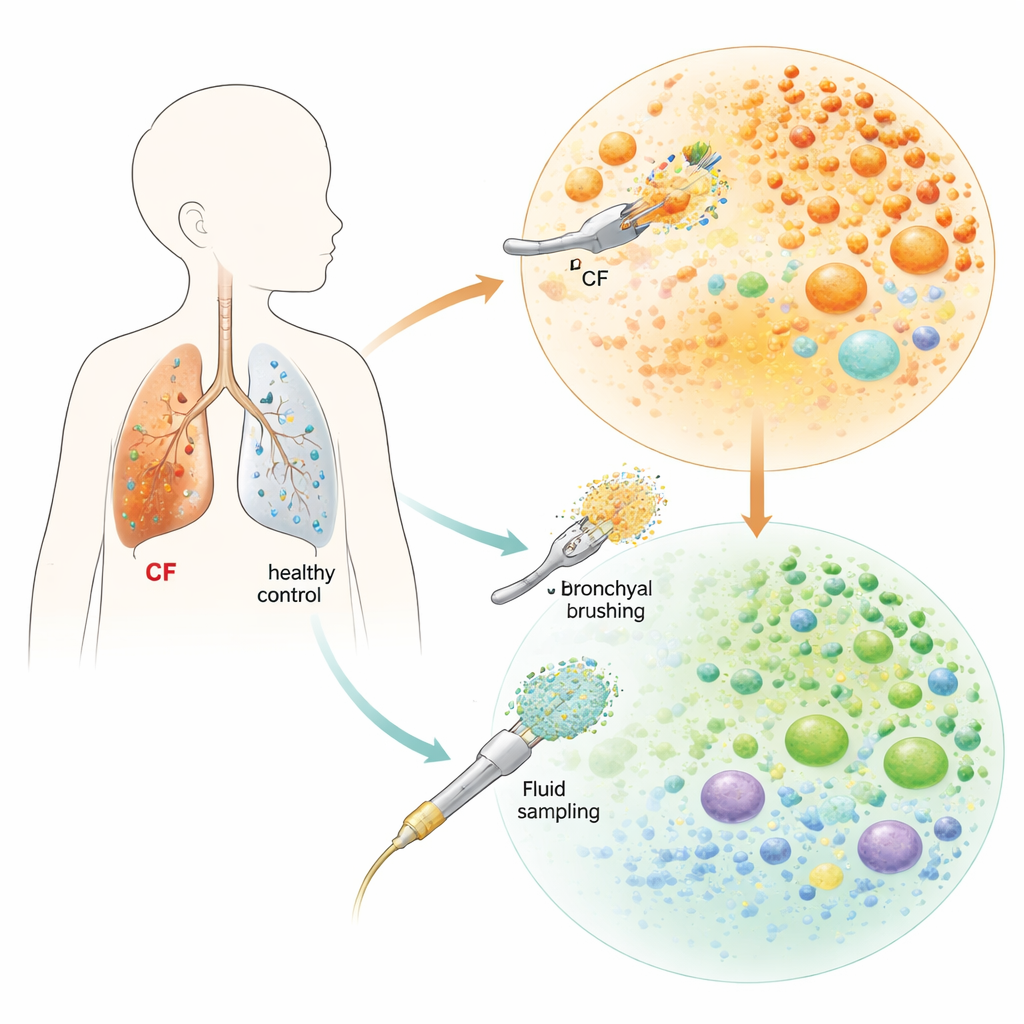
Um campo lotado de células imunes ‘primeiros socorros’
Nas amostras de lavagem pulmonar de crianças sem fibrose cística, a população foi dominada por macrófagos — células de limpeza que patrulham os espaços aéreos e ajudam a manter a paz. Em contraste, as crianças com fibrose cística exibiram uma mudança dramática em direção aos neutrófilos, glóbulos brancos de ação rápida que podem danificar o tecido quando persistem. Os neutrófilos não só eram mais abundantes, como apareceram em várias variantes distintas. Isso incluiu formas imaturas, células inflamatórias altamente ativadas e um subconjunto notável marcado por proteínas de resposta ao estresse conhecidas como proteínas de choque térmico. Embora tais respostas de estresse possam começar como protetoras, elas podem fixar os neutrófilos em um estado agressivo e de longa duração que mantém a inflamação acesa e pode impulsionar o dano das vias aéreas observado na fibrose cística.
Defensores inflamados e reforços ausentes
Os macrófagos que permaneciam nos pulmões com fibrose cística também apresentavam diferenças. Em vez de uma mistura dos tipos de manutenção comuns vista no grupo de comparação, as amostras de fibrose cística estavam enriquecidas por macrófagos que produzem sinais imunes fortes, sugerindo um deslocamento para um papel mais inflamatório. Ao mesmo tempo, havia relativamente poucas células T — outro braço importante do sistema imune — no líquido das vias aéreas das crianças com fibrose cística. Trabalhos anteriores mostram que neutrófilos podem privar as células T dos nutrientes necessários para funcionar, efetivamente empurrando-as para fora das vias aéreas. Essa combinação de neutrófilos agressivos, macrófagos ativados e células T escassas pode ajudar a explicar por que os pulmões com fibrose cística permanecem inflamados e propensos a infecções ao longo de muitos anos.
Um revestimento das vias aéreas que entra na luta
As amostras de escovado permitiram aos pesquisadores observar as células que revestem as vias aéreas: células basais (que podem renovar o epitélio), células ciliadas (com projeções semelhantes a pelos que varrem o muco) e células secretoras (que produzem muco e moléculas protetoras). A mistura geral desses tipos celulares foi similar entre crianças com fibrose cística e o grupo de comparação, mas o comportamento delas não foi. Na fibrose cística, as células secretoras ativaram genes ligados à defesa imune e à atividade antimicrobiana, sugerindo que estão trabalhando em excesso como parte da resposta inflamatória. As células ciliadas também ativaram genes relacionados à inflamação e à resistência a uma forma de morte celular ligada ao ferro e ao dano oxidativo. Juntos, esses padrões apontam para uma superfície das vias aéreas que não é apenas espectadora, mas uma participante ativa e inflamada no processo da doença. 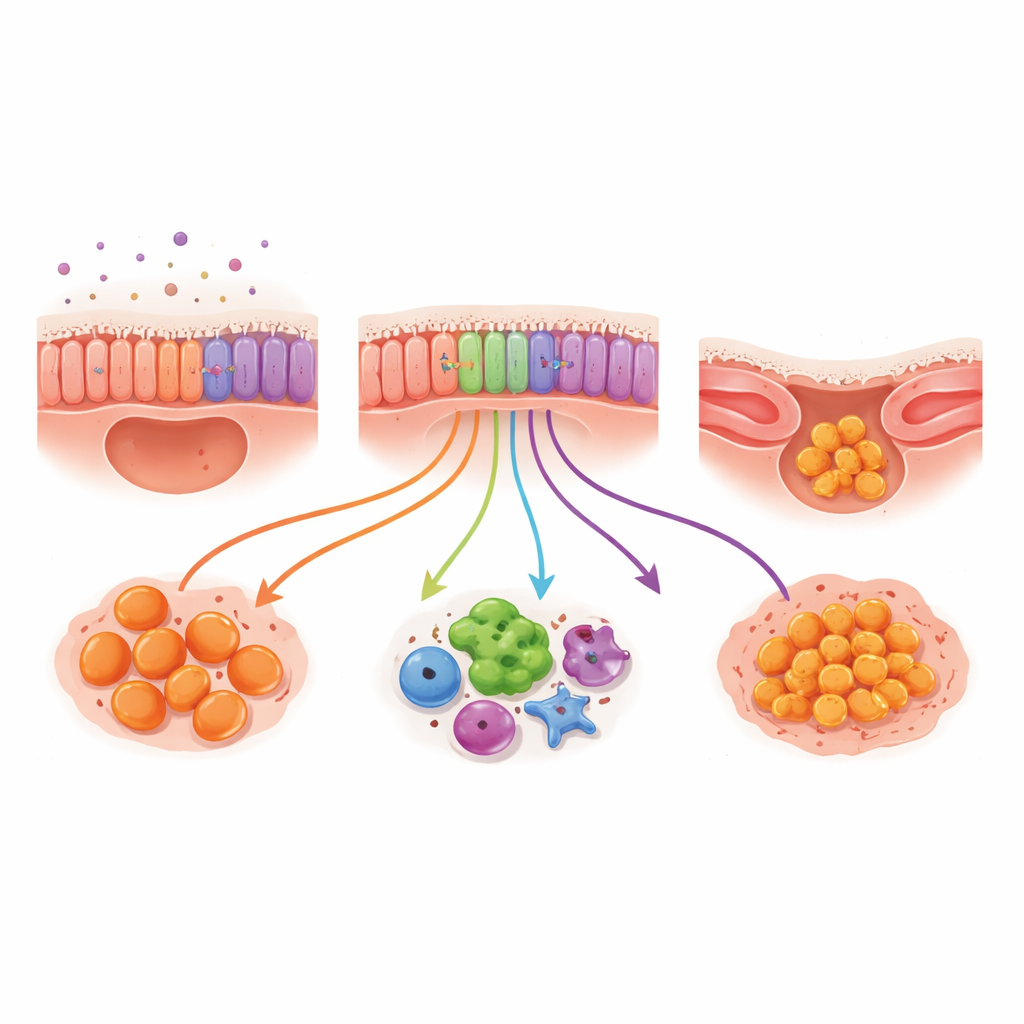
Conversas célula a célula que alimentam o dano pulmonar
Para entender como as células do revestimento das vias aéreas e os neutrófilos se influenciam mutuamente, a equipe analisou as “conversas” entre eles — sinais enviados por um tipo celular e recebidos por outro. Descobriram que as células epiteliais frequentemente atuam como emissoras, usando vários sistemas moleculares para alcançar os neutrófilos. Alguns desses sinais provavelmente ajudam a acalmar a inflamação, enquanto outros encorajam os neutrófilos a se aglomerarem, ativarem-se e engolirem material. Esse empurra-puxa sugere que o epitélio das vias aéreas tenta equilibrar controle de dano e defesa, mas na fibrose cística os sinais pró-inflamatórios parecem prevalecer, mantendo o pulmão em um estado crônico de dano fumegante.
Por que mudanças precoces são difíceis de reverter
Uma descoberta chave é que esses padrões inflamatórios estavam presentes tanto em um bebê quanto em um adolescente que vinha tomando um medicamento avançado para fibrose cística que melhora a proteína defeituosa. Apesar dessa terapia dirigida, as células pulmonares do adolescente ainda se assemelhavam mais às do bebê não tratado do que às das crianças de comparação. Isso implica que, uma vez que o dano estrutural e a inflamação enraizada se desenvolvem, simplesmente restaurar a função da proteína subjacente pode não ser suficiente para redefinir o panorama imunológico e epitelial. O estudo também mostra que a amostragem suave das vias aéreas, combinada com análises gênicas de célula única e espaciais, pode monitorar essas mudanças ao longo do tempo. Essa abordagem pode ajudar a conceber e testar novos tratamentos anti-inflamatórios e antimicrobianos destinados a preservar a estrutura pulmonar desde os primeiros momentos de vida.
Citação: Sun, Y., Vicencio, A.G., Beasley, M.B. et al. The single-cell transcriptional landscape of the pediatric cystic fibrosis lung from minimally invasive respiratory specimens. Sci Rep 16, 8113 (2026). https://doi.org/10.1038/s41598-026-36125-w
Palavras-chave: pulmão com fibrose cística, inflamação neutrofílica, sequenciamento de RNA de célula única, epitélio das vias aéreas, broncoscopia pediátrica