Clear Sky Science · pt
Posições R5 e R7 em esqueletos de fluoroquinolonas promovem a ruptura de filamentos de F-actina
Transformando antibióticos em ajudantes do cérebro
Muitas doenças cerebrais comuns, da doença de Alzheimer ao Parkinson, compartilham um culpado oculto: minúsculos bastões estruturais dentro dos neurônios que ficam travados e rígidos com o tempo. Esses bastões são feitos de uma proteína chamada actina, normalmente uma parte flexível do andaime interno da célula. Este estudo explora uma possibilidade surpreendente — que uma classe bem conhecida de antibióticos, as fluoroquinolonas, poderia ser redesenhada para desmontar suavemente esses feixes nocivos de actina e, potencialmente, ajudar a proteger o cérebro.
Quando os andaimes celulares falham
Neurônios saudáveis remodelam constantemente seu esqueleto interno para formar e ajustar conexões. Os filamentos de actina são centrais nesse processo, formando-se e se desmanchando conforme necessário. Sob estresse, porém, a actina pode travar em agregados teimosos em forma de bastão que entopem a célula, atrapalham o transporte de cargas vitais e favorecem o acúmulo de proteínas associadas a doenças, como amiloide e tau. Ao longo dos anos, esses bastões podem evoluir para estruturas densas conhecidas como corpos de Hirano, comumente observadas em cérebros de pessoas com várias condições neurodegenerativas. Como os fármacos que atuam na actina existentes costumam ser extremamente tóxicos, os pesquisadores buscam pequenas moléculas mais seguras que possam afrouxar esses agregados sem prejudicar as células.
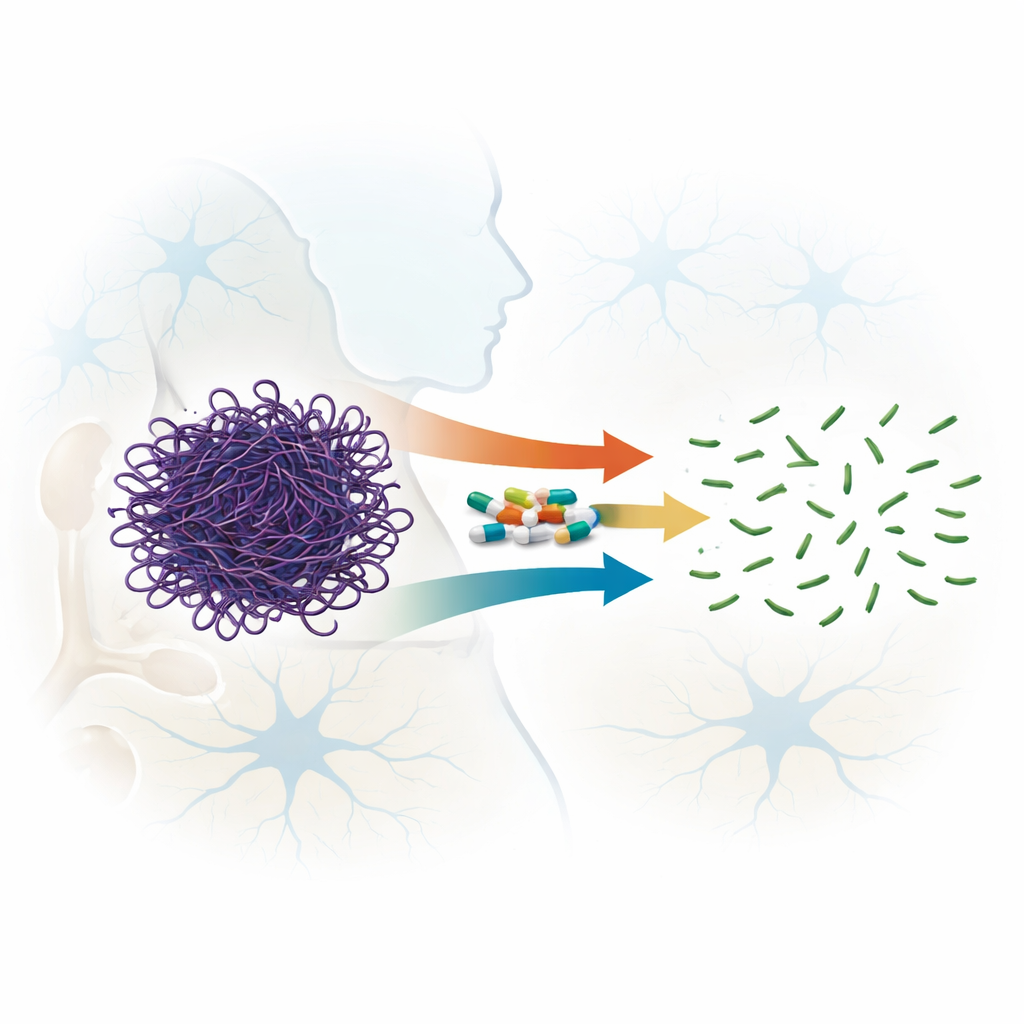
Um talento inesperado de medicamentos familiares
As fluoroquinolonas são antibióticos de amplo espectro usados mundialmente para tratar infecções, e alguns membros mais novos dessa família conseguem atravessar a barreira hematoencefálica. Indícios anteriores sugeriam que certas fluoroquinolonas podiam desestabilizar filamentos de actina. Neste trabalho, os autores compararam sistematicamente sete compostos relacionados, abrangendo quatro gerações da família, para avaliar quão bem eles quebram filamentos de actina pré-formados, em vez de apenas impedir sua formação. Usando medidas de espalhamento de luz, microscopia eletrônica e filtração em gel, mostraram que todos os fármacos testados podiam perturbar filamentos de actina, mas com potências muito diferentes. Dois medicamentos, sparfloxacino (composto de terceira geração) e moxifloxacino (quarta geração), destacaram-se por cortar rápida e irreversivelmente filamentos longos em pedaços muito menores, mesmo em razões droga:proteína relativamente baixas.
Vendo os filamentos se desmancharem
Imagens de alta resolução e testes biofísicos revelaram como os filamentos mudam sob tratamento com os fármacos. A microscopia eletrônica mostrou que a actina não tratada forma fios longos e contínuos, enquanto fluoroquinolonas eficazes convertem esses fios em fragmentos curtos e dispersos. Membros menos potentes produziram filamentos dobrados e angulados, mas não os partiram completamente. Medidas térmicas da estabilidade proteica confirmaram essa ruptura física: uma vez tratados, os filamentos de actina passaram a se comportar mais como sua forma livre e não montada, com temperaturas de fusão mais baixas, embora sua estrutura básica de bloco de construção permanecesse quase inalterada. Isso sugere que os fármacos não desdobram nem danificam a actina em si — eles principalmente forçam a separação das unidades que se unem nos filamentos.
Detalhando o aperto molecular
Para entender por que algumas fluoroquinolonas funcionam melhor que outras, a equipe combinou experimentos avançados de ressonância magnética nuclear com simulações computacionais das interações droga–proteína. Eles descobriram que todos os compostos dependem de um “núcleo” em forma de anel compartilhado para fazer contato com a actina, especialmente em duas posições desse núcleo que tocam repetidamente o filamento. No entanto, grupos químicos extras ligados em sítios específicos — chamados R5 e R7 — influenciam fortemente com que firmeza e onde cada molécula se liga. Nos disruptores mais eficazes, essas posições carregam um grupo amino e sistemas de anéis volumosos que alcançam um pequeno bolso na interface entre filamentos vizinhos de actina. Ali, interferem em contatos estabilizadores-chave, incluindo uma ponte salina importante que normalmente ajuda a manter os filamentos unidos.
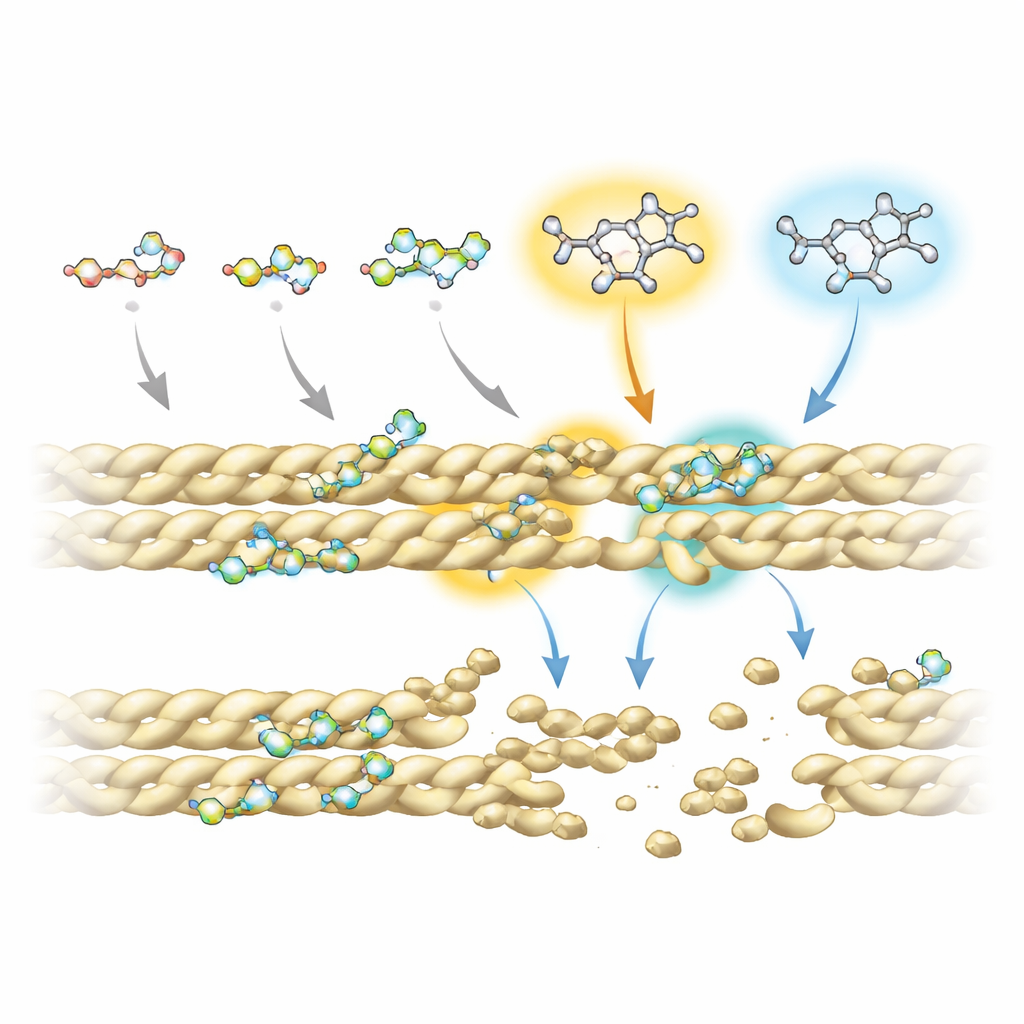
De leveduras a futuras terapias
Os pesquisadores também testaram os fármacos em uma cepa de levedura que naturalmente acumula feixes de actina, imitando aspectos de células doentes. Ao microscópio, leveduras não tratadas mostraram grandes aglomerados brilhantes de actina, enquanto células expostas às fluoroquinolonas — especialmente sparfloxacino, moxifloxacino e, em doses maiores, ácido nalidíxico — exibiram padrões muito mais difusos e puntiformes, indicando que os feixes haviam sido desfeitos. Importante, a ação dos fármacos pareceu relativamente suave: eles enfraqueceram o empacotamento dos filamentos sem distorcer grosseiramente a forma subjacente da actina, e sua ligação foi mais fraca do que a de toxinas clássicas da actina, potencialmente reduzindo o risco de efeitos colaterais severos.
Projetando fármacos mais inteligentes que miram a actina
No conjunto, este estudo demonstra que ajustes sutis em antibióticos conhecidos podem alterar dramaticamente como eles interagem com o andaime interno da célula. Ao identificar as posições R5 e R7 como “botões de controle” chave tanto para a disrupção da actina quanto para a penetração cerebral, os autores esboçam um roteiro para criar novas moléculas inspiradas em fluoroquinolonas que desmontem seletivamente agregados nocivos de actina. Embora essas descobertas sejam uma prova de princípio em estágio inicial, em laboratório, elas levantam a possibilidade de que fármacos futuros derivados de antibióticos familiares possam ajudar a remover andaimes tóxicos em neurônios e retardar ou prevenir algumas formas de neurodegeneração.
Citação: Gupta, R.J., Nair, H., Sarhadi, T.R. et al. R5 and R7 positions on fluoroquinolone scaffolds drive F-actin filament disruption. Sci Rep 16, 9517 (2026). https://doi.org/10.1038/s41598-026-36089-x
Palavras-chave: agregados de actina, antibióticos fluoroquinolônicos, doença neurodegenerativa, reaproveitamento de medicamentos, citoesqueleto