Clear Sky Science · pt
O papel dos genes relacionados à senescência celular na lesão por isquemia–reperfusão e a identificação de seus biomarcadores
Por que o dano cardíaco pode piorar quando o sangue retorna
Quando alguém tem um ataque cardíaco ou passa por cirurgia no coração, os médicos correm para restaurar o fluxo sanguíneo ao músculo cardíaco faminto. Paradoxalmente, essa medida que salva vidas pode causar dano adicional — um problema conhecido como lesão por isquemia–reperfusão. Este estudo explora por que algumas células cardíacas respondem tão mal quando o sangue retorna, focando na biologia do envelhecimento celular e identificando um pequeno conjunto de genes que podem ajudar os médicos a detectar e, eventualmente, tratar esse dano oculto com mais precisão.
Quando o resgate se transforma em novo dano
A lesão por isquemia–reperfusão ocorre em dois atos. Primeiro, uma artéria coronária fica bloqueada e o tecido cardíaco é privado de oxigênio (isquemia). Depois, quando o bloqueio é liberado e o sangue volta em massa (reperfusão), uma explosão de moléculas reativas e inflamação pode danificar células já fragilizadas. As ferramentas atuais — como ECGs, exames de imagem e testes sanguíneos para proteínas como troponina — frequentemente deixam passar danos iniciais ou sutis e não conseguem prever facilmente quem terá problemas a longo prazo. Essa lacuna levou os pesquisadores a investigar mais a fundo, nos eventos moleculares dentro das próprias células cardíacas.
O envelhecimento celular como um motor oculto
Os autores concentram‑se na senescência celular, um estado em que as células param de se dividir permanentemente e adotam um comportamento de “envio de sinais de alarme”. Células cardíacas senescentes secretam uma mistura de moléculas inflamatórias e enzimas conhecida como fenótipo secretório associado à senescência. Essa nuvem química pode agravar a cicatrização, atrair células imunes e interferir na reparação do tecido, criando um ciclo vicioso de dano e disfunção crônica. Ao minerar conjuntos de dados públicos de expressão gênica de corações de camundongos expostos à isquemia–reperfusão e cruzá‑los com centenas de genes ligados ao envelhecimento celular, a equipe reduziu o campo para 26 genes que mudam de forma marcante após a lesão.
Seis genes que formam uma impressão digital diagnóstica
Para encontrar os sinais mais informativos entre esses 26 genes, os pesquisadores usaram vários métodos de aprendizado de máquina. Esses algoritmos procuram combinações de genes que melhor distingam corações lesionados de saudáveis. Após análises de regressão logística, LASSO e máquina de vetor de suporte, emergiram seis genes como um painel diagnóstico poderoso: CDKN2B, ID1, STAT3, TERF2, TP53 e ZNF277. Juntos, seus padrões de atividade puderam identificar a lesão por isquemia–reperfusão com precisão muito alta nos conjuntos de dados combinados, superando muitos marcadores sanguíneos tradicionais em testes internos. Análises de vias gênicas ligaram esses marcadores a circuitos de resposta ao estresse envolvendo dano oxidativo, programas de morte celular e rotas de sinalização bem conhecidas como MAPK e PI3K–AKT, todas as quais determinam se uma célula se recupera ou entra em senescência permanente.
Como o sistema imune entra na história
O dano causado pelo retorno do fluxo sanguíneo não ocorre isoladamente; células imunes rapidamente invadem o coração. Ao estimar a atividade de células imunes a partir dos mesmos dados de expressão gênica, o estudo encontrou sinais claros de maior participação imune em corações lesionados, incluindo vários tipos de células T, células B, macrófagos e células cebadas (mastócitos). Um gene relacionado ao envelhecimento, CDKN2B, acompanhou fortemente células T CD4 de “memória central”, enquanto TP53 se correlacionou com mastócitos ativados. Esses vínculos sugerem que as vias de envelhecimento nas células cardíacas e as mudanças no sistema imune se reforçam mutuamente: células com atuação relacionada ao envelhecimento chamam ajuda imune, e essas respostas imunes podem, por sua vez, aprofundar o dano e a formação de cicatriz.
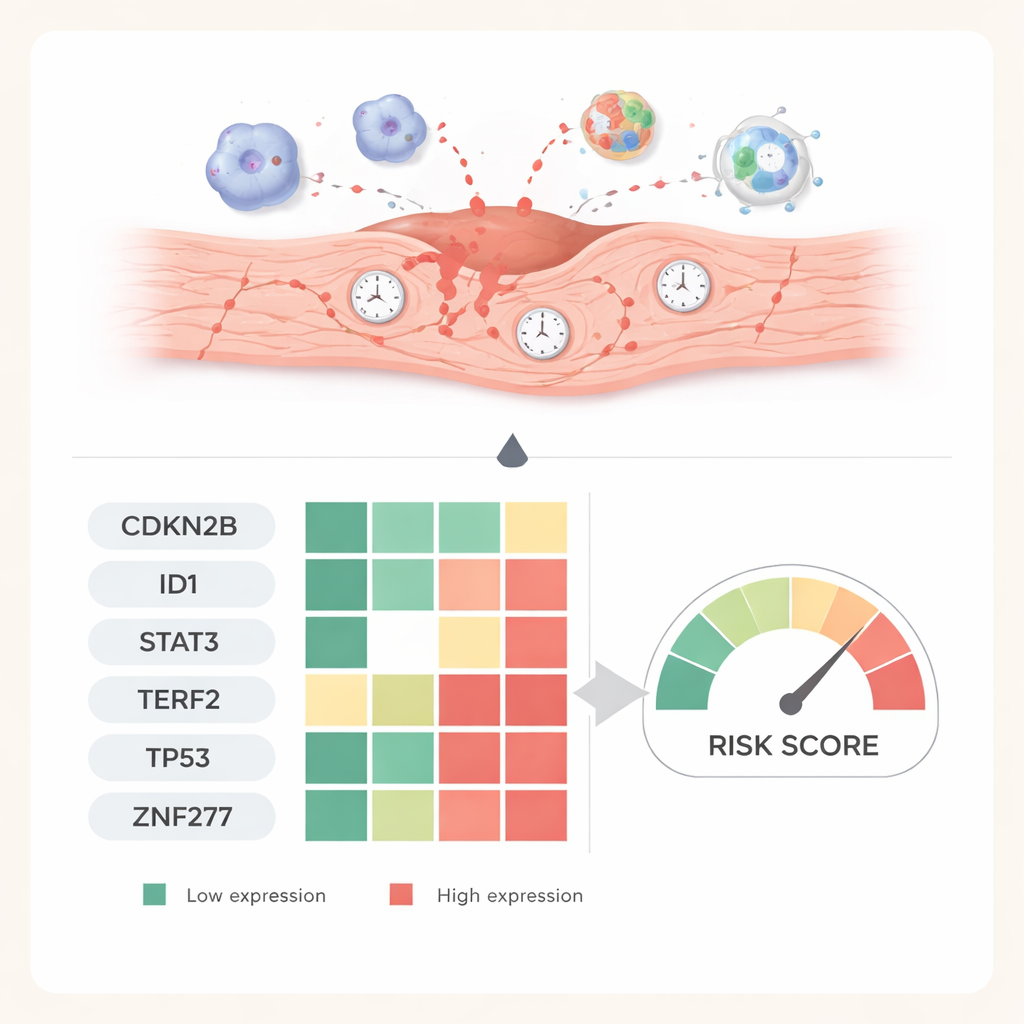
Das previsões computacionais aos corações vivos
Para testar se esses seis genes têm relevância além das telas de computador, os pesquisadores criaram um modelo de camundongo de lesão por isquemia–reperfusão. Eles mediram a atividade gênica em diferentes momentos após a restauração do fluxo sanguíneo e usaram colorações teciduais para visualizar as proteínas correspondentes em fatias cardíacas. Um gene, CDKN2B, aumentou de forma contínua ao longo de uma semana, sugerindo que ajuda a trancar as células danificadas em um estado senescente de longo prazo. Outros, incluindo ID1, STAT3, TP53, TERF2 e ZNF277, caíram abruptamente no início e depois se recuperaram gradualmente, espelhando mudanças entre estresse agudo, dano ativo e reparo posterior. Esses padrões dependentes do tempo sustentam a ideia de que cada gene captura uma fase diferente da resposta do coração.
O que isso pode significar para os pacientes
Para um público leigo, a mensagem principal é que o estudo conecta o dano relacionado a infarto à biologia do envelhecimento celular e identifica uma “impressão digital” de seis genes que sinaliza esse dano em modelos experimentais. Embora o trabalho ainda seja pré‑clínico e baseado principalmente em dados de camundongos e bancos públicos, ele oferece um roteiro para novos exames sanguíneos ou de tecido que poderiam detectar lesão por isquemia–reperfusão mais cedo e com mais especificidade do que as ferramentas atuais. A longo prazo, entender como esses genes relacionados ao envelhecimento regulam inflamação, cicatrização e reparo pode abrir portas para tratamentos que não apenas desobstruam artérias bloqueadas, mas também ajudem o coração revascularizado a se recuperar de forma mais completa.
Citação: Sun, L., Liu, H., Jia, T. et al. The role of cellular senescence-related genes in ischemia–reperfusion injury and the identification of their biomarkers. Sci Rep 16, 5211 (2026). https://doi.org/10.1038/s41598-026-36076-2
Palavras-chave: lesão por isquemia reperfusão, senescência celular, infarto, biomarcadores, inflamação imune