Clear Sky Science · pt
Expressão de ACE2 por células epiteliais colônicas está associada à infecção viral, imunidade e metabolismo energético
Por que o intestino importa em um vírus respiratório
Quando pensamos na COVID-19, imaginamos pulmões cheios de líquido e pacientes com dificuldade para respirar. No entanto, muitas pessoas infectadas pelo SARS-CoV-2 também desenvolvem dor abdominal, diarreia e problemas intestinais de longa duração. Este estudo investiga por que o intestino — especialmente o cólon — pode ser um alvo importante do vírus. Ao analisar células individuais do cólon de crianças, os pesquisadores mostram que uma porta de entrada viral chave, a proteína ACE2, é altamente ativa em células intestinais específicas e está ligada não apenas à infecção viral, mas também às nossas defesas imunes e à forma como as células gerenciam energia.
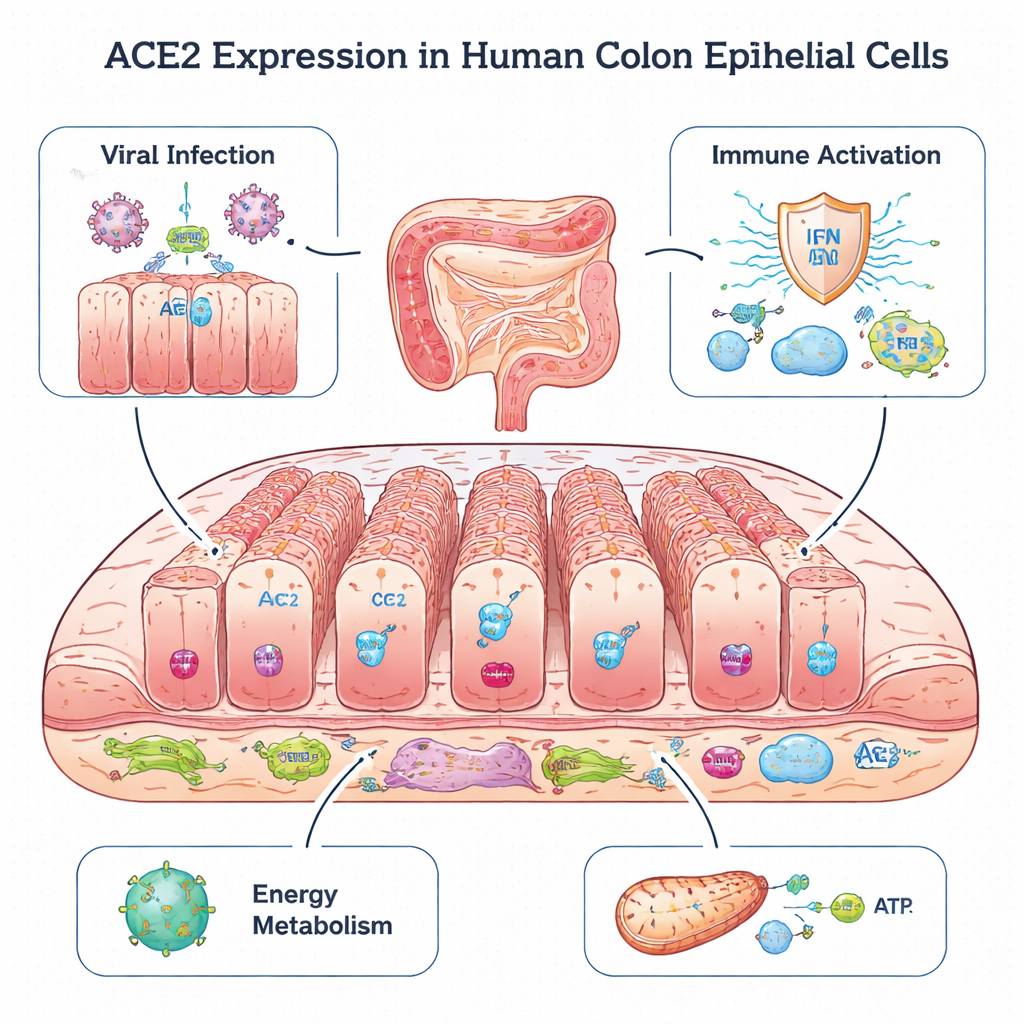
Uma porta celular no cólon
ACE2 é mais conhecida como o principal ponto de entrada que tanto o vírus SARS original quanto o SARS-CoV-2 usam para infectar células no pulmão. Paradoxalmente, estudos em animais sugerem que a ACE2 também pode proteger os tecidos contra danos, ajudando a manter em equilíbrio um sistema hormonal que controla a pressão arterial. No intestino, já se sabe que a ACE2 apoia um microbioma saudável e previne inflamação. Neste trabalho, os cientistas reanalisaram dados de sequenciamento de RNA de célula única (single-cell RNA-seq) de biópsias de cólon de 17 crianças: algumas com intestinos saudáveis e outras com colite ou doença inflamatória intestinal, incluindo retocolite ulcerativa e doença de Crohn. Essa técnica permitiu ver quais genes estão ativos em milhares de células individuais e localizar exatamente onde a ACE2 está ligada.
Colonócitos: alvos preferenciais e primeiros respondedores
A análise revelou que a ACE2 está concentrada quase exclusivamente em colonócitos, um tipo importante de célula epitelial que reveste o interior do cólon e fica voltada para o conteúdo intestinal. Em comparação com outras células epiteliais, os colonócitos também mostraram maior atividade de genes que ajudam os vírus a entrar nas células, brotar e sair. Ao mesmo tempo, essas células expressaram muitos genes envolvidos na detecção de material genético viral e na ativação de respostas de interferon do tipo I e tipo III — sistemas de alarme precoce essenciais da defesa imune. Elas também produziram sinais inflamatórios e moléculas que apresentam fragmentos virais às células T, o que sugere que os colonócitos são tanto potenciais alvos virais quanto sentinelas iniciais importantes que alertam o sistema imune.
Redes conectadas de imunidade e uso de energia
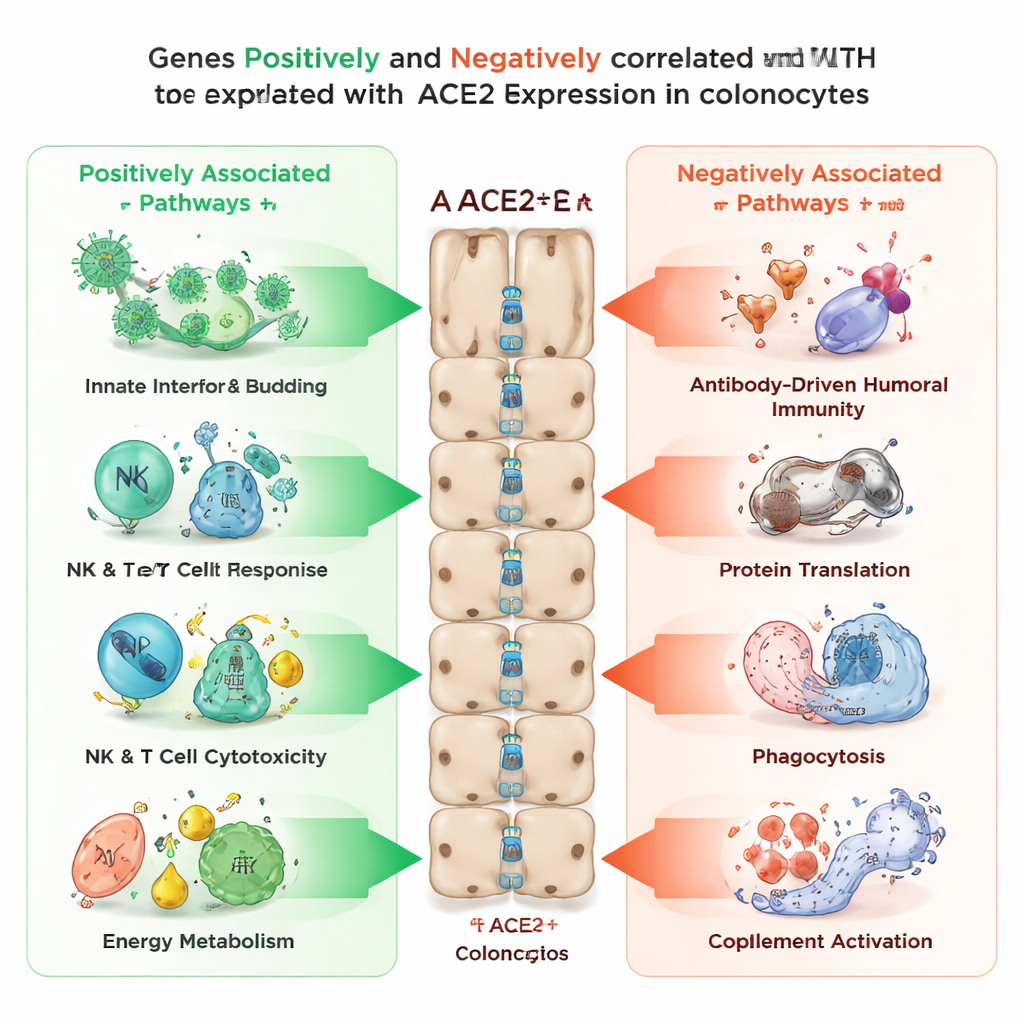
Os pesquisadores então investigaram quais outros genes tendem a ser ligados ou desligados em conjunto com a ACE2 nos colonócitos. Encontraram mais de 3.400 genes cuja expressão aumentava com os níveis de ACE2 e mais de 2.100 que diminuíam à medida que a ACE2 aumentava. Genes que se correlacionaram positivamente com a ACE2 estavam enriquecidos em processos relacionados à entrada e liberação viral, sinalização imune inata, atividade citotóxica de células natural killer e células T, e várias vias de produção de energia dentro das células, incluindo função mitocondrial e processamento de gorduras e açúcares. Em contraste, genes que se moviam na direção oposta — altos quando a ACE2 estava baixa — estavam associados à imunidade baseada em anticorpos (humoral), à maquinaria de síntese proteica da célula, a processos de “comer célula” como a fagocitose, e ao sistema complemento, outro braço da defesa imune. Esse padrão sugere que a ACE2 marca um estado em que os colonócitos estão sintonizados para uma detecção antiviral rápida e produção de energia, enquanto outros programas imunes mais lentos ficam suprimidos.
Evidência de intestinos inflamados
Para verificar se esses padrões ocorrem em tecidos reais, a equipe usou imunofluorescência multiplex — uma técnica que ilumina proteínas específicas com cores diferentes — em amostras de cólon de crianças com retocolite ulcerativa, doença de Crohn e de controles. Confirmaram que a proteína ACE2 se localiza principalmente em células epiteliais marcadas por EPCAM. Em pacientes com doença inflamatória intestinal, células positivas para ACE2 mostraram níveis mais altos de IFNA4 e RSAD2, duas proteínas fortemente associadas à sinalização por interferon e à atividade antiviral. Isso indica que, no intestino inflamado, as células colonocíticas que exprimem ACE2 não são apenas portas de entrada potenciais para vírus; elas também são pontos de intensa resposta antiviral.
O que isso significa para pacientes e terapias futuras
Para leigos, a mensagem é que o cólon não é um espectador passivo na COVID-19. A mesma proteína que permite a entrada do vírus nas células também ajuda a coordenar a imunidade intestinal e o uso de energia, especialmente em crianças com inflamação intestinal pré-existente. Esse papel duplo pode ajudar a explicar por que alguns pacientes desenvolvem sintomas gastrointestinais e por que pessoas com doença inflamatória intestinal têm desfechos complexos, mas não uniformemente piores, durante a COVID-19. O trabalho também alimenta discussões mais amplas sobre fármacos que atuam em vias de coagulação e pressão arterial, alguns dos quais podem reduzir danos pulmonares e vasculares em infecções graves. Embora o estudo se baseie em correlações e não possa provar causa e efeito, ele destaca as células colonocíticas ricas em ACE2 como atores importantes na interseção entre entrada viral, defesa imune e metabolismo — apontando o intestino como um campo-chave e potencialmente tratável na doença por coronavírus.
Citação: Qi, Y., Huang, Y., Chen, H. et al. ACE2 expression by colonic epithelial cells is associated with viral infection, immunity, and energy metabolism. Sci Rep 16, 5738 (2026). https://doi.org/10.1038/s41598-026-36052-w
Palavras-chave: ACE2, colonócitos, COVID-19 intestinal, doença inflamatória intestinal, imunidade antiviral