Clear Sky Science · pt
Classificação da gravidade da demência relacionada ao Alzheimer a partir de imagens por ressonância magnética usando otimização sem derivadas de rede neural convolucional
Ajudando médicos a detectar demência mais cedo
Com o envelhecimento das populações, muitas famílias se preocupam com perda de memória e demência. Exames cerebrais podem revelar alterações precoces associadas à doença de Alzheimer, mas ler milhares de imagens manualmente é lento e difícil, mesmo para especialistas. Este estudo apresenta uma ferramenta computacional inteligente que analisa ressonâncias magnéticas do cérebro e classifica as pessoas em quatro níveis de gravidade da demência, de sem demência a comprometimento moderado. O sistema foi projetado para ser ao mesmo tempo extremamente preciso e leve o suficiente para rodar em computadores comuns de hospitais, tornando a análise avançada de imagens mais acessível.
Um novo assistente inteligente para exames cerebrais
Os pesquisadores concentram-se em um tipo de inteligência artificial chamado rede neural convolucional, ou CNN, que se destaca em identificar padrões em imagens. Em vez de apenas decidir se alguém tem Alzheimer, a ferramenta distingue quatro estágios: sem demência, muito leve, leve e moderada. Para isso, a equipe treinou o modelo em grandes coleções públicas de ressonâncias magnéticas já rotuladas por especialistas. O objetivo era duplo: alcançar precisão quase perfeita e manter o modelo compacto e rápido, para que fosse prático para uso clínico cotidiano, e não apenas para laboratórios de pesquisa bem financiados.
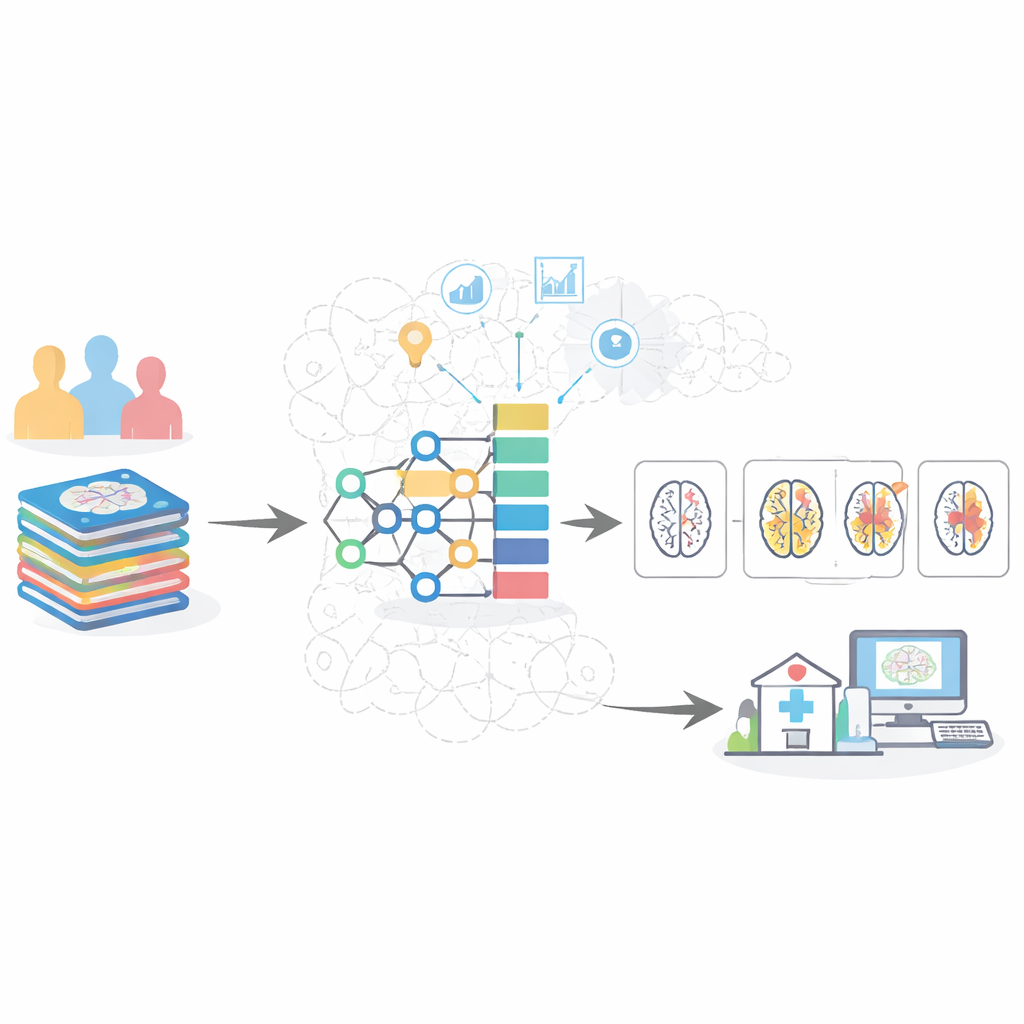
Balanceando os dados e limpando as imagens
Um desafio central em dados médicos é que nem todos os estágios da doença estão igualmente representados. Nessas coleções de exames cerebrais, casos saudáveis e muito leves são comuns, enquanto imagens de demência moderada são muito mais raras. Sistemas de IA padrão tendem então a “jogar pelo seguro”, superestimando as classes comuns e perdendo casos iniciais ou moderados. Para contrabalançar isso, os autores usaram uma estratégia em duas etapas: primeiro removeram imagens limítrofes e confusas e em seguida criaram exemplos sintéticos realistas dos estágios sub-representados. Paralelamente, prepararam cuidadosamente cada fatia de RM filtrando, isolando o cérebro dos tecidos circundantes e normalizando brilho e contraste para que o modelo pudesse focar em características medicamente relevantes, como redução de estruturas profundas da memória e alargamento de espaços preenchidos por fluido.
Projetando uma rede menor e mais inteligente
Em vez de depender de métodos tradicionais de treinamento que ajustam parâmetros seguindo gradientes matemáticos, a equipe usou um conjunto de técnicas chamadas otimização sem derivadas. Começaram com uma CNN convencional maior e então empregaram busca evolutiva e busca de arquitetura neural para evoluir um desenho mais simples com apenas três camadas convolucionais e bem menos filtros. Otimização bayesiana afinou em seguida como a rede deveria ser treinada, enquanto recozimento simulado e poda removeram conexões desnecessárias após o treinamento. O resultado final, chamado DAPA-CNN, tem aproximadamente 85% menos parâmetros ajustáveis do que o modelo inicial, usa cerca de um quarto da memória e treina em menos de dois terços do tempo, mas ainda assim captura os padrões cruciais das imagens.
Desempenho quase perfeito e explicações visuais claras
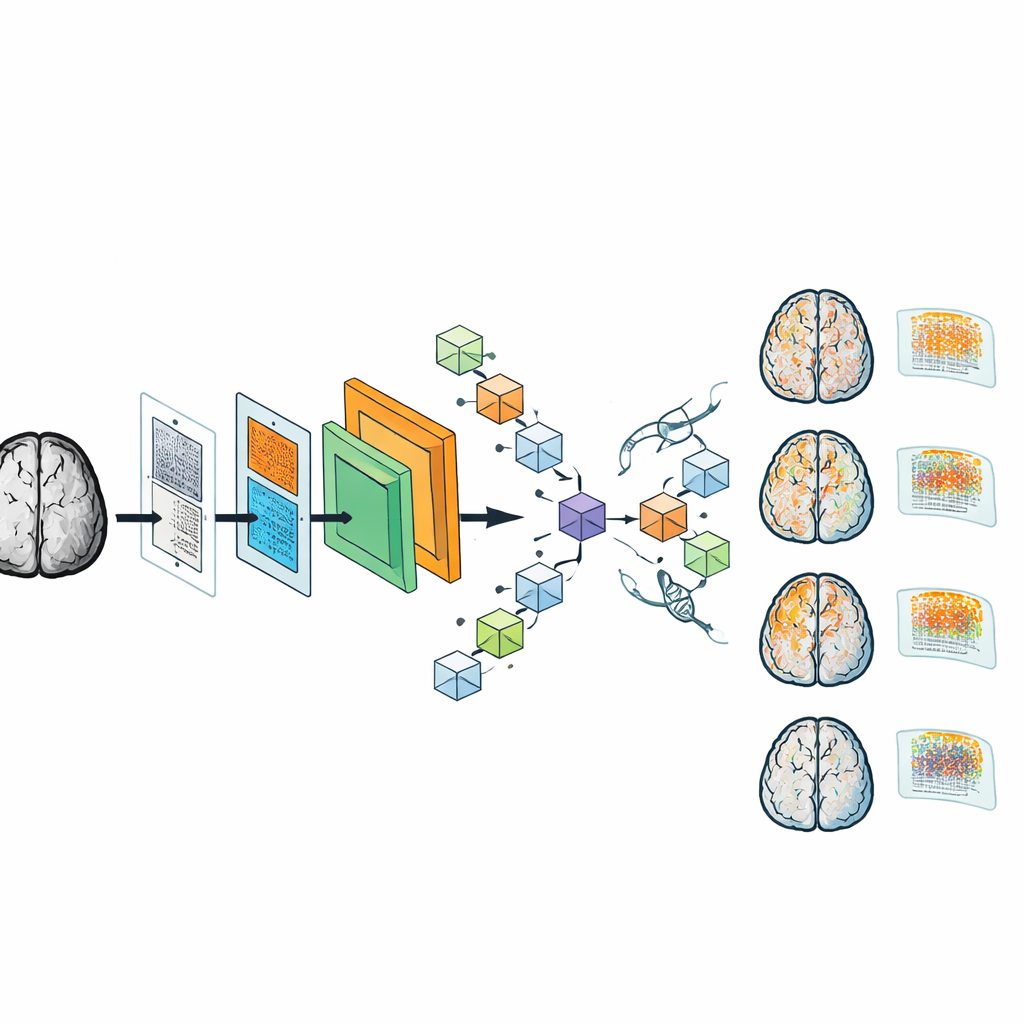
Apesar do tamanho reduzido, o DAPA-CNN mostrou-se notavelmente preciso. Em um grande conjunto de dados de Alzheimer, classificou corretamente o estágio da demência em quase todos os casos, com acurácia e outras métricas de desempenho rondando 99%. O modelo também generalizou bem para um conjunto de dados multicêntrico separado, coletado em scanners diferentes, sugerindo robustez às variações reais na imagem. Para tornar o sistema mais transparente para os clínicos, os autores geraram mapas de ativação de classe — sobreposições semelhantes a mapas de calor que mostram quais regiões do cérebro influenciaram determinada decisão. Em estágios iniciais, esses mapas enfatizam áreas envolvidas na memória que se sabe deteriorarem primeiro na doença de Alzheimer; em estágios avançados, eles se expandem para regiões corticais mais amplas, alinhando-se ao entendimento clínico da progressão da doença.
O que isso significa para pacientes e clínicas
Para não especialistas, a principal mensagem é que o estudo oferece uma ferramenta rápida, compacta e interpretável para avaliar a gravidade da demência a partir de ressonâncias magnéticas de rotina. Ao balancear os dados de treinamento e modelar cuidadosamente a rede com otimização sem derivadas, os autores criaram um modelo capaz de rodar em hardware modesto, entregando acurácia próxima da perfeição e destacando as regiões cerebrais por trás de suas decisões. Se confirmado em futuros ensaios clínicos prospectivos, tal tecnologia poderia apoiar diagnósticos mais precoces, estadiamento mais consistente entre hospitais e melhor acompanhamento de como a doença de Alzheimer altera o cérebro ao longo do tempo.
Citação: Ganesan, S.K., Velusamy, P., Parthsarathy, P. et al. Alzheimer’s related dementia severity classification from magnetic resonance imaging using derivative-free optimization of convolutional neural network. Sci Rep 16, 10077 (2026). https://doi.org/10.1038/s41598-026-36037-9
Palavras-chave: doença de Alzheimer, RM do cérebro, estadiamento da demência, aprendizado profundo, IA em imagens médicas