Clear Sky Science · pt
Aprendizado auto-supervisionado em grafos prevê associações entre RNA não codificante e doenças
Por que o RNA oculto importa para nossa saúde
A maioria de nós aprendeu que a principal função do RNA é ajudar a construir proteínas. Mas na última década, cientistas descobriram vastas quantidades de RNAs “não codificantes” que nunca se tornam proteínas e, ainda assim, ajudam a controlar como nossas células funcionam. Muitas dessas moléculas hoje são conhecidas por promover ou suprimir cânceres e outras doenças complexas. Descobrir quais RNAs não codificantes estão ligados a quais doenças pode revelar novas formas de diagnosticar doenças precocemente ou projetar tratamentos mais precisos — mas testar todas as possibilidades no laboratório seria impossivelmente lento. Este estudo apresenta um método computacional poderoso que pode vasculhar enormes redes biológicas e propor de forma confiável as conexões RNA–doença mais promissoras para os pesquisadores verificarem em experimentos.
De lixo a peças-chave celulares
Por anos, os RNAs não codificantes foram descartados como restos sem significado da atividade gênica. Hoje sabemos que famílias como microRNAs, longos RNAs não codificantes e RNAs circulares ajudam a orquestrar processos vitais, desde o empacotamento do DNA até ligar e desligar genes e retransmitir sinais dentro das células. Como atuam em tantos pontos de controle, até pequenas alterações nesses RNAs podem desequilibrar o sistema a favor do câncer ou de outras doenças. Clínicos já começaram a vê-los como potenciais biomarcadores e alvos para medicamentos. O desafio é a escala: existem milhares de RNAs diferentes e centenas de doenças, e experimentos tradicionais para testar cada ligação possível são caros e demoram. É aí que a predição computacional entra, oferecendo um modo de reduzir o espaço de busca.
Como ler uma rede biológica
Métodos computacionais anteriores tentaram prever ligações RNA–doença dividindo grandes tabelas de dados em peças mais simples ou treinando modelos de aprendizado de máquina em exemplos conhecidos. Essas abordagens ajudaram, mas frequentemente ignoravam como RNAs e doenças estão entrelaçados em redes. As modernas “redes neurais gráficas” tratam RNAs e doenças como pontos conectados por linhas, muito parecido com uma rede social. Elas podem aprender padrões sobre quem está ligado a quem. No entanto, a maioria desses métodos em grafos precisa de muitos exemplos de treinamento confiáveis e de muitos atributos de entrada cuidadosamente escolhidos. Isso os torna sensíveis a dados ausentes, medições ruidosas e sobreajuste — performando bem nos dados conhecidos, mas falhando ao prever associações novas.
Aprendendo a partir dos próprios dados
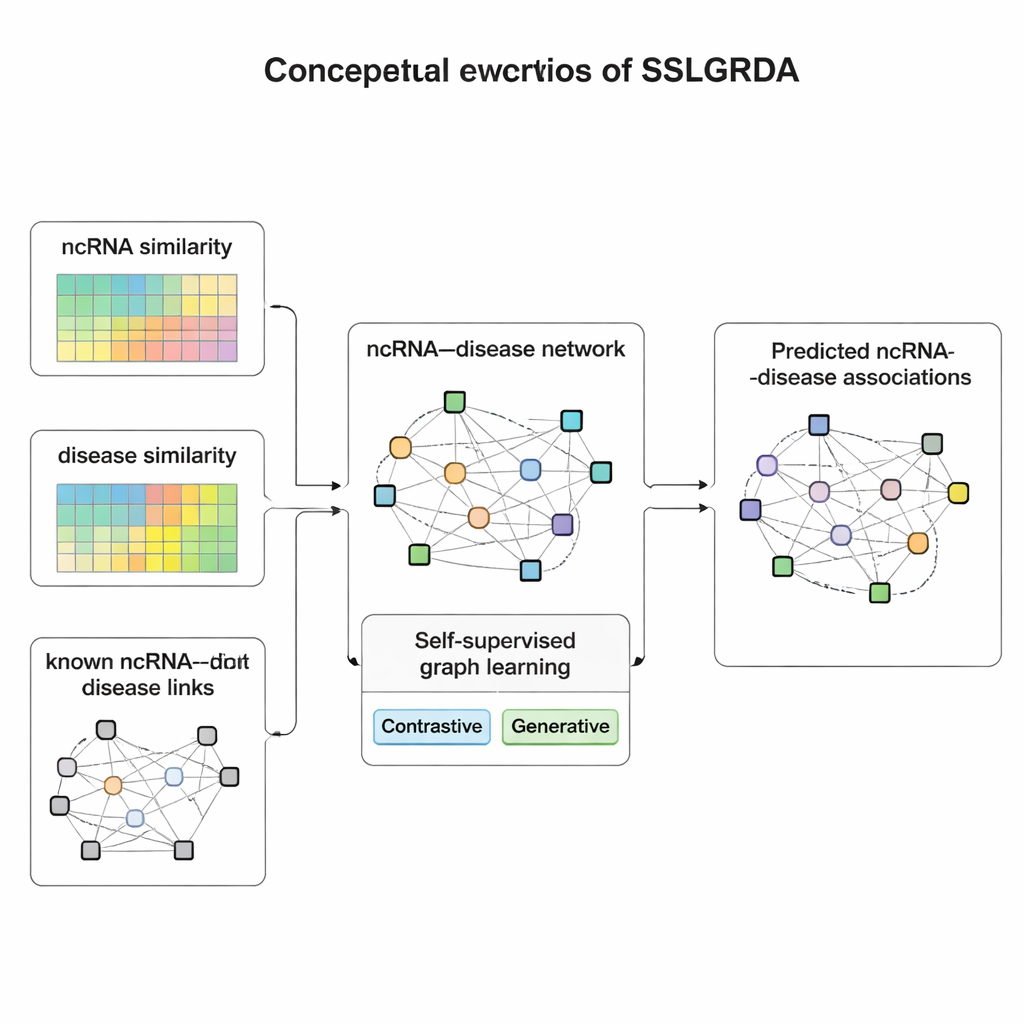
Os autores apresentam o SSLGRDA, uma nova estrutura que ensina um modelo em grafo a aprender padrões úteis sem depender fortemente de dados rotulados. A ideia-chave é o “aprendizado auto-supervisionado”: em vez de ser informado sobre qual RNA emparelha com qual doença, o modelo inventa suas próprias tarefas de prática baseadas apenas na estrutura e nos atributos da rede. Os pesquisadores constroem dois tipos de grafos. Um mantém RNAs e doenças como tipos de nós diferentes conectados por ligações conhecidas. O outro os mistura em uma única grande rede que também inclui informações de similaridade — o quanto dois RNAs ou duas doenças são parecidos — de modo que itens com poucas conexões ganhem vizinhos de suporte. Sobre esses grafos, o SSLGRDA usa dois estilos de auto-treinamento. Estratégias contrastivas pedem ao modelo que reconheça que diferentes “visões” de um mesmo nó (por exemplo, suas conexões versus seus atributos) devem levar a representações internas semelhantes, ao mesmo tempo que separam claramente nós não relacionados. Estratégias generativas escondem deliberadamente partes das características de entrada e desafiam o modelo a reconstruí-las, encorajando-o a capturar uma estrutura mais profunda em vez de memorizar ruído.
Colocando o método à prova
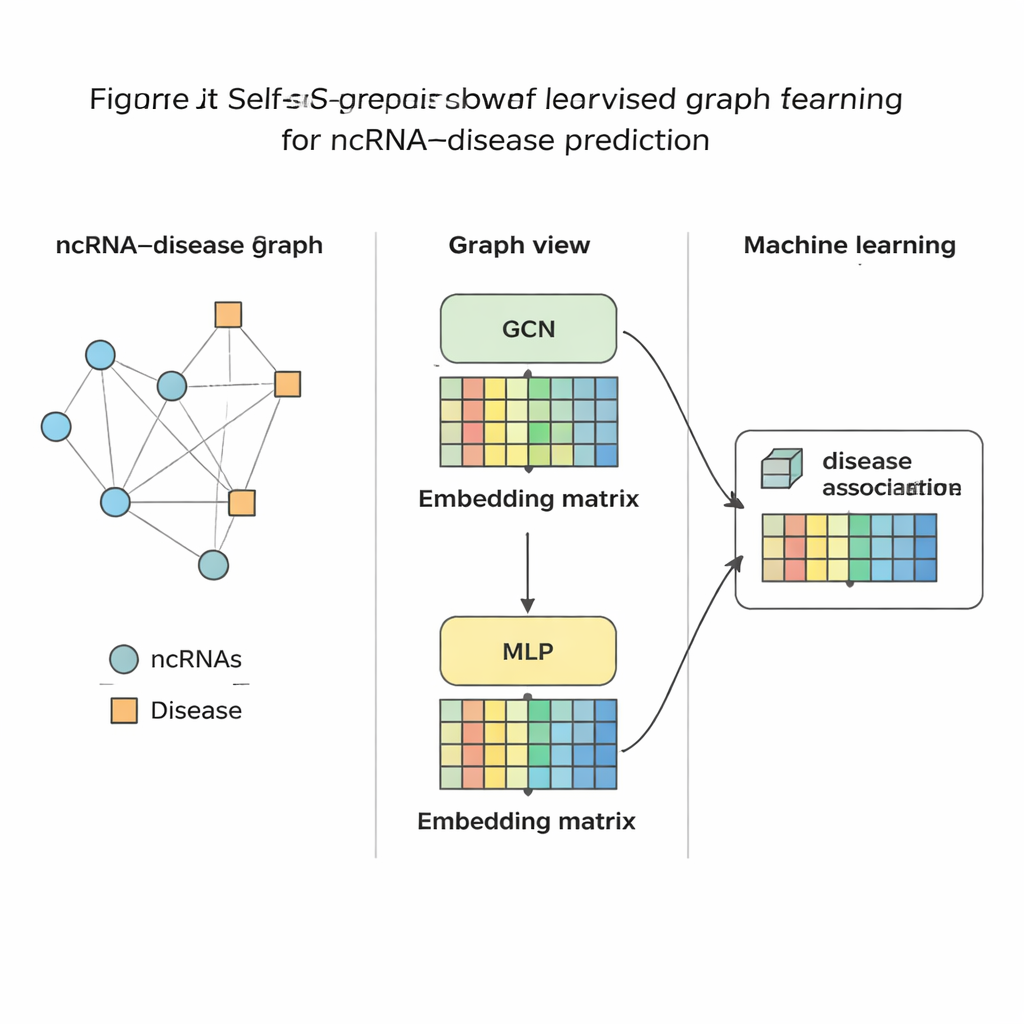
Uma vez que o SSLGRDA destila cada RNA e cada doença em uma impressão digital numérica compacta, um classificador padrão de aprendizado de máquina é treinado para julgar se um vínculo entre eles é provável ou não. Os autores avaliaram essa abordagem em nove conjuntos de dados diferentes cobrindo três tipos principais de RNA e centenas de doenças. Em toda a avaliação, suas variantes auto-supervisionadas contrastivas no grafo misto (homogêneo) tiveram o melhor desempenho, superando uma gama de ferramentas existentes, incluindo fortes linhas de base baseadas em grafos. O método não apenas alcançou maior precisão em testes globais, como também classificou os parceiros corretos no topo quando se focalizou em um RNA ou em uma doença de cada vez — crucial para uso no mundo real, em que um biólogo pode começar a partir de um único câncer e perguntar quais RNAs estudar. Eles também mostraram que as mesmas ideias se transferem bem para outras redes biomédicas, como aquelas que conectam microrganismos a doenças ou a fármacos.
Das predições a potenciais terapias
Para demonstrar valor prático, a equipe aplicou o SSLGRDA para buscar novos RNAs não codificantes envolvidos no câncer de mama, câncer de cólon e várias outras condições. Muitas das sugestões mais bem classificadas foram posteriormente confirmadas em bases de dados independentes ou relatórios científicos, apoiando a capacidade do modelo de identificar padrões biologicamente relevantes. Para não especialistas, a conclusão é que este trabalho fornece uma maneira mais inteligente de minerar o emaranhado cada vez maior de dados biológicos em busca de pistas ocultas sobre doenças. Ao aprender automaticamente como RNAs e doenças se agrupam e interagem, métodos em grafos auto-supervisionados como o SSLGRDA podem guiar pesquisadores de laboratório para os alvos mais promissores, potencialmente acelerando o caminho dos dados brutos para diagnósticos e tratamentos melhores.
Citação: Wu, Q., Tang, S. Self-supervised learning on graphs predicts non-coding RNA and disease associations. Sci Rep 16, 5231 (2026). https://doi.org/10.1038/s41598-026-36030-2
Palavras-chave: RNA não codificante, associação com doenças, redes neurais gráficas, aprendizado auto-supervisionado, biologia computacional