Clear Sky Science · pt
Efeitos do emaranhamento molecular na estabilidade de proteínas em um proteoma bacteriano
Por que a vida lotada das proteínas importa
Dentro de cada célula viva, as proteínas cumprem suas funções em um espaço tão cheio de outras moléculas que quase metade do volume pode estar ocupada. Ainda assim, a maioria dos experimentos de laboratório estuda proteínas em soluções diluídas, quase vazias. Este artigo faz uma pergunta simples, mas importante: como essa realidade congestionada altera a estabilidade e o comportamento das proteínas, e o que isso significa para o funcionamento da vida em escala molecular?
Espiando um mundo celular apertado
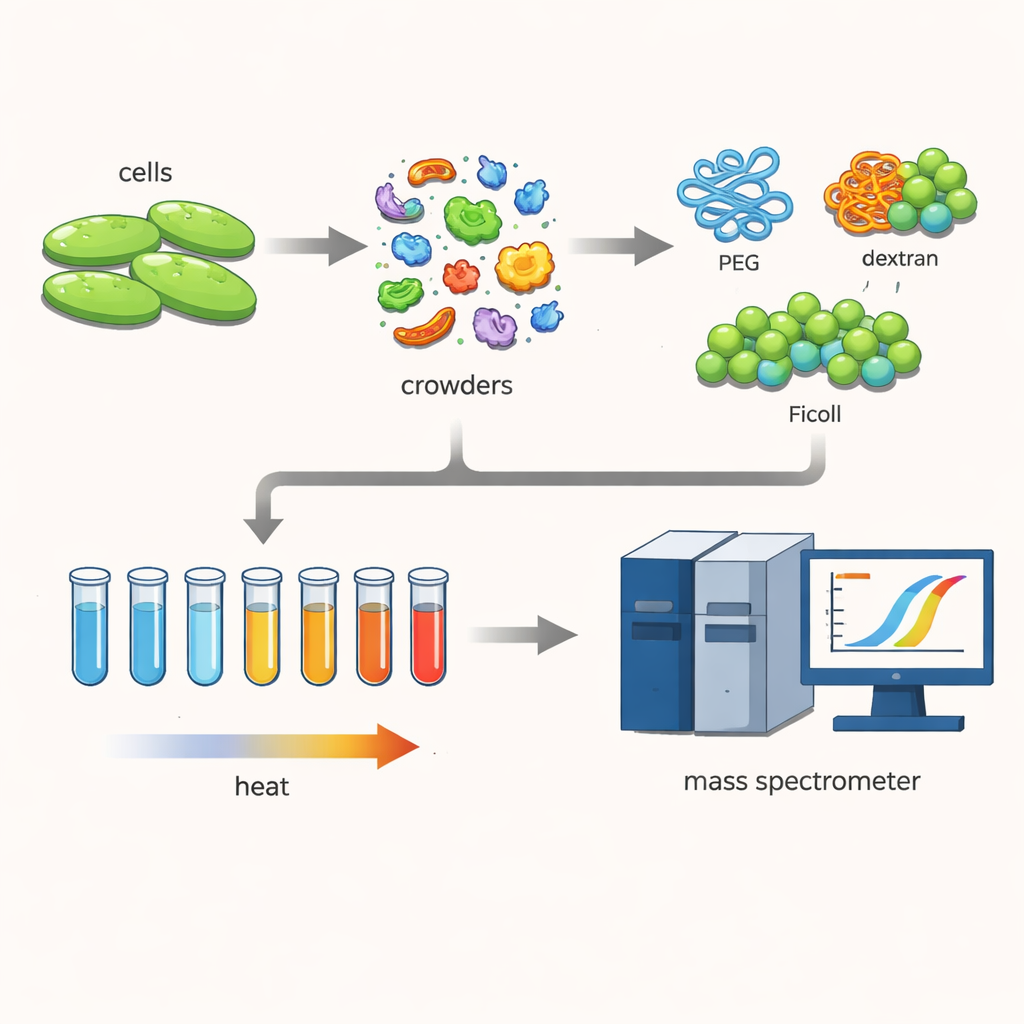
Para investigar isso, os pesquisadores trabalharam com uma bactéria chamada Cupriavidus necator, um microrganismo de interesse para tecnologias verdes, como captura de carbono e produção de bioplásticos. Eles romperam as células de forma suave, mantendo centenas de proteínas próximas de suas formas naturais. Em seguida, adicionaram altas concentrações de polímeros grandes e hidrofílicos—agentes de “emaranhamento” comuns chamados PEG, dextrana e Ficoll—frequentemente usados para imitar o interior denso das células.
Observando as proteínas derreterem
A equipe usou uma técnica conhecida como perfilagem térmica do proteoma. Eles aqueceram muitas amostras pequenas da mistura de proteínas em etapas, de 30 a 70 graus Celsius. À medida que a temperatura subia, proteínas menos estáveis se desnaturavam e agregavam, saindo da solução. Ao marcar as proteínas solúveis remanescentes e medi‑las com um espectrômetro de massa sensível, os cientistas puderam reconstruir curvas de fusão para cada proteína e determinar sua temperatura de fusão—o ponto em que metade deixou o estado solúvel e funcional. Comparar essas temperaturas com e sem os agentes de emaranhamento revelou como o ambiente denso deslocou a estabilidade das proteínas.
Um quadro misto: algumas proteínas mais firmes, outras mais frágeis
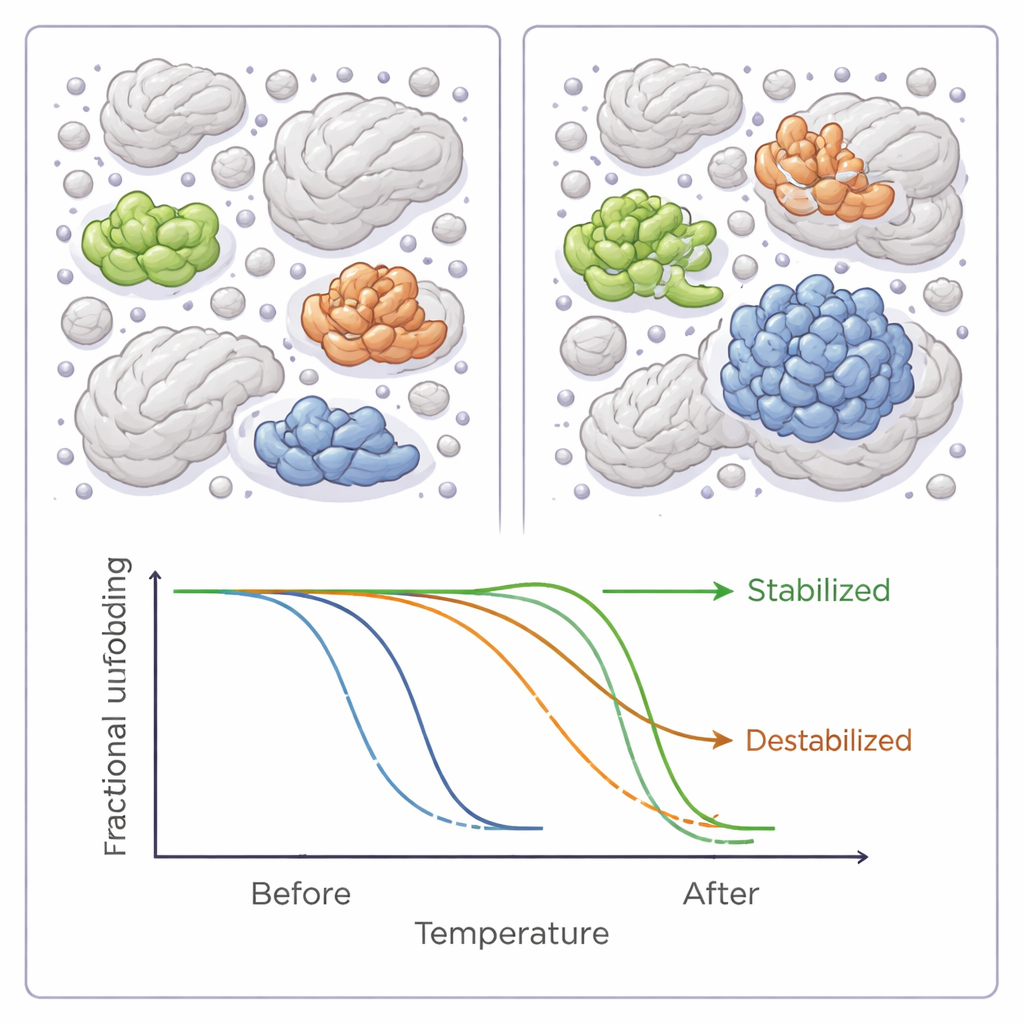
Em média, a adição de qualquer um dos seis polímeros reduziu as temperaturas de fusão em todo o proteoma bacteriano, sugerindo um leve efeito global de desestabilização. Mas essa tendência geral ocultou uma história muito mais sutil. Para dezenas de proteínas individuais, os agentes de emaranhamento ou claramente aumentaram ou diminuíram a estabilidade, às vezes em vários graus. A maioria das proteínas foi afetada por apenas um dos seis reagentes, mas um punhado respondeu a vários, e quase todas essas responderam de forma consistente—ou estabilizadas ou desestabilizadas—sugerindo características subjacentes compartilhadas na forma como interagem com os crowders.
O que faz uma proteína ganhar ou perder em uma multidão
Quando os autores analisaram mais de perto as propriedades dessas proteínas sensíveis, padrões emergiram. Proteínas que se tornaram mais estáveis em condições de maior emaranhamento tendiam a ser mais hidrofóbicas—isto é, apresentavam superfícies mais repelentes de água—e eram com mais frequência enzimas clássicas com sítios ativos bem definidos. Também era mais provável que estivessem envolvidas em interações proteína‑proteína ou apresentassem modificações químicas que ajustam sua função. Proteínas desestabilizadas, em contraste, eram em média menores e menos decoradas com tais modificações. Esses achados ecoam modelos computacionais e outros experimentos que sugerem que o emaranhamento pode favorecer certas proteínas enquanto torna outras mais vulneráveis, dependendo do tamanho, forma e de como normalmente interagem com parceiros.
Além do simples aperto: como os crowders realmente atuam
Explicações tradicionais para o emaranhamento molecular focam no “volume excluído”, a ideia de que moléculas grandes simplesmente deixam menos espaço, empurrando proteínas a permanecer dobradas. Se essa fosse toda a história, esperar‑se‑ia que os agentes de emaranhamento principalmente estabilizassem proteínas e que houvesse fortes ligações com o quão volumosos ou viscosos os polímeros são. Em vez disso, os autores observaram apenas conexões fracas com o tamanho e a espessura dos polímeros. Seus dados se ajustaram melhor a uma imagem de “exclusão preferencial”: crowders e proteínas evitam‑se quimicamente, o que indiretamente favorece certos estados dobrados, mas também pode perturbar interações delicadas que mantêm outras proteínas estáveis. Em suma, não é apenas um aperto físico, mas um sutil empurrar e puxar químico que molda o comportamento das proteínas.
O que isso significa para entender a química da vida
Para não especialistas, a mensagem chave é que proteínas dentro das células não podem ser completamente compreendidas isoladamente, nadando em tampões claros. A selva molecular densa ao redor pode tornar algumas proteínas mais resistentes e outras mais frágeis, alterando como redes inteiras de reações se comportam. Este estudo, ao medir mudanças de estabilidade para centenas de proteínas ao mesmo tempo, mostra que os efeitos do emaranhamento são complexos e específicos por proteína, e provavelmente dirigidos por interações diretas tanto quanto pelo simples empacotamento. À medida que pesquisadores projetam medicamentos, enzimas industriais ou micróbios engenheirados, reconhecer essa realidade lotada será crucial para prever como as proteínas realmente se comportam em sistemas vivos.
Citação: McKeever, K., Dillon, E.T., Wynne, K. et al. Molecular crowding effects on protein stability in a bacterial proteome. Sci Rep 16, 5908 (2026). https://doi.org/10.1038/s41598-026-35990-9
Palavras-chave: emaranhamento molecular, estabilidade de proteínas, perfilagem térmica do proteoma, proteoma bacteriano, ambiente celular