Clear Sky Science · pt
Deficiência de Negr1 altera sinalização do glutamato e a via da quinurenina em um modelo murino de transtornos psiquiátricos
Por que este estudo cerebral importa
Muitas doenças mentais comuns, da depressão à esquizofrenia, estão ligadas a mudanças sutis em como as células cerebrais se comunicam. Este estudo investiga um gene de risco, chamado NEGR1, em camundongos para ver como sua perda altera a química e o comportamento cerebral. Ao acompanhar como esses animais se movem após um fármaco que interrompe brevemente um receptor cerebral chave, e ao medir compostos químicos relacionados no cérebro, os pesquisadores revelam como genética, sexo e metabolismo cerebral podem se combinar para moldar a vulnerabilidade a transtornos psiquiátricos.
Um gene que mantém os sinais cerebrais em equilíbrio
O gene NEGR1 produz uma proteína de superfície celular que ajuda os neurônios a formar e estabilizar conexões. Trabalhos anteriores mostraram que remover esse gene em camundongos altera a estrutura cerebral, reduz certas conexões inibitórias (GABA) e modifica respostas a fármacos ligados à dopamina, como a anfetamina. Como essas mudanças indicam um deslocamento em direção a sinais excitatórios mais fortes, a equipe focou em outro grande sistema excitatório: o glutamato e seus receptores NMDA, centrais para aprendizagem, memória e comportamento flexível. Eles também examinaram a “via da quinurenina”, uma rota metabólica que quebra o aminoácido triptofano em compostos que podem tanto fortalecer quanto bloquear os receptores NMDA.
Testando o comportamento com um fármaco alucinógeno
Para sondar a função dos receptores NMDA, os pesquisadores usaram MK-801, um fármaco conhecido que bloqueia brevemente esses receptores e pode mimetizar aspectos do desequilíbrio do glutamato observados em condições psiquiátricas. Camundongos machos e fêmeas carregavam o gene Negr1 normal ou não o possuíam. Os animais receberam injeções diárias de MK-801 e foram testados em uma arena de campo aberto, onde foram monitorados automaticamente o movimento total, o tempo nos cantos e rotações semelhantes a giros. Em machos sem exposição prévia ao fármaco, uma única dose de MK-801 provocou um surto de atividade mais intenso nos camundongos deficientes em Negr1 do que nos normais, sugerindo que seus cérebros eram incomumente sensíveis a essa perturbação da sinalização do glutamato.
Um padrão surpreendente de tolerância rápida
Quando o MK-801 foi administrado repetidamente, o padrão mudou. Nos machos, a atividade teve picos em alguns dias, mas caiu a cada segundo dia, formando um padrão em zigue-zague que sugeria tolerância rápida e parcial aos efeitos do fármaco. Ao longo de nove dias, machos normais mostraram uma resposta crescente consistente com sensibilização, enquanto machos deficientes em Negr1 exibiram uma construção atenuada de atividade e variações menos marcantes dia a dia, indicando sensibilidade alterada dos receptores NMDA. As fêmeas de ambos os genótipos se adaptaram ainda mais rápido: por volta do quinto dia, o MK-801 deixou de produzir fortes efeitos comportamentais, então o tratamento foi interrompido. Em todas as medidas, o sexo teve grande influência, e efeitos claros do genótipo apareceram principalmente nos machos.
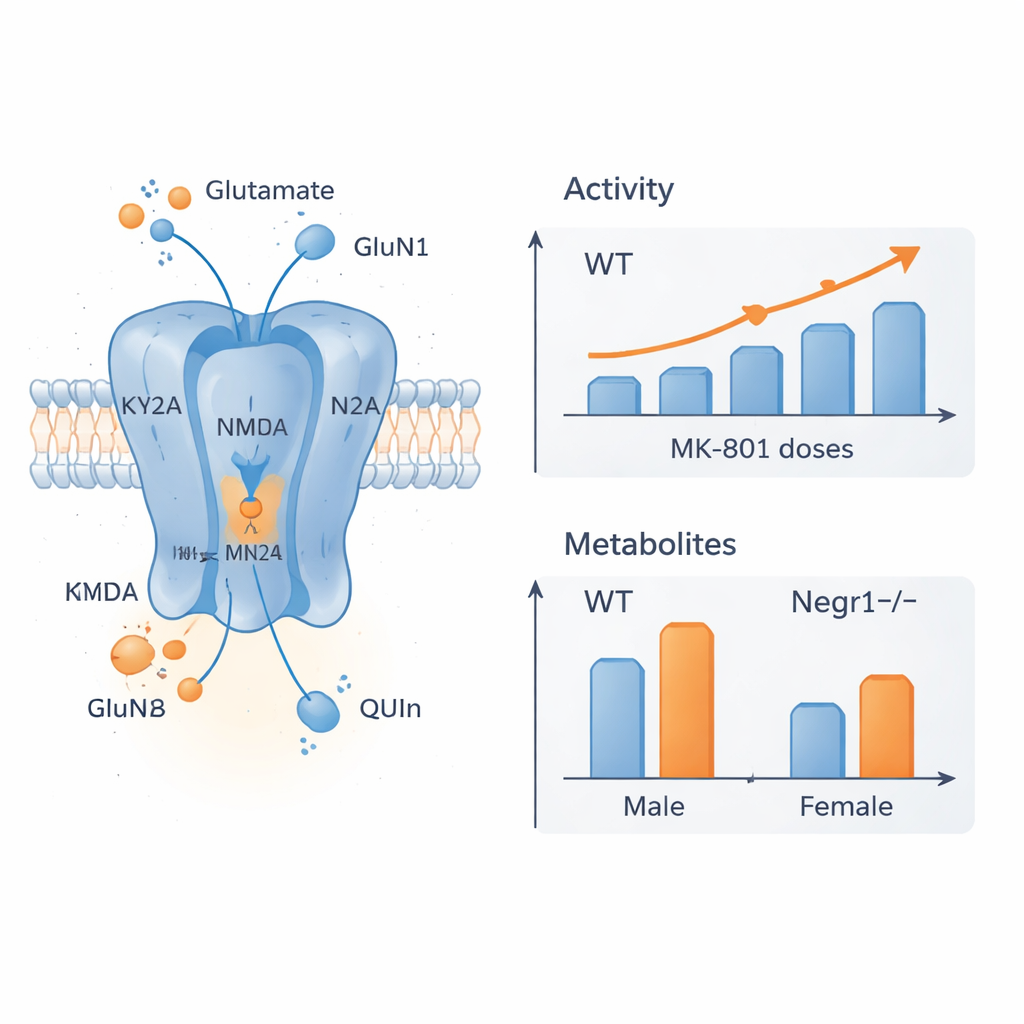
Mudanças em receptores e compostos cerebrais
Para descobrir o que estava por trás dessas diferenças comportamentais, a equipe mediu a atividade gênica de subunidades chave dos receptores NMDA e de uma enzima que produz D‑serina, um co-sinal para esses receptores. Eles se concentraram em regiões cerebrais cruciais para humor e cognição: córtex frontal e hipocampo. No córtex frontal, fêmeas deficientes em Negr1 tratadas com MK-801 mostraram redução na expressão de subunidades principais do receptor, sugerindo que seus cérebros ajustam a composição dos receptores em resposta tanto à mutação quanto ao fármaco. No hipocampo de machos, camundongos deficientes em Negr1 apresentaram expressão basal mais alta de certas subunidades do NMDA, em linha com evidências anteriores de mais receptores disponíveis; o tratamento com MK-801 então puxou esses níveis de volta em direção ao normal. Paralelamente, análises químicas detalhadas no sangue e em múltiplas regiões cerebrais revelaram que vários metabólitos da via da quinurenina e o próprio glutamato foram alterados de forma específica por sexo e região, com o córtex frontal sendo o mais afetado e algumas mudanças se tornando mais marcantes com a idade.
O que isso significa para entender doenças mentais
Em conjunto, esses achados apresentam o NEGR1 como um organizador molecular que ajuda a manter o equilíbrio entre sinais excitatórios e inibitórios no cérebro, em parte moldando a função dos receptores NMDA e o metabolismo do triptofano. Quando Negr1 está ausente, os camundongos respondem de maneira diferente ao bloqueio dos receptores NMDA, mostram mudanças químicas dependentes do sexo e desenvolvem tolerância gradual de maneiras incomuns. Para o leitor leigo, a mensagem-chave é que um único gene de risco não age isoladamente: seus efeitos dependem do sexo, da região cerebral e do estado metabólico. Este trabalho reforça a ideia de que direcionar vias ligadas ao NEGR1 — em vez de apenas receptores isolados — pode, em última instância, ajudar a personalizar tratamentos para doenças mentais marcadas por desequilíbrios do glutamato.
Citação: Kuuskmäe, C., Mikheim, K., Mohammadrahimi, N. et al. Negr1 deficiency alters glutamate signalling and kynurenine pathway in a mouse model of psychiatric disorders. Sci Rep 16, 5317 (2026). https://doi.org/10.1038/s41598-026-35968-7
Palavras-chave: gene NEGR1, receptor NMDA, sinalização do glutamato, via da quinurenina, transtornos psiquiátricos