Clear Sky Science · pt
APOBEC3B melhora a eficácia dos inibidores de PARP na eliminação de células-tronco do câncer de ovário
Por que esta pesquisa importa para pacientes com câncer de ovário
Muitas mulheres com câncer de ovário avançado respondem bem inicialmente a medicamentos modernos chamados inibidores de PARP, que exploram vulnerabilidades no sistema de reparo de DNA do tumor. No entanto, com o tempo a doença frequentemente retorna, à medida que as células tumorais aprendem a sobreviver a esses tratamentos. Este estudo investiga um aliado inesperado dentro das próprias células cancerosas — uma enzima que altera o DNA chamada APOBEC3B — e mostra que, sob condições adequadas, ela pode tornar as células-tronco do câncer de ovário mais fáceis de eliminar com inibidores de PARP.
Um câncer letal que volta com frequência
O carcinoma seroso de alto grau é a forma mais comum e mais letal de câncer de ovário. Geralmente é diagnosticado tardiamente, quando a doença já se espalhou pelo abdome, e mais de 80% das pacientes com doença avançada têm recidiva dentro de cinco anos. Um suspeito chave nessas recidivas é uma pequena população de “células-tronco cancerígenas”. Essas células podem se autorrenovar, sobreviver à quimioterapia e reconstruir tumores após o tratamento. Entender o que torna essas células com características de tronco resistentes — e como atacá-las — é essencial para melhorar a sobrevida a longo prazo.
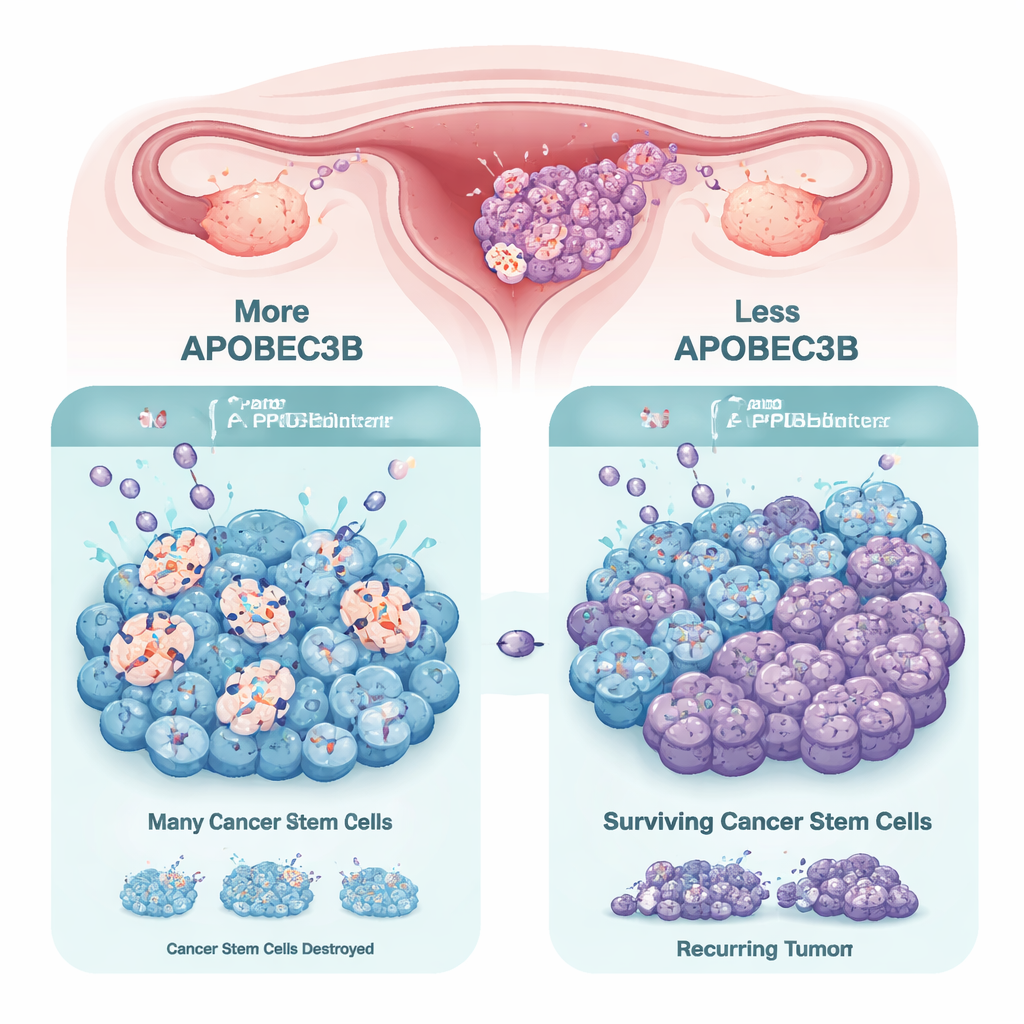
Uma enzima mutante com dupla vida
A família de enzimas APOBEC3 normalmente ajuda a proteger nossas células contra vírus ao alterar letras específicas do DNA, o que pode introduzir mutações. Em muitos cânceres, um membro dessa família, o APOBEC3B, está hiperativo e contribui para danos ao DNA e caos genético, impulsionando a evolução tumoral e a resistência a terapias. Em tumores ovarianos e modelos derivados de pacientes, os pesquisadores confirmaram que o APOBEC3B costuma ser a enzima APOBEC3 mais abundante. Contudo, ao comparar células tumorais comuns com “tumorspheres” — modelos 3D enriquecidos em células com aparência de tronco — eles descobriram que as células semelhantes a tronco reduzem consistentemente a expressão de APOBEC3B. Isso sugere que as células-tronco cancerígenas podem diminuir sua carga de mutações para preservar sua sobrevivência e capacidade de autorrenovação.
Reduzir APOBEC3B torna as células-tronco mais resistentes
Para testar se o APOBEC3B realmente influencia a característica de tronco, a equipe usou ferramentas genéticas para reduzir sua expressão em modelos de câncer de ovário derivados de pacientes e em linhagens celulares estabelecidas. Quando os níveis de APOBEC3B foram reduzidos, as células cancerosas formaram tumorspheres com mais eficiência e exibiram níveis mais altos de marcadores clássicos de pluripotência como SOX2, OCT4 e NANOG. A fração de células com propriedades semelhantes às de células-tronco aumentou, indicando que a perda de APOBEC3B ajuda as células cancerosas a migrar para um estado mais resiliente e parecido com tronco. Em camundongos, tumores sem APOBEC3B não cresceram mais rapidamente por si só, mas se comportaram de forma diferente quando tratados com inibidores de PARP.
Mais APOBEC3B, mais dano — e melhor resposta ao medicamento
Os pesquisadores então investigaram como o APOBEC3B afeta o desempenho dos inibidores de PARP, como o Olaparibe, que atuam bloqueando o reparo do DNA e empurrando as células cancerosas para um dano letal no genoma. Em várias linhagens de câncer de ovário, reduzir o APOBEC3B tornou as células mais resistentes aos inibidores de PARP, especialmente em tumorspheres 3D enriquecidos em células com características de tronco. Por outro lado, aumentar o APOBEC3B sensibilizou certas células aos inibidores de PARP, reduzindo muito sua sobrevivência. Em experimentos com camundongos, tumores com níveis normais de APOBEC3B encolheram ou tiveram crescimento dramaticamente reduzido com Olaparibe, enquanto tumores deficientes em APOBEC3B continuaram a crescer apesar do tratamento. Análises moleculares explicaram por quê: altos níveis de APOBEC3B aumentaram o estresse de replicação do DNA e quebras de fita dupla, ativando vias de sinalização de dano ao DNA. Quando o APOBEC3B foi silenciado, o dano ao DNA induzido por inibidores de PARP, a ativação de checkpoints e o estresse de replicação diminuíram, e as células tinham mais probabilidade de interromper o ciclo celular de forma segura em vez de morrer.
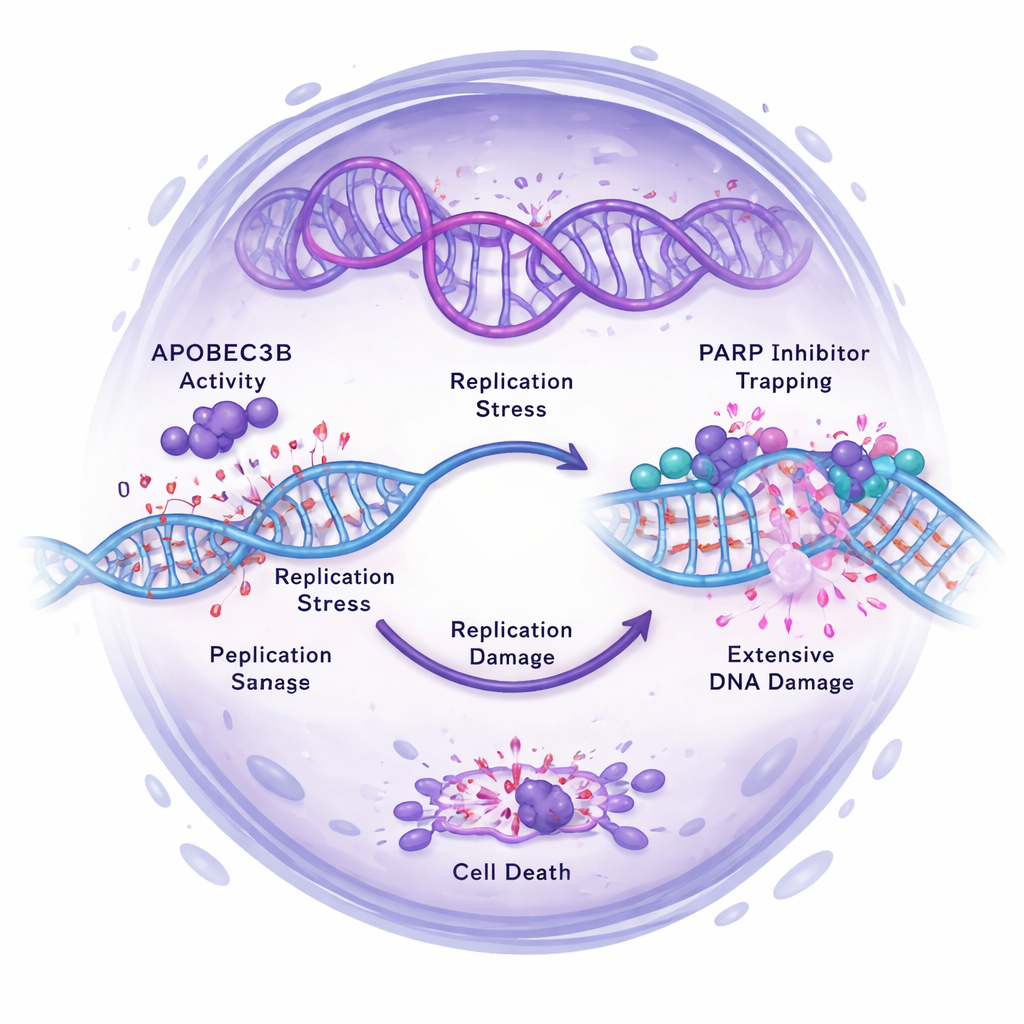
Uma nova forma de pensar sobre resistência e desenho de tratamentos
Aprofundando-se com sequenciamento de RNA, a equipe descobriu que a combinação da perda de APOBEC3B e da inibição de PARP reprogramou muitos genes envolvidos na replicação e reparo do DNA, reforçando a ideia de que o APOBEC3B amplifica os efeitos nocivos dos inibidores de PARP sobre o genoma das células cancerosas. Eles também testaram se outra enzima de reparo, UNG, era necessária para esse efeito e descobriram que a sensibilidade aos inibidores de PARP em células com alto APOBEC3B foi em grande parte independente da UNG. No conjunto, os dados apontam para o estresse de replicação induzido por APOBEC3B — e não apenas sua atividade mutagênica — como o principal fator que ajuda os inibidores de PARP a matar células-tronco do câncer de ovário.
O que isso significa para pacientes e futuras terapias
Para um público leigo, a mensagem é que nem todo caos genético dentro de um tumor é uma má notícia. Neste estudo, níveis mais altos da enzima mutadora APOBEC3B tornaram, na verdade, as células-tronco do câncer de ovário mais vulneráveis aos inibidores de PARP ao sobrecarregar sua capacidade de reparo do DNA. Quando o APOBEC3B foi reduzido, as células-tronco cancerígenas tornaram-se mais parecidas com células-tronco e mais capazes de resistir ao tratamento. Esses achados sugerem que medir os níveis de APOBEC3B poderia ajudar a prever quais pacientes se beneficiarão mais dos inibidores de PARP, e que o momento ou a combinação de futuros medicamentos direcionados ao APOBEC3B com inibidores de PARP precisa ser planejada com cuidado. Aproveitar o efeito de “auto-sabotagem” do APOBEC3B nas células cancerosas pode abrir novas estratégias para prevenir recidivas e eliminar mais efetivamente as raízes dos tumores ovarianos.
Citação: Rivera, M., Liu, L., Enlund, S. et al. APOBEC3B enhances the efficacy of PARP inhibitors in elimination of ovarian cancer stem cell. Sci Rep 16, 5194 (2026). https://doi.org/10.1038/s41598-026-35939-y
Palavras-chave: câncer de ovário, inibidores de PARP, células-tronco cancerígenas, APOBEC3B, resistência a medicamentos