Clear Sky Science · pt
KIN17 facilita o início e a progressão de tumores renais pela via PI3K‑AKT‑mTOR
Por que este estudo sobre câncer de rim importa
O câncer de rim vem sendo detectado com mais frequência, mas para muitos pacientes a doença continua difícil de controlar quando se espalha. Este estudo investiga em escala microscópica — até o nível de moléculas individuais dentro das células tumorais — para entender o que impulsiona o crescimento e a invasão dos tumores renais e se um fármaco experimental pode frear esse processo. Os resultados apontam para uma proteína pouco conhecida, KIN17, como um novo agente nocivo no câncer renal e sugerem uma maneira de atacá‑la indiretamente com um tratamento oral.
Um motor oculto dentro dos tumores renais
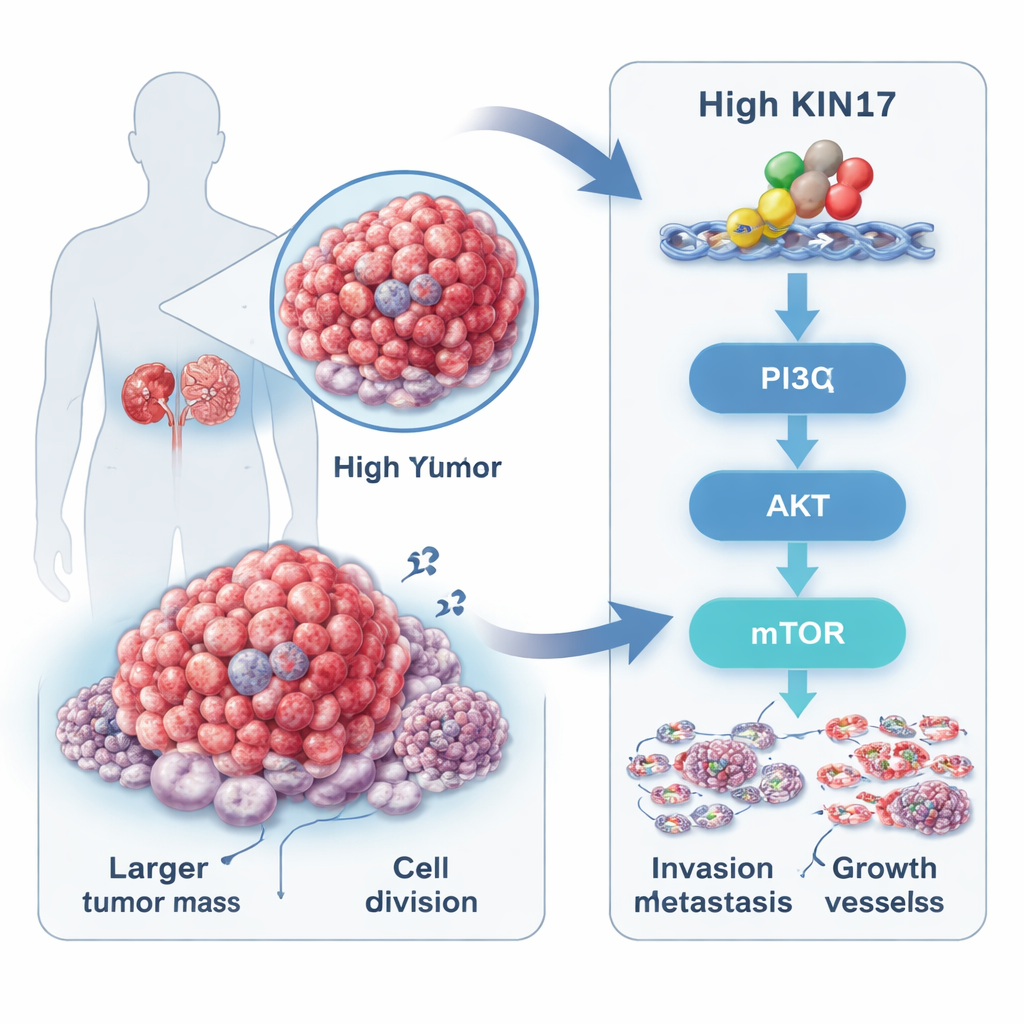
O carcinoma de células renais, a forma mais comum de câncer de rim, frequentemente começa sem sintomas e é descoberto tardiamente. Os pesquisadores focalizaram em uma proteína chamada KIN17, conhecida há muito por seu papel na proteção e replicação do DNA, mas só recentemente associada a vários outros cânceres. Ao analisar bases de dados públicas e amostras tumorais de 88 pacientes, eles descobriram que os níveis de KIN17 eram muito mais altos nos tumores renais do que no tecido não canceroso adjacente. Pacientes cujos tumores apresentavam mais KIN17 tendiam a ter cânceres maiores, doença de grau mais alto, estádio mais avançado e maior disseminação à distância, e viveram menos que aqueles com baixos níveis de KIN17. Esse padrão sugere que KIN17 não é apenas um espectador, mas está intimamente ligado à agressividade do tumor.
Testando KIN17 em células cancerosas
Para descobrir o que KIN17 faz dentro das células do câncer renal, a equipe modificou linhagens celulares de laboratório para reduzir ou aumentar a expressão de KIN17. Quando diminuíram KIN17, as células cresceram mais lentamente, formaram menos colônias e tiveram menor capacidade de migrar e invadir membranas artificiais. Mais dessas células ficaram presas na fase de repouso do ciclo celular e sofreram morte celular, com níveis mais altos de apoptose. O oposto ocorreu quando KIN17 foi superexpresso: as células multiplicaram‑se mais rápido, replicaram o DNA com mais facilidade, fecharam lacunas em camadas celulares mais rapidamente e invadiram de forma mais agressiva. Esses experimentos mostraram que KIN17 funciona como um pedal do acelerador para o crescimento e a disseminação das células do câncer renal.
Uma via de crescimento flagrante em ação
Os pesquisadores então perguntaram como KIN17 exerce esse efeito. As varreduras de atividade gênica e os testes proteicos apontaram para uma conhecida rede de crescimento e sobrevivência dentro das células chamada via PI3K–AKT–mTOR. Essa via é frequentemente comparada a um centro de controle que diz às células quando crescer, dividir‑se e evitar a morte. Células do câncer renal com altos níveis de KIN17 apresentaram sinais de ativação maiores — marcas químicas chamadas fosfatos — em componentes-chave dessa via, mesmo que a quantidade total dessas proteínas não tenha mudado. Quando KIN17 foi reduzido, essas marcas de ativação caíram, e moléculas associadas à movimentação e invasão celular também se alteraram. Em experimentos com camundongos, tumores formados por células ricas em KIN17 cresceram maiores e mais rápido, e colorações teciduais mostraram que a mesma via de crescimento estava fortemente ativada nesses tumores.
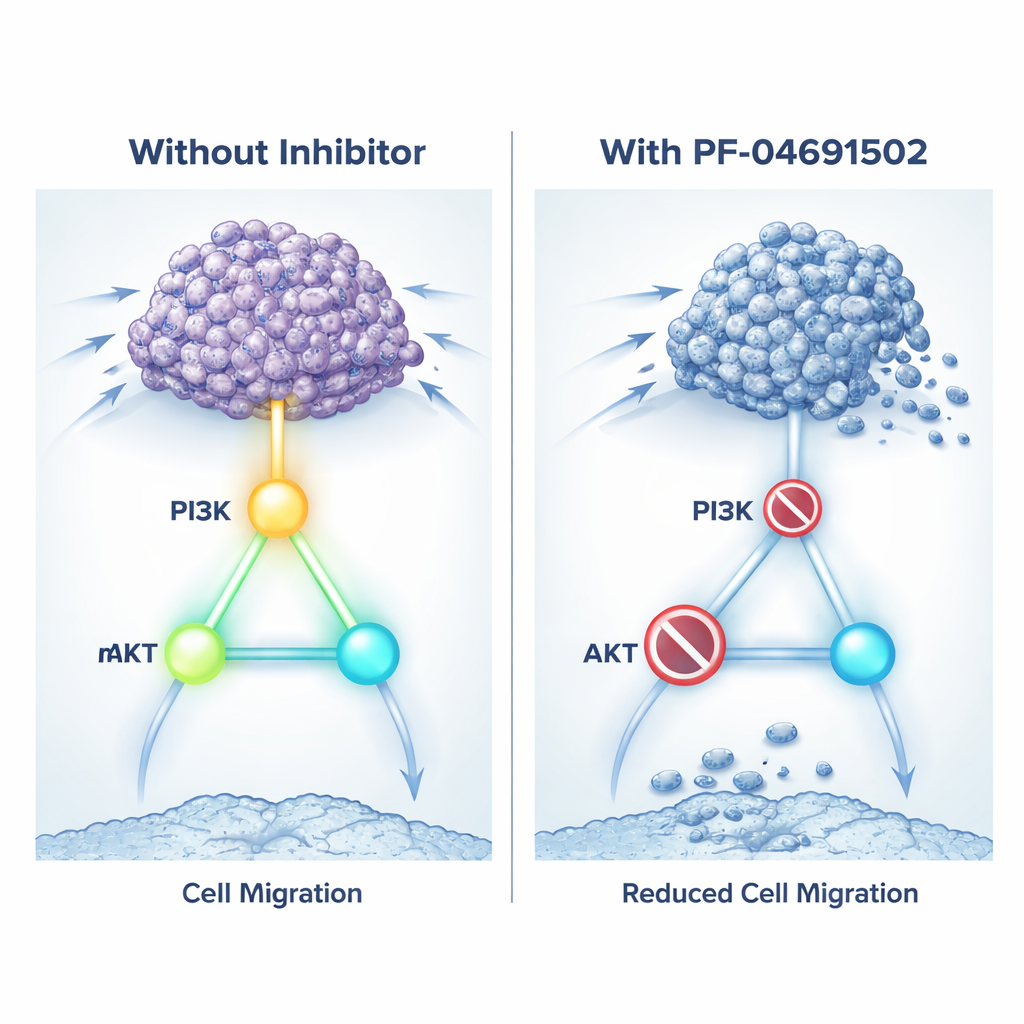
Abaixando o sinal com um fármaco de dupla ação
Como bloquear KIN17 diretamente ainda não é possível com medicamentos disponíveis, a equipe testou uma tática diferente: desligar a via de crescimento que ela parece controlar. Usaram PF‑04691502, um fármaco experimental que inibe tanto a PI3K quanto a mTOR, dois interruptores-chave da via. Em cultura, tratar células de câncer renal com altos níveis de KIN17 com esse inibidor retardou seu crescimento, reduziu a capacidade de migração e formação de colônias e aumentou a morte celular. O fármaco também diminuiu as marcas de ativação na PI3K, AKT e mTOR e reduziu os níveis de proteínas relacionadas à invasão. Em camundongos com tumores renais, doses diárias de PF‑04691502 encolheram tumores que superproduziam KIN17 e reduziram marcadores de divisão celular ao mesmo tempo em que aumentaram sinais de morte celular. Em essência, o fármaco foi capaz de atenuar os efeitos nocivos de KIN17 silenciando sua via de crescimento preferida.
O que isso pode significar para pacientes
Para pessoas com câncer de rim, esses achados sugerem duas ideias promissoras. Primeiro, medir KIN17 em amostras tumorais pode ajudar os médicos a avaliar quão agressivo é um tumor e sua probabilidade de se disseminar. Segundo, tumores que dependem fortemente de KIN17 podem ser especialmente vulneráveis a fármacos que atingem a via PI3K–AKT–mTOR, como PF‑04691502 ou inibidores de dupla ação similares já em testes clínicos para outros cânceres. Embora ainda seja necessário muito trabalho antes que qualquer novo tratamento chegue à clínica, este estudo mapeia uma cadeia clara de eventos — de KIN17, por meio de uma via de crescimento-chave, até a expansão tumoral descontrolada — e mostra que romper essa cadeia pode retardar o câncer de rim em laboratório e em animais.
Citação: Wen, Y., Lyu, L., Zhang, H. et al. KIN17 facilitates the initiation and progression of renal tumor progression through the PI3K-AKT-mTOR pathway. Sci Rep 16, 5721 (2026). https://doi.org/10.1038/s41598-026-35851-5
Palavras-chave: carcinoma de células renais, KIN17, PI3K AKT mTOR, terapia alvo, PF-04691502