Clear Sky Science · pt
Similaridades em alterações de expressão gênica e metilação entre dois modelos de rato de epilepsia adquirida
Por que mudanças nos genes importam para as convulsões
A epilepsia afeta milhões de pessoas e, para cerca de um em cada três, os remédios atuais não conseguem controlar totalmente as convulsões. A maioria dos fármacos apenas atenua as tempestades elétricas no cérebro, mas não impede que a epilepsia se desenvolva. Este estudo investiga se marcas químicas duradouras no DNA e a forma como genes são ligados ou desligados podem explicar como um cérebro saudável se torna epiléptico — e se essas alterações são compartilhadas entre diferentes formas da doença.
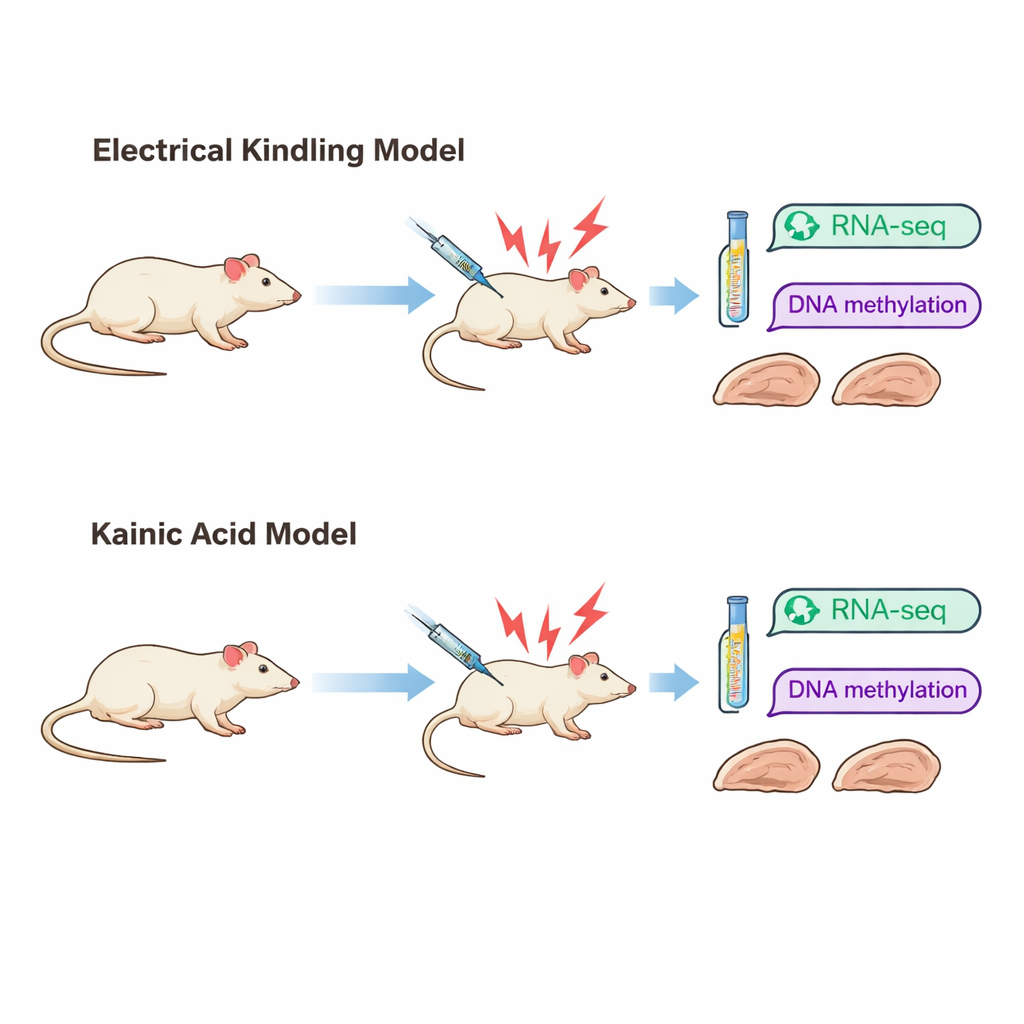
Dois caminhos diferentes para a mesma doença
Os pesquisadores concentraram-se na epilepsia do lobo temporal, uma forma comum da condição que frequentemente resiste ao tratamento. Eles usaram dois modelos bem estabelecidos em ratos que imitam maneiras diferentes pelas quais a epilepsia pode surgir. No modelo de “kindling” (sensibilização), pulsos elétricos breves são aplicados a uma parte do hipocampo ao longo do tempo até que as convulsões se tornem fáceis de desencadear. No modelo de “ácido cainico”, um composto químico provoca um surto intenso de convulsões, após o qual convulsões espontâneas aparecem mais tarde. Embora ambos os modelos produzam, em última instância, comportamento externo semelhante — convulsões convulsivas severas —, o dano cerebral observado é muito diferente. Ratos submetidos ao kindling apresentam preservação significativa da estrutura tecidual, enquanto ratos tratados com ácido cainico mostram perda celular pronunciada e cicatrização em regiões-chave do hipocampo.
Lendo a atividade genética do cérebro
Para ver como esses caminhos diferentes para a epilepsia alteram o cérebro em nível molecular, a equipe examinou o hipocampo depois que ratos de cada modelo haviam experimentado três convulsões severas. Mediram quais genes estavam mais ou menos ativos usando sequenciamento de RNA, e mapearam marcas químicas chamadas grupos metila no DNA usando um método conhecido como sequenciamento bisulfito de representação reduzida. Mudanças na atividade gênica refletem como as células estão respondendo e se adaptando, enquanto as marcas de metilação são frequentemente consideradas uma “memória” de longo prazo que pode influenciar se genes são ligados ou desligados.
Alterações na atividade gênica superam marcas no DNA
Os dois modelos produziram padrões de atividade gênica marcadamente diferentes. O modelo de kindling mostrou alterações em mais de dez vezes o número de genes em comparação com o modelo de ácido cainico. Ainda assim, quando os pesquisadores sobrepuseram as duas listas, encontraram mais de cem genes que mudaram em ambos os modelos, e a maioria desses mudou na mesma direção. Um exemplo é Mmp9, um gene associado a como as células cerebrais remodelam suas conexões e ao dano relacionado a convulsões; ele foi fortemente aumentado em ambos os modelos. Essas mudanças compartilhadas sugerem que existem respostas genéticas centrais à epileptogênese, mesmo quando o gatilho inicial e a lesão cerebral visível diferem.
As marcas no DNA contam uma história diferente
Quando a equipe examinou a metilação do DNA, o quadro mudou. Ambos os modelos mostraram muitos genes com metilação alterada, e houve uma sobreposição considerável entre eles. Entretanto, apenas um subconjunto modesto de genes apresentou tanto metilação alterada quanto atividade alterada dentro do mesmo modelo, e ainda menos se comportaram dessa maneira em ambos os modelos. Em alguns desses genes compartilhados, como Nedd9 e Ptpre, a expressão aumentou em ambos os modelos, mas a direção da mudança de metilação do DNA em sítios individuais podia ser oposta entre os modelos. No geral, não houve uma regra simples de que “mais metilação significa menos atividade gênica” ou o contrário. Isso sugere que, nesses modelos de epilepsia, a maioria das mudanças na atividade gênica não é diretamente conduzida por alterações amplas na metilação do DNA.
O que isso significa para tratamentos futuros
Para quem espera terapias melhores para a epilepsia, esses achados trazem tanto cautela quanto orientação. O trabalho mostra que os programas genéticos ativados durante o desenvolvimento da epilepsia podem ser bastante específicos ao modelo, e que a metilação do DNA é apenas uma parte de um quadro regulatório maior e mais complexo. Alvos gênicos promissores identificados em um único modelo animal podem não se generalizar, por isso devem ser testados em múltiplos modelos antes de avançar rumo a tratamentos humanos. Ao mesmo tempo, o pequeno conjunto de genes que mudam tanto na expressão quanto na metilação entre os modelos pode representar pontos de partida especialmente robustos para desenvolver terapias modificadoras da doença que visem não apenas a atenuação das convulsões, mas a prevenção do estabelecimento da epilepsia.
Citação: Purnell, B.S., Hur, J., Ruskin, D. et al. Commonalities in gene expression and methylation changes across two rat models of acquired epilepsy. Sci Rep 16, 5095 (2026). https://doi.org/10.1038/s41598-026-35826-6
Palavras-chave: epileptogênese, metilação do DNA, expressão gênica, epilepsia do lobo temporal, modelos em rato