Clear Sky Science · pt
Estresse mecânico favorecendo a migração heterogênea de células de câncer de pulmão em canais confinados e investigando o crescimento de esferoides tumorais de células migrantes em espaço confinado
Por que apertar células cancerígenas importa
O câncer não se espalha em espaço aberto. À medida que células tumorais deixam seu sítio original, elas precisam se espremer por pequenas fendas em tecidos, paredes de vasos sanguíneos e outras estruturas congestionadas. Este estudo faz uma pergunta simples, porém poderosa: dentro de uma população mista de células de câncer de pulmão, quais realmente conseguem passar por esses pontos estreitos e que tipo de tumor elas formam depois? As respostas podem ajudar a explicar por que algumas células cancerígenas são mais perigosas que outras e podem orientar novas maneiras de prever ou retardar a metástase.
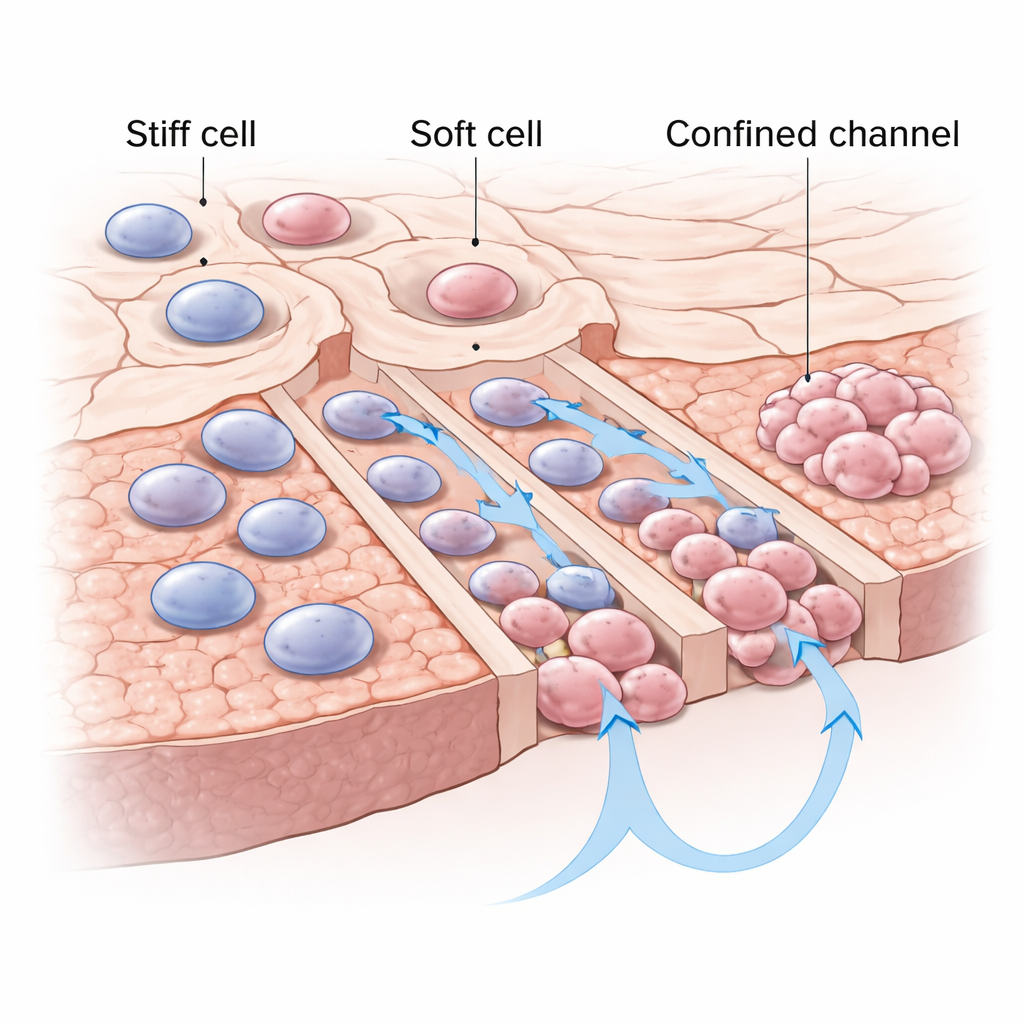
Células mais macias se dão melhor em espaços apertados
Os autores focaram em uma característica física das células que a maioria das pessoas nunca ouve falar: a rigidez. Algumas células cancerígenas são relativamente rígidas, enquanto outras são macias e facilmente deformáveis. Usando chips microfluídicos especialmente projetados — pequenos dispositivos plásticos gravados com canais mais estreitos que uma célula típica — eles aprisionaram células individuais de câncer de pulmão nas entradas de canais estreitos (confinados) e altos (não confinados). Após 24 horas, mais células únicas escolheram e atravessaram com sucesso os canais estreitos e confinados do que os mais abertos, e elas se moveram mais rápido dentro dessas passagens apertadas. Quando os pesquisadores depois sondaram a mecânica das células com um microscópio de força atômica (uma espécie de “dedo” em escala nanométrica), descobriram que os viajantes nos canais confinados eram consistentemente mais macios do que seus homólogos que ficaram para trás ou se moveram em canais não confinados.
Uma assinatura molecular da suavidade
Para entender o que tornava algumas células mais macias, a equipe examinou uma proteína estrutural chamada vimentina e uma proteína de suporte nuclear codificada pelo gene LMNA. A vimentina faz parte do arcabouço interno que ajuda a célula a resistir à deformação. Células que haviam se espremido por canais confinados mostraram níveis menores de vimentina em comparação com células em canais espaçosos ou em placas de cultura padrão. Imagens de alta resolução revelaram que, nas migrantes confinadas, a rede de vimentina estava mais frouxamente organizada tanto ao redor do corpo celular quanto próxima ao núcleo, em vez de densamente agrupada. Testes de expressão gênica em nível de célula única confirmaram que tanto o gene da vimentina (VIM) quanto o LMNA, que ajuda a manter o núcleo mecanicamente robusto, estavam diminuídos nas células que preferiram rotas confinadas.
Tornar células mais macias aumenta a migração confinada
Os pesquisadores então perguntaram se poderiam intencionalmente amaciar as células e ver se isso alteraria seu comportamento. Eles usaram duas abordagens: um tratamento bioquímico (TGF-β1) conhecido por remodelar o citoesqueleto, e compressão mecânica suave usando lâminas de silicone macio pressionando as células. Ambos os métodos reduziram a rigidez e diminuíram os níveis de vimentina sem matar as células. Quando essas células pré-amelhoradas foram introduzidas no dispositivo microfluídico, uma fração ainda maior migrou para os canais estreitos em comparação com células não tratadas. Isso sugere que a suavidade não é apenas um efeito colateral do confinamento; é uma propriedade que pode ser ajustada e que influencia fortemente se uma célula pode entrar e atravessar pequenas aberturas.
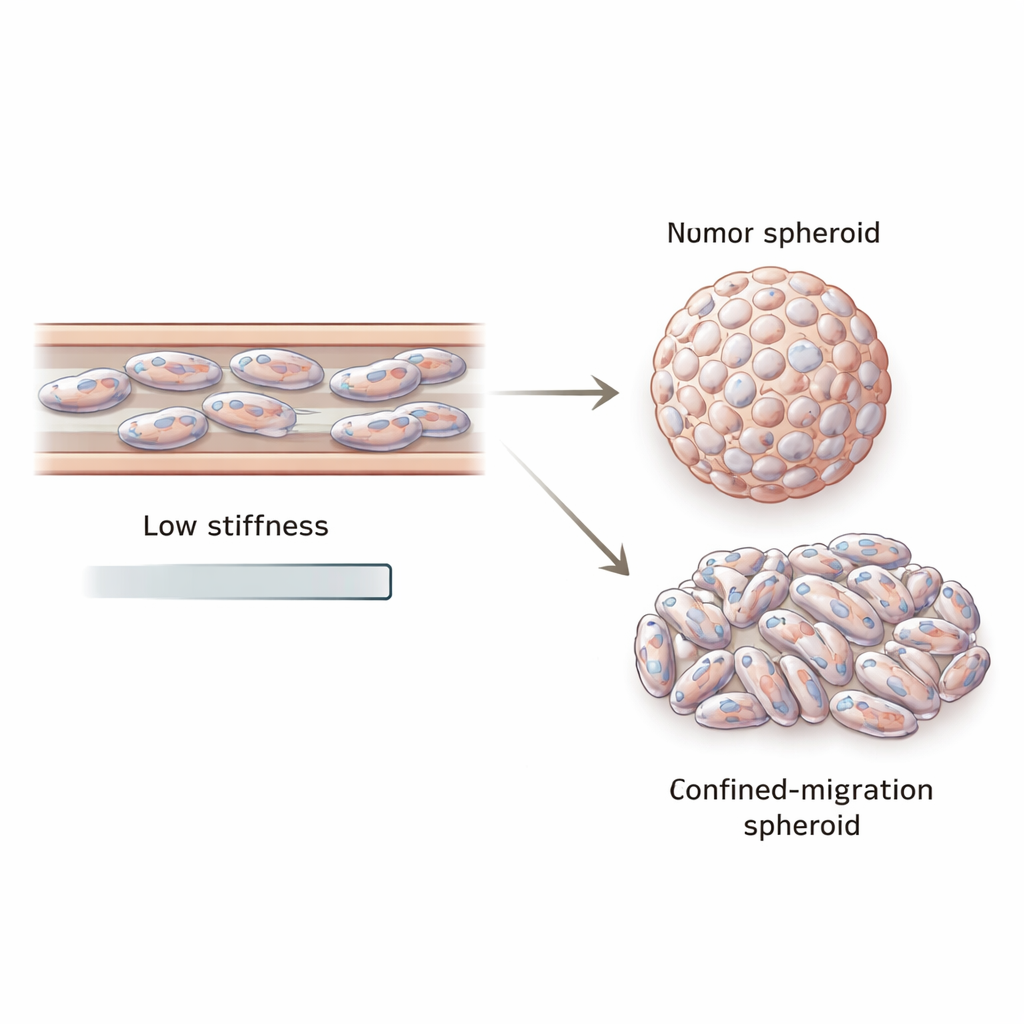
De células espremidas a bolas tumorais deformadas
A metástase, porém, não é apenas sobre movimento. Células que escapam também devem regredir e formar novos tumores. Para mimetizar essa etapa, a equipe usou um segundo sistema de confinamento chamado trans-well, onde as células migram através de poros minúsculos antes de serem coletadas e cultivadas em poços antiaderentes para formar “esferoides” tumorais tridimensionais. Esferoides cultivados a partir de células que passaram por migração confinada foram menores e visivelmente menos arredondados do que esferoides cultivados a partir das mesmas linhagens celulares sem o aperto prévio. Seus núcleos celulares estavam mais alongados e deformados, e esses esferoides continuaram a mostrar expressão reduzida de VIM e LMNA. Mesmo dentro de esferoides individuais, os níveis de vimentina variaram do centro para a borda, sugerindo diversidade mecânica e genética no tumor resultante.
O que isso significa para entender a metástase
De forma direta, este estudo mostra que, entre muitas células de câncer de pulmão, as mais macias têm maior probabilidade de escapar por espaços apertados, sobreviver à jornada e depois formar aglomerados tumorais de forma estranha e mecanicamente frágeis com núcleos distorcidos. Essas células carregam e mantêm uma assinatura molecular distinta — baixos níveis de genes estruturais-chave — que liga como elas se movem a como crescem. Embora o trabalho tenha sido realizado em dispositivos de laboratório cuidadosamente controlados em vez de em pacientes, ele oferece um roteiro físico e genético de uma célula cancerígena “migrante confinada”. A longo prazo, medir ou direcionar a suavidade celular e seus marcadores moleculares pode tornar-se parte de estratégias para entender, rastrear ou, eventualmente, interromper as subpopulações celulares mais invasivas do câncer.
Citação: Alam, M.K., Ma, Y., Zhai, J. et al. Mechano-stress endorsing heterogeneous lung cancer cells migration into confined channels and investigating tumor spheroids growth of confined space migrating cells. Sci Rep 16, 6649 (2026). https://doi.org/10.1038/s41598-026-35818-6
Palavras-chave: rigidez de células cancerígenas, migração celular confinada, esferoides de câncer de pulmão, vimentina e LMNA, mecânica tumoral