Clear Sky Science · pt
SwiM-UNet leve com adaptador multidimensional para segmentação médica eficiente em dispositivos
Exames mais inteligentes à beira do leito
Exames cerebrais podem revelar tumores que ameaçam a vida, mas transformar imagens brutas em contornos claros que os médicos possam usar ainda é demorado e exige muito do computador. Este estudo apresenta o SwiM-UNet, um novo algoritmo capaz de segmentar tumores cerebrais a partir de exames de ressonância magnética 3D com precisão de ponta, ao mesmo tempo em que roda de forma eficiente em dispositivos locais, aproximando a análise precisa das imagens do leito do paciente ou mesmo de clínicas móveis. 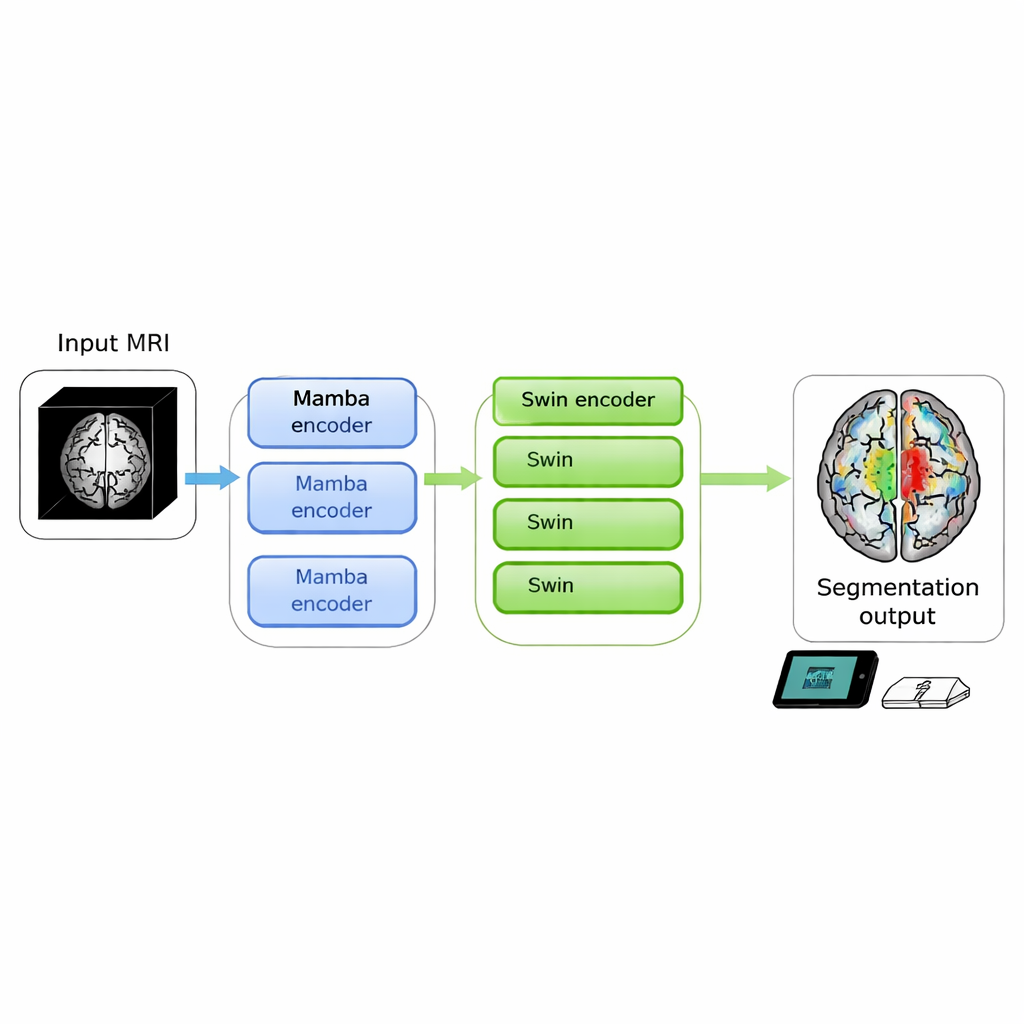
Por que contornos precisos dos tumores importam
A medicina moderna depende fortemente de imagens para planejar cirurgias, radioterapia e tratamentos medicamentosos. Para tumores cerebrais, os médicos precisam não só ver que há um tumor, mas saber exatamente onde começam e terminam suas partes distintas. Essa tarefa, chamada segmentação, costuma ser feita ou refinada por especialistas fatia a fatia — um processo que consome tempo, atrasa decisões e varia entre profissionais. Ferramentas automáticas de segmentação baseadas em deep learning melhoraram essa situação, mas as mais precisas frequentemente exigem grandes processadores gráficos, o que dificulta seu uso direto na clínica, especialmente em máquinas menores ou portáteis.
Duas ideias poderosas que não cabem facilmente em máquinas pequenas
Avanços recentes em visão computacional vêm principalmente de duas famílias de modelos. Sistemas baseados em transformers, como o Swin Transformer, são excelentes em captar padrões globais em um exame 3D inteiro e têm impulsionado segmentadores de tumor cerebral de alto desempenho. Contudo, sua operação central, chamada self-attention, torna-se extremamente custosa à medida que o tamanho da imagem cresce, limitando seu uso em tempo real ou em hardware compacto. Uma família mais nova, conhecida como Mamba e baseada em modelos de espaço de estados, oferece uma solução engenhosa: processa sequências em tempo praticamente linear, reduzindo o número de computações necessárias. Experimentos iniciais em imagens médicas mostraram que modelos ao estilo Mamba são rápidos e eficientes, mas geralmente ficam atrás dos transformers em qualidade de segmentação, especialmente para formas complexas de tumor.
Misturando velocidade e precisão em um único projeto
Os autores propuseram unir as forças de ambos os mundos em um modelo 3D único. O SwiM-UNet mantém a estrutura em U amplamente usada em imagem médica, com um codificador que comprime a informação e um decodificador que reconstrói segmentações detalhadas. Nas etapas iniciais, quando o exame ainda é grande e de alta resolução, eles usam blocos Mamba eficientes para manter as contas manejáveis. Mais profundo na rede, depois que os dados foram amostrados para baixo, eles mudam para blocos Swin Transformer enxutos que já podem modelar relações de longo alcance sem sobrecarregar o hardware. Uma ponte personalizada chamada MS-adapter conecta esses dois regimes. Ela observa as características ao longo da largura, altura e profundidade do volume separadamente, e também entre canais, e aprende, por meio de pequenas unidades de gating, quanto cada visão deve influenciar a representação final. 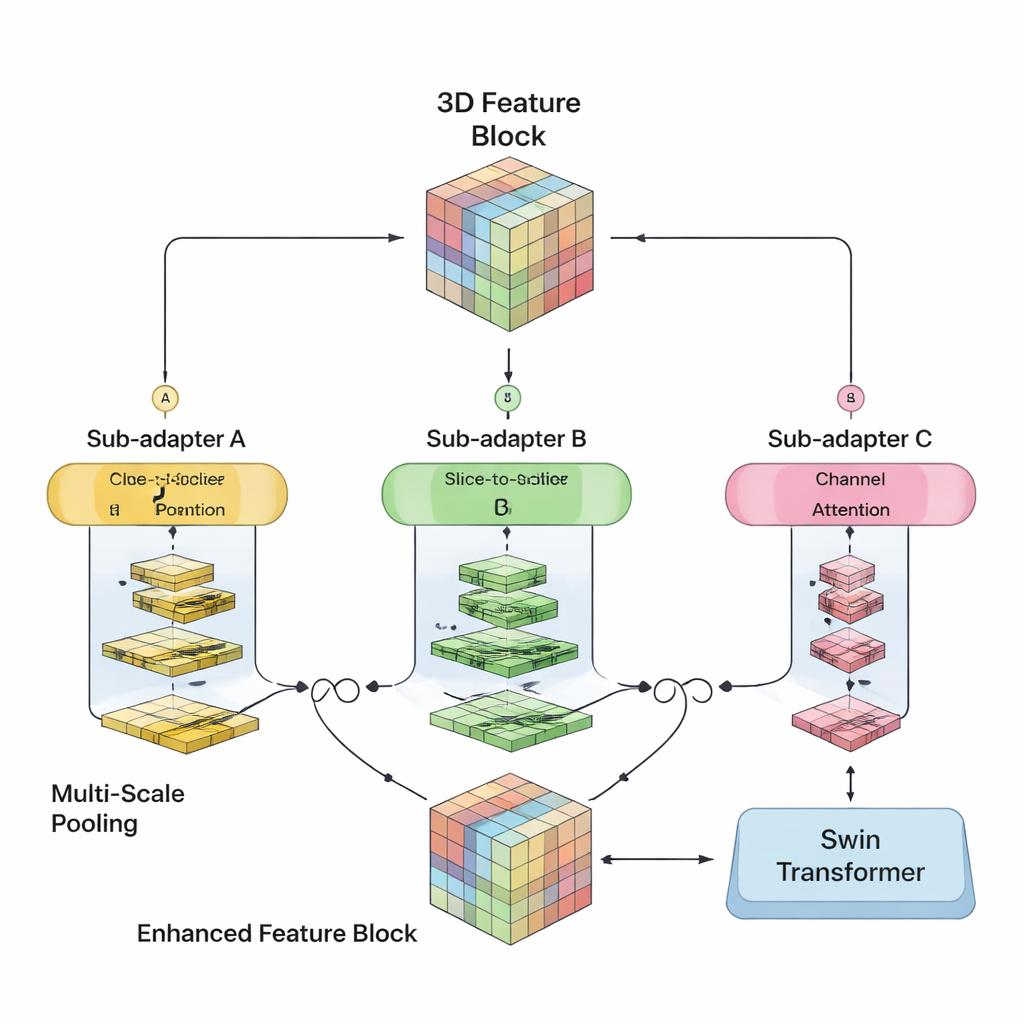
Fazendo mais com menos computação
Além desse arranjo híbrido, a equipe reduz a computação excessiva usando camadas totalmente conectadas de baixa ordem (low-rank) e um decodificador que deliberadamente diminui o número de canais que precisa processar. Testaram várias variantes com diferentes combinações de camadas Mamba e Swin e descobriram que usar Mamba nas três primeiras etapas do codificador e Swin apenas na etapa mais profunda ofereceu o melhor equilíbrio entre velocidade e precisão. Em dois grandes conjuntos públicos de tumores cerebrais dos desafios BraTS 2023 e 2024, o SwiM-UNet alcançou maior precisão e contornos mais precisos do que modelos apenas com transformers, apenas Mamba e anteriores híbridos, enquanto usava bem menos operações em ponto flutuante e reduzindo o tempo de inferência para cerca de 45 milissegundos por patch de exame em uma placa gráfica moderna.
Pronto para dispositivos do mundo real
Para verificar se esses ganhos importam fora do laboratório, os autores compararam as demandas computacionais do modelo com as capacidades de sistemas de borda clínicos típicos — consoles de MRI portáteis, computadores de ponto de atendimento e estações de trabalho de sala de cirurgia. A análise sugere que, ao contrário de modelos transformer mais pesados, o SwiM-UNet se encaixa confortavelmente nos limites de energia, memória e velocidade desses dispositivos, frequentemente atendendo aos requisitos em tempo real. Também teve bom desempenho em um conjunto separado de tomografia abdominal (CT), indicando que a abordagem pode se generalizar além de tumores cerebrais e mesmo além de MRI.
O que isso significa para pacientes e clínicos
Na prática, o SwiM-UNet demonstra que é possível aproximar-se da precisão dos modelos de segmentação mais sofisticados enquanto mantém a computação leve o suficiente para uso em dispositivo. Isso pode possibilitar contornos de tumor mais rápidos e consistentes em emergências, hospitais rurais ou unidades móveis de imagem sem enviar exames sensíveis para servidores distantes. Embora sejam necessários trabalhos adicionais para adaptar o método a diferentes aparelhos e condições, esse desenho híbrido aponta para um futuro em que análise de imagem de alta qualidade roda onde o paciente está, e não apenas em centros de dados.
Citação: Noh, Y., Lee, S., Jin, S. et al. Lightweight SwiM-UNet with multi-dimensional adaptor for efficient on-device medical image segmentation. Sci Rep 16, 5807 (2026). https://doi.org/10.1038/s41598-026-35771-4
Palavras-chave: segmentação de tumor cerebral, IA em imagens médicas, redes neurais híbridas, inferência em dispositivo, análise de MRI 3D