Clear Sky Science · pt
Variantes de splicing de KChIP1 modulam canais Kv4 promovendo características de inativação do tipo P/C
Como poros minúsculos moldam o ritmo elétrico do cérebro
Cada pensamento, memória e movimento no cérebro depende de sinais elétricos rápidos em neurônios. Esses sinais são ajustados com precisão por poros microscópicos — canais iônicos — que deixam partículas carregadas entrarem e saírem. Este artigo investiga como variações sutis de uma proteína acessória, KChIP1, podem alterar dramaticamente o comportamento de uma família de canais (Kv4), mudando a facilidade com que os neurônios disparam rajadas repetidas de atividade elétrica.
Canais de potássio como pedal de freio do cérebro
Os canais Kv4 conduzem uma chamada corrente de potássio do tipo A que liga e desliga rapidamente no corpo celular e nos ramos dos neurônios. Essa corrente ajuda a determinar quão facilmente um neurônio dispara e quão fielmente ele acompanha sinais de entrada, especialmente em taxas de disparo baixas. Os canais Kv4 não atuam sozinhos: eles se montam com proteínas auxiliares em um complexo de várias partes que inclui proteínas DPP e proteínas KChIP. Esses parceiros influenciam a rapidez com que os canais se desligam e com que voltam a ficar prontos para abrir novamente. Até agora, a maioria dos trabalhos sugeria que os KChIPs, de modo geral, aceleram a recuperação dos canais Kv4 após eles se desligarem, permitindo que os neurônios respondam rapidamente a entradas repetidas.
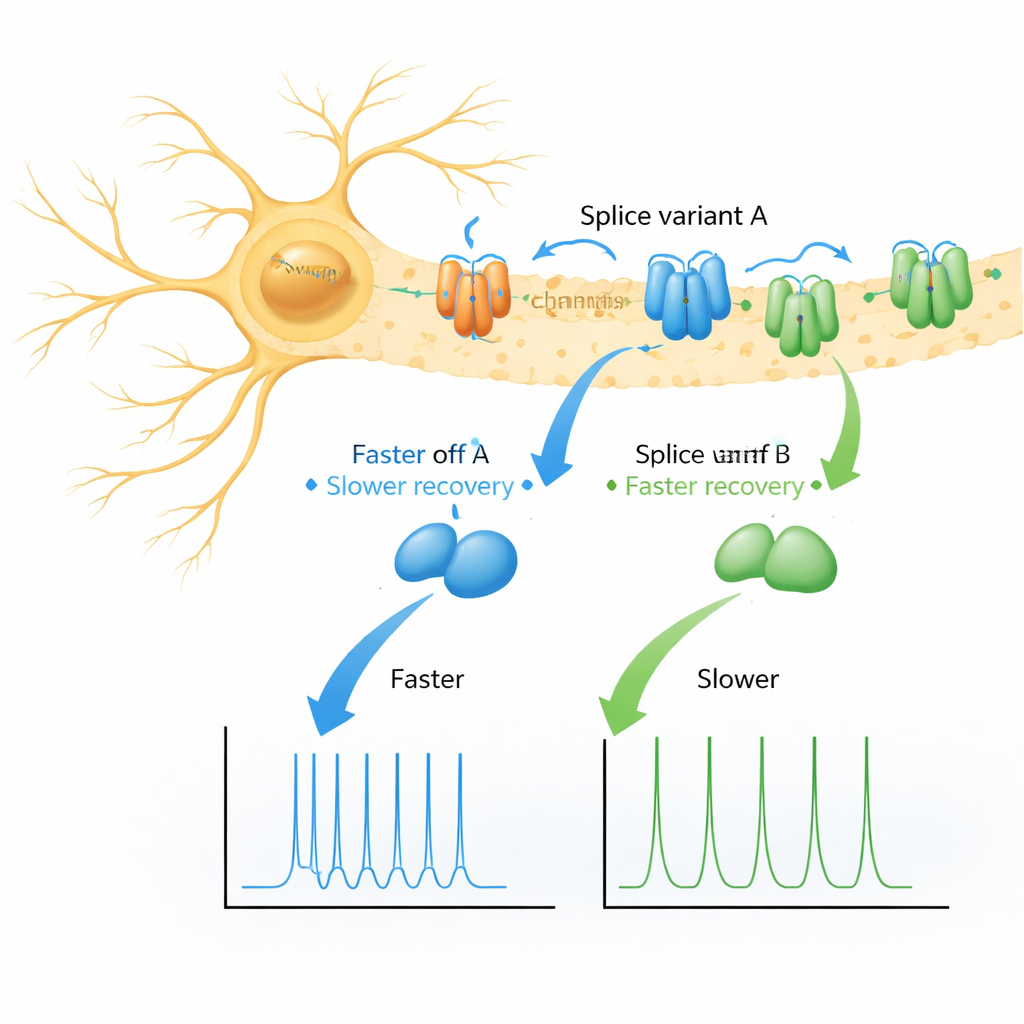
Duas variantes da proteína, dois sabores de recuperação
Os autores se concentraram em duas versões quase idênticas (variantes de splicing) de KChIP1, chamadas 1a e 1b, que diferem apenas por uma curta “cauda” aromática no início de 1b. Usando ovos de rã como um sistema de teste controlado, expressaram vários tipos de canais Kv4 isoladamente, com cada variante de KChIP1, com DPP ou com ambos os auxiliares juntos. Como esperado, tanto 1a quanto 1b remodelaram levemente o desligamento dos canais durante um passo de voltagem, sem causar mudanças dramáticas. A surpresa veio ao examinar como os canais se recuperavam após o desligamento: em vez de um retorno único e suave ao estado pronto, os canais emparelhados com 1a ou 1b mostraram duas fases distintas de recuperação — uma rápida e outra muito mais lenta — sendo a via lenta muito mais pronunciada para 1b.
Uma via lenta oculta revelada
Quando os canais Kv4 foram expressos sem KChIP1, eles se recuperaram por uma via simples e rápida, e a DPP acelerou isso ainda mais. A adição de KChIP1 alterou esse padrão. Com 1a, a maioria dos canais ainda se recuperou rapidamente, mas uma pequena fração fez um desvio lento de volta ao estado pronto. Com 1b, uma fração muito maior entrou nessa rota lenta, estendendo a recuperação para segundos. Esse efeito apareceu em todos os subtipos de Kv4 testados e persistiu mesmo na presença de DPP, indicando que a via lenta é uma característica intrínseca dos complexos que contêm KChIP1, e não um artefato de um canal ou configuração experimental particular. Os autores também encontraram que 1b deslocou a faixa de voltagem de "desligamento" dos canais para valores mais negativos, tendendo ainda mais a torná-los indisponíveis durante atividade contínua.
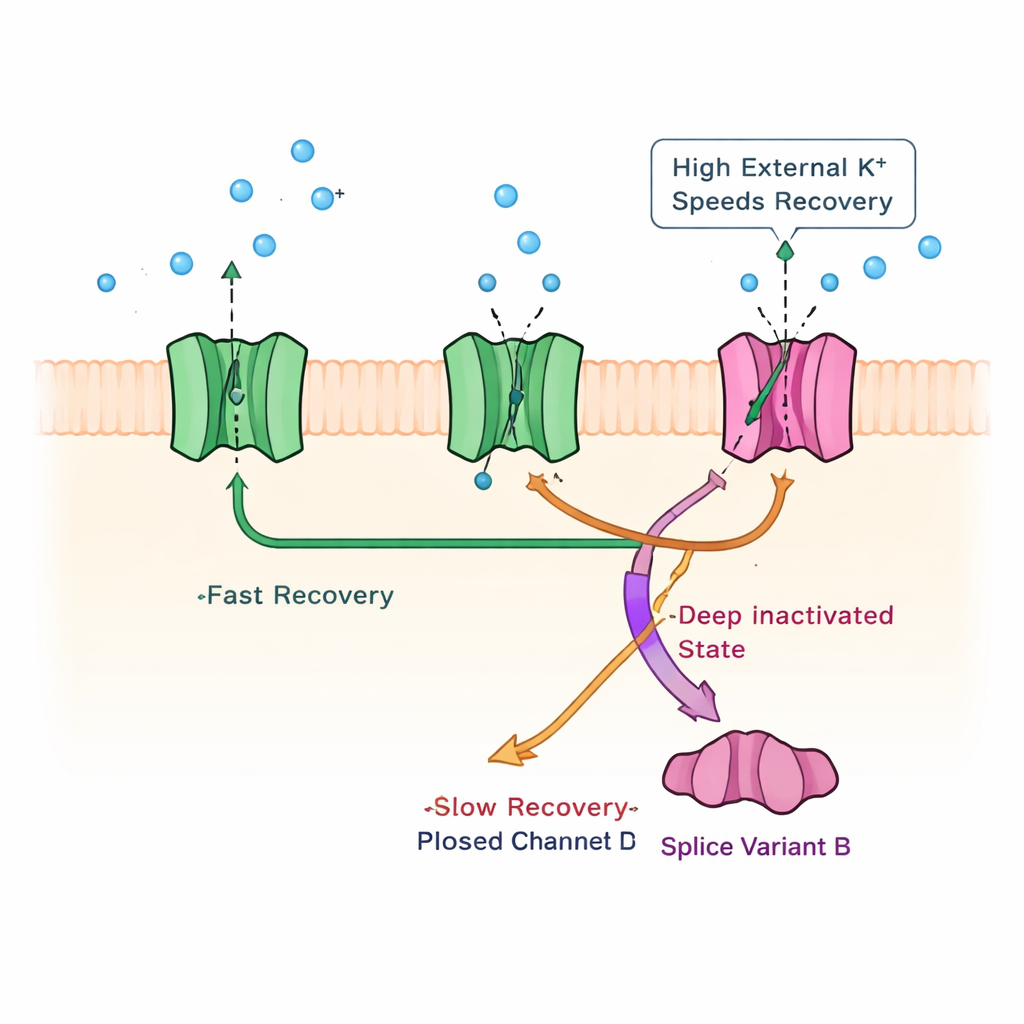
Descobrindo um mecanismo de inativação latente
Para entender que mudança física dentro do canal explica essa recuperação lenta, o grupo investigou mecanismos de inativação conhecidos de outros canais de potássio. Eles descartaram um bloqueio clássico do tipo "bola-e-corrente" na boca interna do canal ao cortar parte da cauda interna do canal; a fase lenta persistiu. Em seguida, usaram altos níveis de potássio externo, um artifício conhecido por alterar um processo de inativação centrado no poro em outros canais. Nessas condições, o desligamento da corrente ficou mais rápido, mas, crucialmente, a própria fase de recuperação lenta acelerou de forma específica, como se o alto potássio estivesse liberando os canais de um estado bloqueado profundo e duradouro. Mutações estratégicas em um segmento de gating do canal apoiaram ainda mais a ideia de que KChIP1b promove uma rota de inativação centrada no poro — normalmente fraca em canais Kv4 — que coexiste com a inativação de estado fechado usualmente mais rápida.
Por que isso importa para a atividade cerebral
As descobertas sugerem que, ao selecionar entre KChIP1a, KChIP1b ou misturas de ambos, os neurônios podem afinar com precisão quão rápido as correntes do tipo A se recuperam entre picos. Em células ricas em KChIP1b, uma fração significativa dos canais Kv4 fica "estacionada" em um estado inativado profundo e de reversão lenta, limitando sua disponibilidade durante disparos rápidos. Isso pode permitir que certos interneurônios — células que coordenam e restringem a atividade nos circuitos cerebrais — disparem em frequências mais altas ou com padrões de temporização distintos. Em essência, uma pequena diferença de splicing em uma proteína acessória desbloqueia um modo de freio oculto nos canais de potássio, adicionando uma nova camada de flexibilidade à forma como o cérebro controla seus próprios ritmos elétricos.
Citação: Cao, W., Tachtsidis, G. & Bähring, R. KChIP1 splice variants modulate Kv4 channels by promoting P/C-type inactivation features. Sci Rep 16, 2632 (2026). https://doi.org/10.1038/s41598-026-35770-5
Palavras-chave: Canais de potássio Kv4, Variantes de splicing de KChIP1, Corrente tipo A, Excitabilidade neuronal, Inativação de canais