Clear Sky Science · pt
O papel do receptor nicotínico de acetilcolina α7 na promoção da polarização de macrófagos M2 em sítios inflamatórios
Como os nervos ajudam a acalmar a inflamação descontrolada
Quando cortamos um dedo ou combatemos uma infecção, nossos corpos desencadeiam inflamação para nos proteger. Mas se essa reação persiste por muito tempo, pode danificar tecidos saudáveis e impulsionar doenças crônicas. Este estudo explora como um receptor “calmante” específico em células imunes, chamado receptor nicotínico de acetilcolina α7 (α7nAChR), ajuda a direcionar a inflamação para a cura em vez do dano, oferecendo pistas para novos tratamentos de condições como sepse, doença intestinal e artrite.
As duas faces das equipes de limpeza do sistema imune
Macrófagos são células imunes que funcionam como equipes de limpeza e reparo. Eles podem alternar entre dois modos principais. No modo “ataque”, frequentemente chamado M1, liberam substâncias agressivas para matar germes e remover detritos. No modo “cura”, conhecido como M2, liberam sinais calmantes que aquietam a inflamação e promovem a reparação tecidual. Uma resposta saudável começa com mais células M1 e gradualmente migra para M2 à medida que o perigo passa. Os autores queriam saber se o α7nAChR, um receptor originalmente famoso por seu papel na comunicação nervosa e nos efeitos da nicotina no cérebro, também ajuda a orientar os macrófagos para esse estado de cura M2 durante a inflamação.
Um interruptor ligado aos nervos que favorece a cura
Para investigar isso, os pesquisadores usaram camundongos que tinham ou não o α7nAChR e desencadearam inflamação na cavidade abdominal de duas maneiras: com um componente bacteriano (mimetizando infecção) e com manipulação intestinal suave (mimetizando lesão cirúrgica estéril). Eles mediram marcadores moleculares que distinguem o comportamento M1 do M2 e usaram citometria de fluxo para contar as proporções de cada tipo de macrófago. Em camundongos normais, a fase inicial da inflamação foi dominada por sinais M1, mas ao longo dos um a dois dias seguintes, os marcadores de células M2 aumentaram, refletindo uma mudança natural para o reparo. Em camundongos sem α7nAChR, contudo, os marcadores pró‑inflamatórios foram mais altos, os marcadores de cura foram mais baixos, e a proporção de macrófagos M2 na área inflamada foi consistentemente reduzida, inclinando o equilíbrio local para um estado mais danoso, dominado por M1.
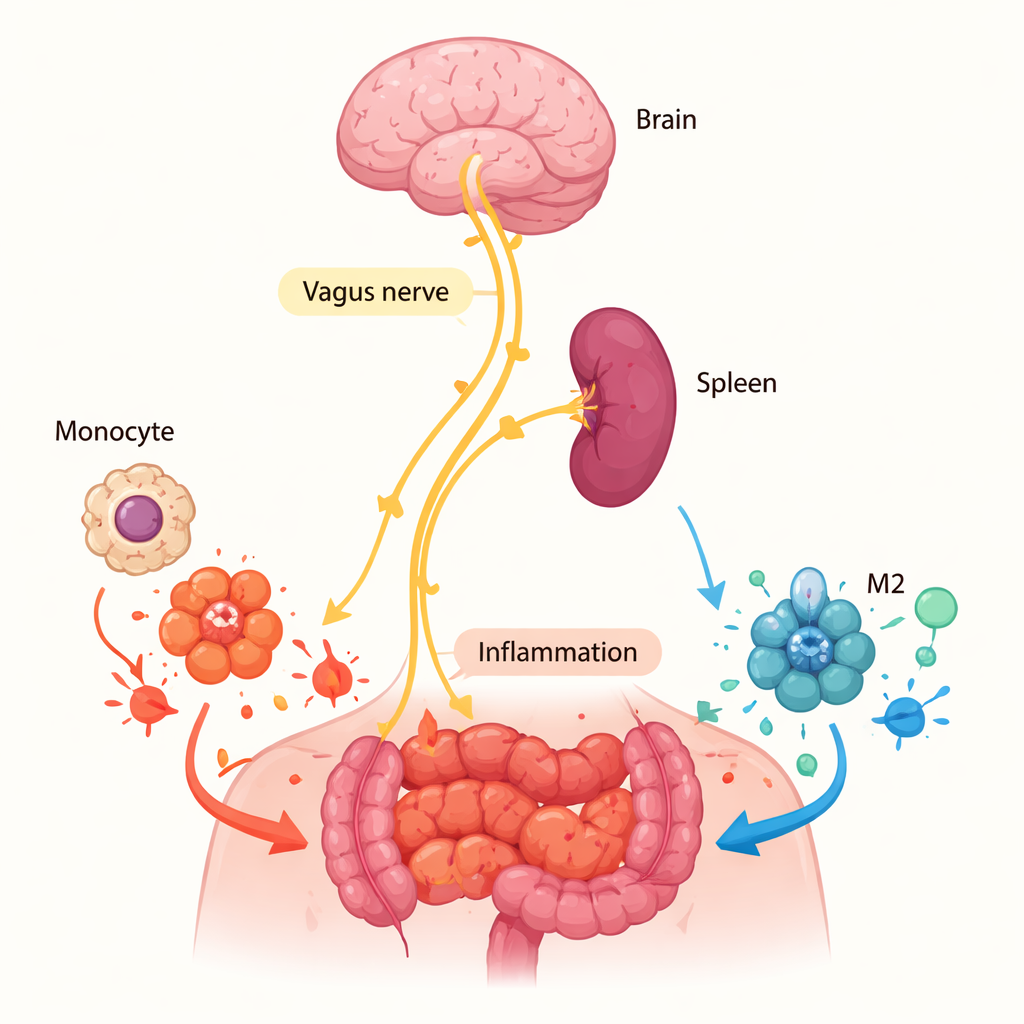
Por que o baço importa mais do que a ferida
A equipe então perguntou onde o α7nAChR estava desempenhando esse papel. Poderia ter atuado diretamente no sítio inflamatório se células locais estivessem liberando acetilcolina, o químico que ativa o receptor. Mas medições de acetilcolina no líquido abdominal e em culturas celulares do tecido inflamado praticamente não detectaram sinal local forte, o que vai contra essa hipótese. Em vez disso, a atenção voltou-se para o baço, um órgão imune chave já conhecido por participar de uma “via colinérgica anti‑inflamatória” controlada pelo nervo vago. Quando os pesquisadores removeram cirurgicamente o baço de camundongos normais e então induziram inflamação abdominal, a proporção de macrófagos M2 na cavidade peritoneal caiu, e o número total de macrófagos diminuiu. Esse padrão espelhou o observado em camundongos sem α7nAChR, sugerindo que sinais conduzidos por nervos no baço preparam monócitos — os precursores dos macrófagos — para tornarem‑se células M2 antes mesmo de chegarem ao tecido inflamado.
Testando o interruptor em células humanas
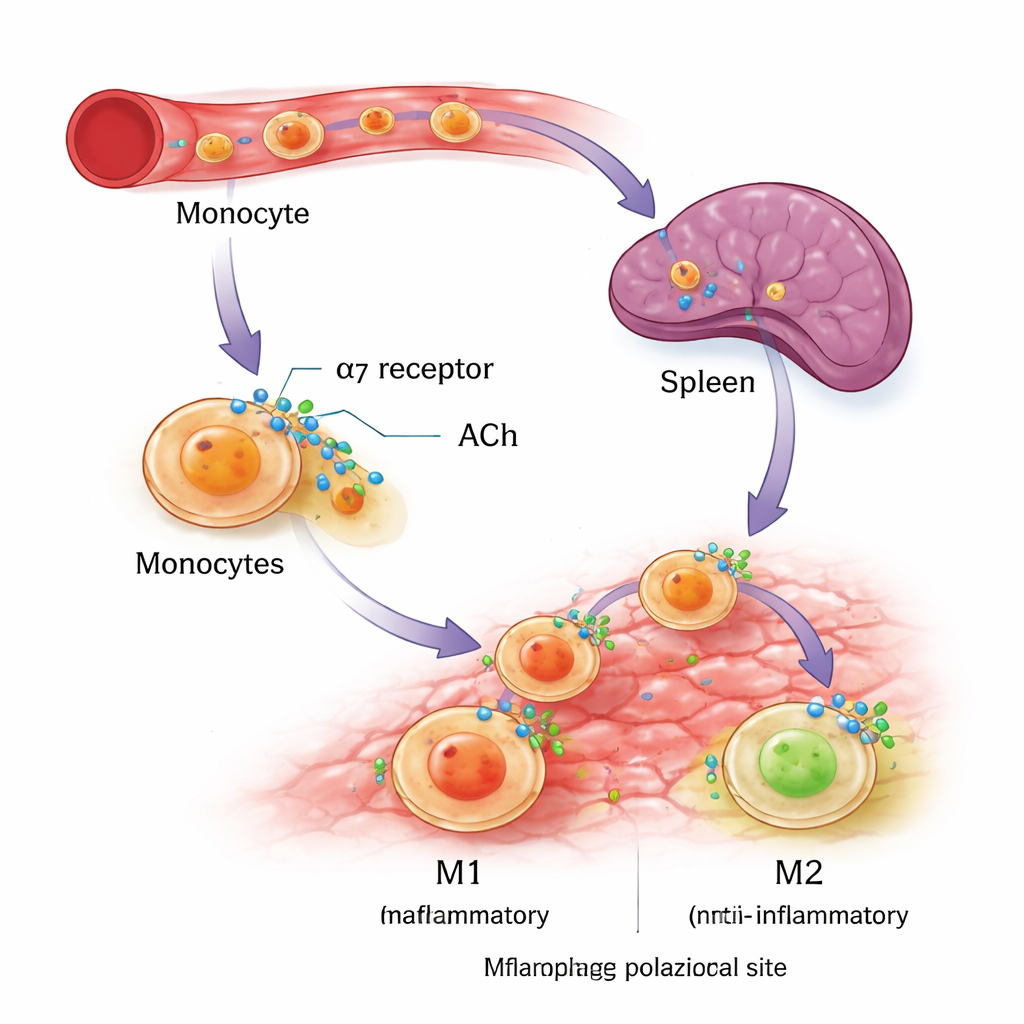
Para verificar se o mesmo receptor pode modular células humanas, os cientistas usaram monócitos cultivados em laboratório a partir de uma linha leucêmica (THP‑1) e de sangue doado por humanos. Eles induziram esses resultados a se diferenciarem em macrófagos M1 ou M2 usando sinais imunes padrão e depois adicionaram um fármaco que ativa especificamente o α7nAChR. Em ambas as fontes de células humanas, ativar o α7nAChR não aumentou marcadores M1, mas elevou claramente marcos-chave do comportamento M2, incluindo a proteína de superfície CD206 e a molécula anti‑inflamatória interleucina‑10. Esses experimentos apoiam a ideia de que o α7nAChR age como um interruptor de polarização, facilitando que macrófagos em desenvolvimento adotem uma identidade de reparo sem simplesmente desligar a resposta imune por completo.
De pistas sobre a nicotina a terapias futuras
Os achados ajudam a explicar várias observações intrigantes, como por que estimular o nervo vago pode melhorar doenças inflamatórias e por que fumantes, apesar de muitos riscos à saúde, parecem ter um risco um pouco menor de certas condições intestinais — a nicotina pode ativar o α7nAChR. Em vez de apenas bloquear moléculas inflamatórias, o α7nAChR parece ajudar o corpo a converter suas equipes de limpeza imunológica em células M2 mais focadas no reparo, particularmente por meio do treinamento de monócitos no baço. Para um leigo, isso significa que nosso sistema nervoso faz mais do que perceber dor ou controlar músculos; ele também orienta discretamente as células imunes a saber quando combater e quando curar. Aprender a acionar com segurança esse interruptor interno com drogas ou estimulação nervosa direcionada pode abrir novas formas de acalmar a inflamação nociva preservando a capacidade do corpo de se defender.
Citação: Mihara, T., Tanabe, H., Nonoshita, Y. et al. The role of the α7 nicotinic acetylcholine receptor in promoting M2 macrophage polarization at inflammatory sites. Sci Rep 16, 5267 (2026). https://doi.org/10.1038/s41598-026-35757-2
Palavras-chave: polarização de macrófagos, inflamação, nervo vago, receptor nicotínico de acetilcolina, regulação imune