Clear Sky Science · pt
Formas fisiologicamente relevantes dos traçadores radioativos Tc- e Re-pirofosfato e a base de sua sensibilidade aos amiloides de transtirretina
Por que essa história de imagem do coração importa
Muitas pessoas desenvolvem depósitos silenciosos de proteínas mal dobradas, chamados amiloides, no coração à medida que envelhecem. Alguns desses depósitos, especialmente aqueles formados a partir de uma proteína sanguínea chamada transtirretina, podem tornar o coração mais rígido e levar a doença grave. Os médicos recorrem cada vez mais a um radiotraçador conhecido como pirofosfato de tecnécio‑99m (99mTc‑PYP) para visualizar esses depósitos em exames. Ainda assim, surpreendentemente, a forma exata desse traçador no organismo e por que ele parece “preferir” certos tipos de amiloide não estavam claras. Este artigo combina teoria e experimento para revelar como o traçador realmente se apresenta em condições fisiológicas e como essa forma pode permitir que ele se dirija a fibrilas de transtirretina prejudiciais.
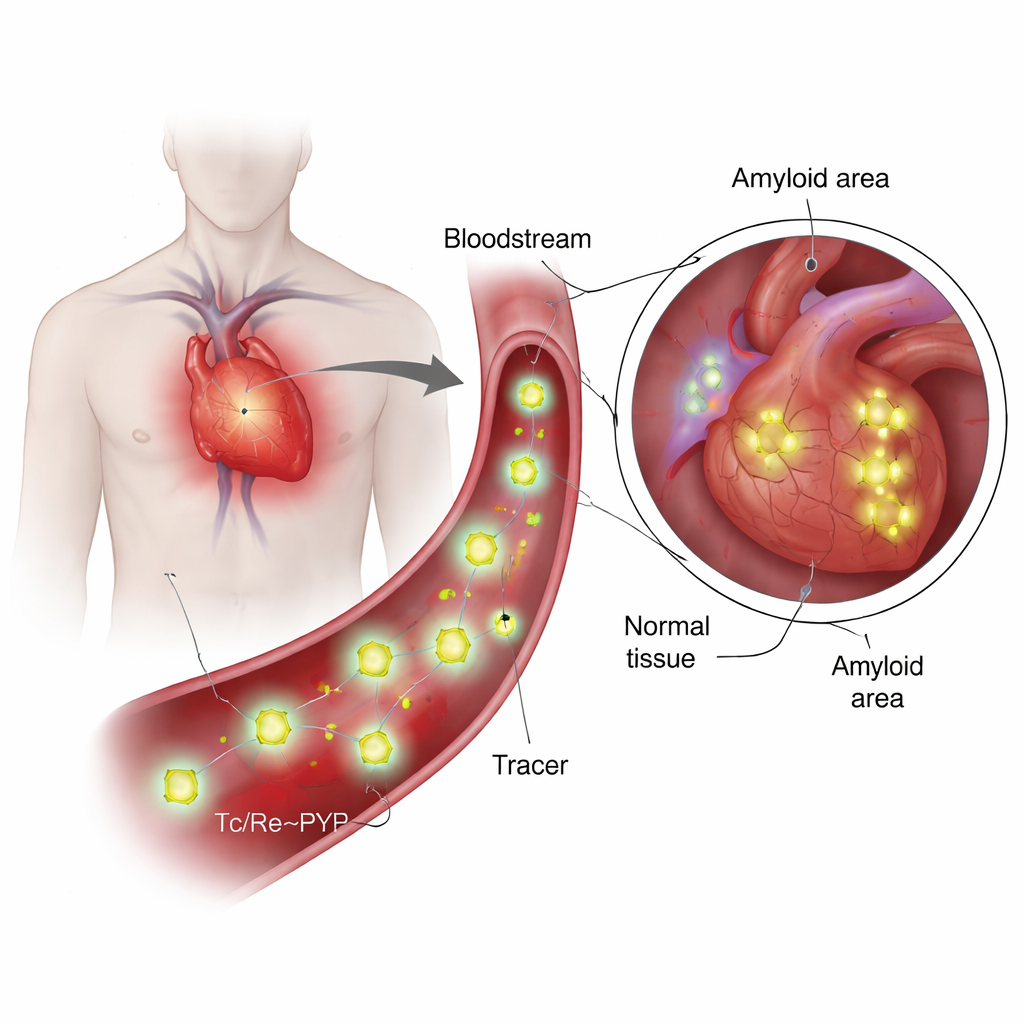
O que são esses traçadores e por que são especiais?
O 99mTc‑PYP tem sido usado por décadas para imagem óssea, porque tende a se acumular onde o cálcio e a renovação mineral são altos. Mais recentemente, os clínicos descobriram que ele também pode distinguir entre dois tipos principais de amiloidose cardíaca: uma formada por cadeias leves de anticorpos (AL) e outra por transtirretina (ATTR). No ATTR, o coração costuma aparecer com sinal forte nas varreduras com PYP, enquanto os casos AL tendem a permanecer com sinal fraco, mesmo quando o acúmulo de cálcio parece semelhante. Essa discrepância levantou uma questão central: o traçador está aderindo apenas ao cálcio, ou está interagindo diretamente com a proteína amiloide? Responder isso requer conhecer a verdadeira estrutura química do traçador em condições semelhantes às do sangue, algo que trabalhos anteriores apenas esboçaram de forma ampla.
Usando um substituto mais seguro para ver o invisível
Porque o tecnécio é radioativo e está presente apenas em quantidades minúsculas nas preparações médicas, é difícil estudá‑lo diretamente com muitas técnicas de laboratório. Os autores, portanto, usaram rênio, um elemento intimamente relacionado com tamanho e preferências de ligação quase idênticas mas com química mais conveniente, como substituto. Eles prepararam misturas de rênio‑pirofosfato em condições que imitam os kits clínicos de PYP e então as sondaram com um conjunto de ferramentas: cálculos quânticos de alto nível, absorção no ultravioleta‑visível, várias espectroscopias vibracionais (infravermelho e Raman), ressonância magnética nuclear, espectrometria de massa e espectroscopia Mössbauer do estanho. Juntos, esses métodos permitiram testar muitos candidatos estruturais e reduzir quais espécies são prováveis em pH neutro, como o do sangue.
Uma forma molecular flexível, mas reconhecível
As evidências combinadas apontam para um “núcleo” comum: um complexo octaédrico no qual um átomo de tecnécio ou rênio no estado de oxidação +4 está ligado a dois grupos pirofosfato e duas moléculas de água. Em termos simples, o metal fica no centro de uma gaiola quase octaédrica formada por átomos de oxigênio, com os pirofosfatos atuando como âncoras multifacetadas e as moléculas de água ocupando as posições restantes. Essa unidade básica diaqua dipirofosfato não é rígida. Como os braços do pirofosfato podem girar e formar ligações de hidrogênio internas com as águas ligadas, a molécula assume muitas formas ligeiramente diferentes em solução. Cálculos e espectros sugerem que essas variações deslocam seus padrões de absorção de luz e assinaturas vibracionais, explicando por que as bandas experimentais são largas e por que estudos anteriores tiveram dificuldade em definir uma estrutura única e limpa.
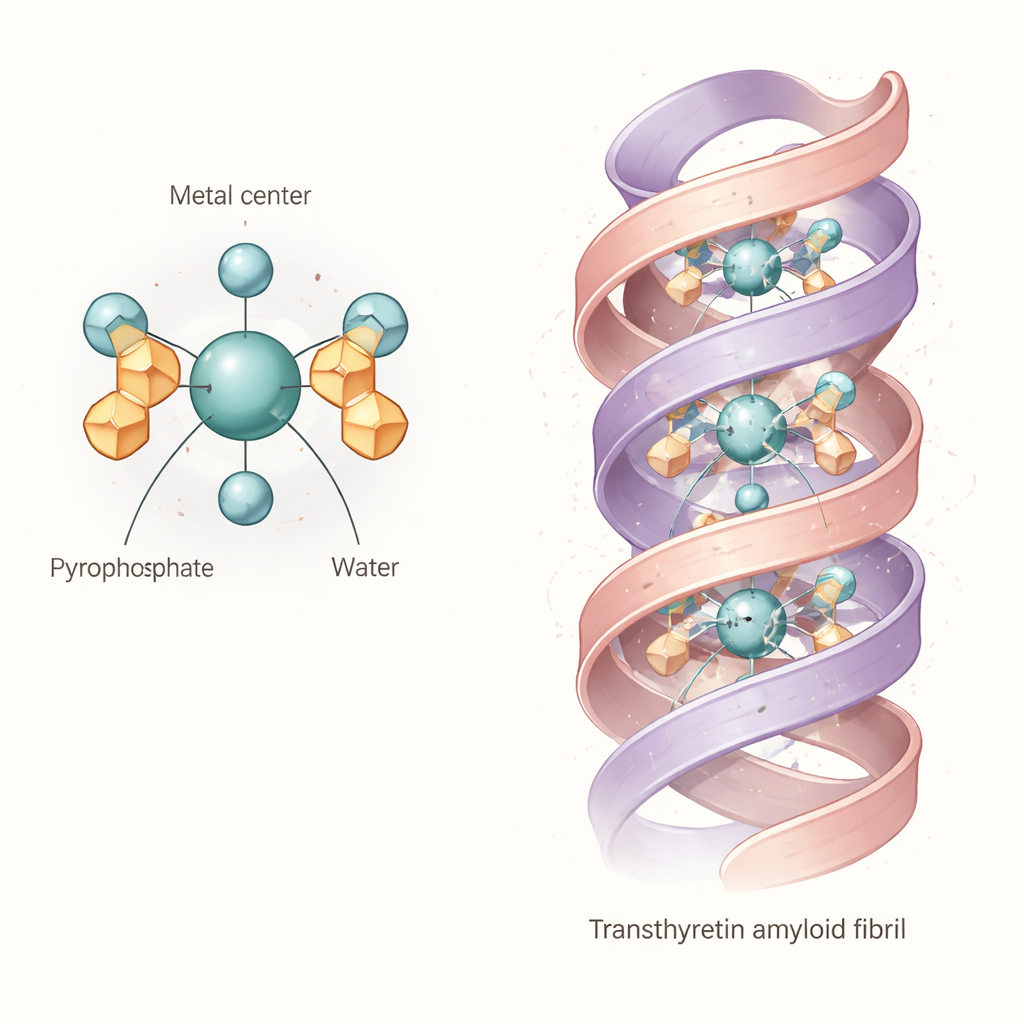
O que isso significa para a ligação ao amiloide cardíaco
Os autores então perguntaram se esse complexo flexível poderia plausivelmente encaixar diretamente nas fibrilas de transtirretina. Usando uma estrutura detalhada por criomicroscopia eletrônica de uma fibrila humana de transtirretina, eles realizaram buscas de acoplamento computacional com o complexo modelado de tecnécio‑pirofosfato. Os resultados mostram que a unidade diaqua dipirofosfato pode caber em um canal central que percorre a fibrila, formando múltiplas ligações de hidrogênio e pontes salinas com cadeias laterais carregadas que revestem a cavidade. Isso sugere que, pelo menos para algumas conformações de fibrilas de transtirretina, o traçador não está apenas marcando depósitos minerais nas imediações; ele pode ser apreendido diretamente pela estrutura proteica. A maleabilidade estrutural do traçador provavelmente o ajuda a se adaptar a bolsões e padrões de cargas ligeiramente diferentes nas fibrilas de pacientes reais.
Implicações para diagnóstico e traçadores futuros
Para o leitor leigo, a conclusão é que a amplamente usada varredura cardíaca com PYP se baseia em um traçador mais sutil e sensível à proteína do que se pensava anteriormente. Em condições fisiológicas, é melhor concebê‑lo como uma pequena gaiola metal‑pirofosfato que carrega água, capaz de flexionar e formar múltiplos pontos de contato com canais de amiloide de transtirretina. Essa visão ajuda a explicar por que o traçador mostra sinais fortes em algumas doenças amiloides e não em outras, e por que pequenas mudanças na proteína ou em seu ambiente podem causar perdas de sensibilidade difíceis de entender. Ao esclarecer a forma e o padrão de carga do traçador em ação, o estudo estabelece uma base para projetar agentes de imagem ou terapêuticos de próxima geração que reconheçam de forma mais seletiva as fibrilas causadoras de doença no coração e além.
Citação: Simon, K.Z., Béres, K.A., Farkas, A. et al. Physiologically relevant forms of Tc- and Re-pyrophosphate radioactive tracers and the basis of their transthyretin amyloid sensitivity. Sci Rep 16, 6111 (2026). https://doi.org/10.1038/s41598-026-35746-5
Palavras-chave: amiloidose cardíaca, transtirretina, pirofosfato de tecnécio, imagem molecular, química de radiotraçadores